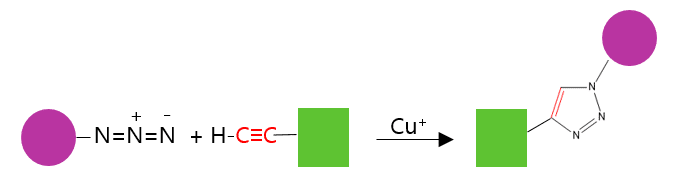1.1 Forskningsfortælling: Klikkemi er nobelpriskemi
Hvordan baner nye kemiske reaktioner vejen for nye lægemidler?

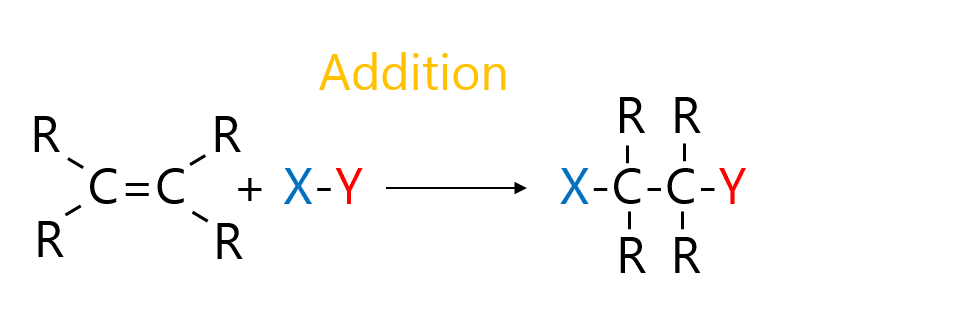
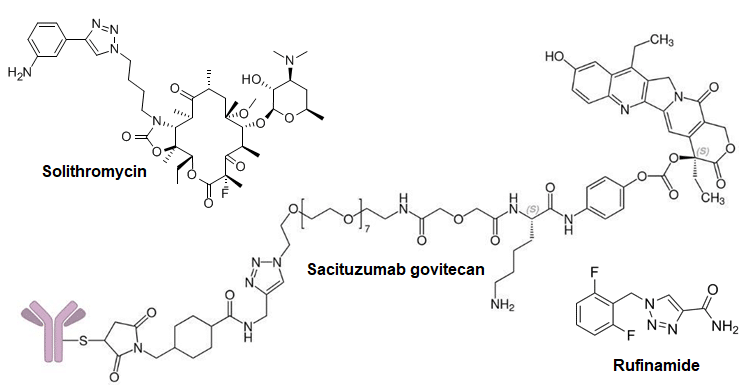
Når nye lægemidler udvikles i dag, er mange af dem udviklet med brug af en relativt ny kemisk reaktion – en klikkemi reaktion. Professor Morten Meldal, fra Kemisk Institut, Københavns Universitet fik tildelt Nobelprisen i kemi i 2022 for sin opdagelse af netop klikkemi. Med Mortens klikreaktion har forskning og industri fået en ny kemisk reaktion. Den har gjort det muligt at binde to eller flere molekyler sammen, helt uden at der dannes andre produkter, illustreret i figur 2.

Klikkemi er et superanvendeligt værktøj inden for områder som materialekemi og medicinalkemi, samt i forskning og udvikling af nye lægemidler. Anvendelsen er bred, fra maling, der bedre binder sig til en overflade, til udvikling af ny medicin og nye behandlingsformer. Med en klikreaktion har kemikeren et værktøj (’click and connect’) til at fremstille store komplekse molekyler.
Som mange andre store opdagelser, var den ikke planlagt. Christian Tornøe, der var Mortens ph.d-studerende, udtaler at ’hvis ikke der havde været plads til at fejle, havde vi ikke haft en modtager af nobelprisen i kemi i 2022’. Morten og Christian undersøgte tilbage i 2001 en fejlslagen kemisk reaktion, hvor der var dannet et helt andet produkt end det forventede. En undersøgelse af de ’fejlslagne forsøg’ ledte dem på sporet af klikkemi. Det viste sig, at de havde opdaget en ny type reaktion.
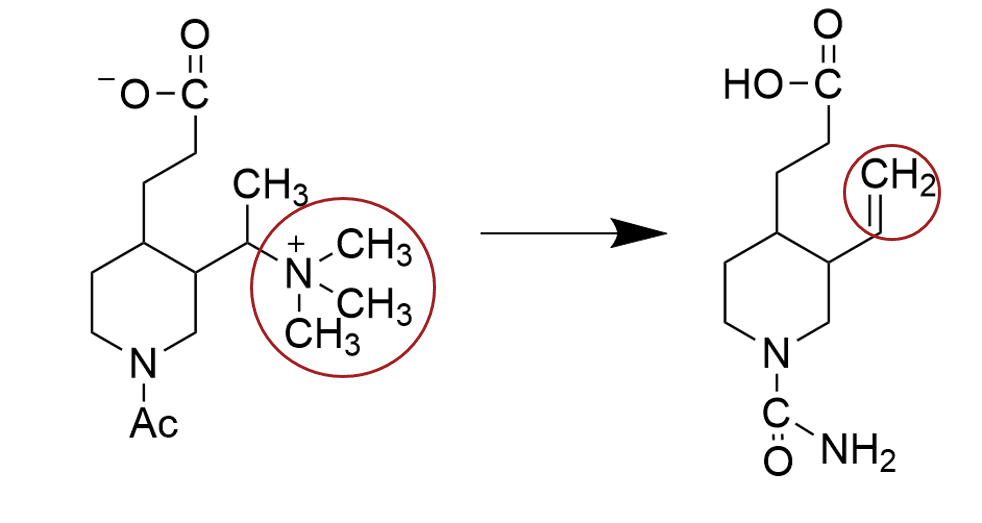
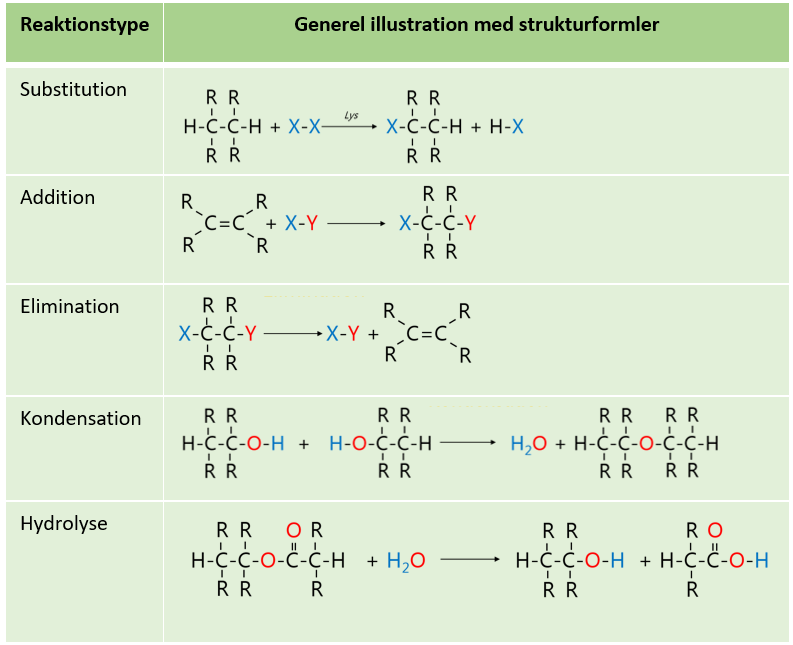
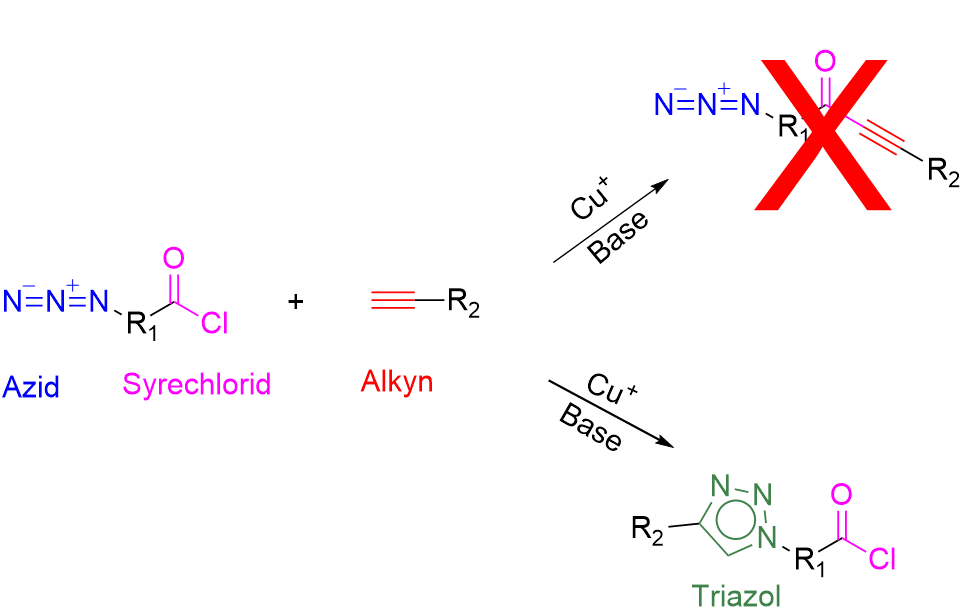
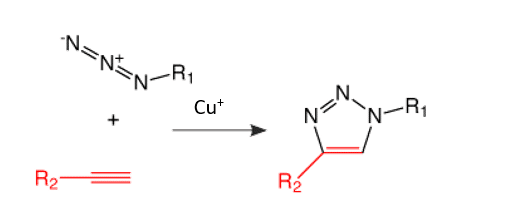
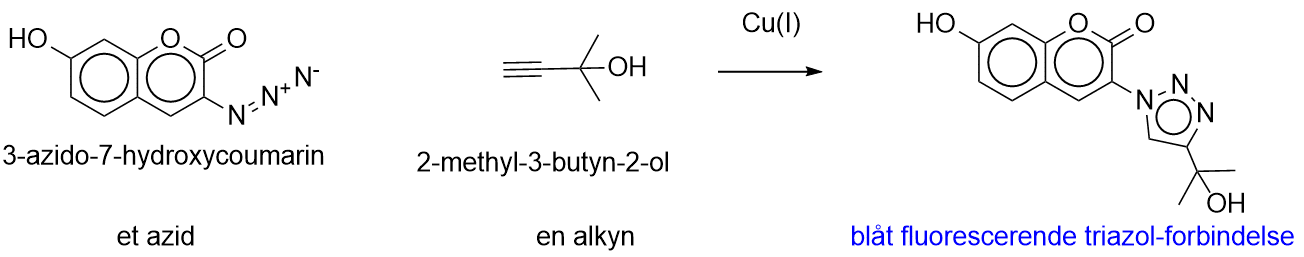
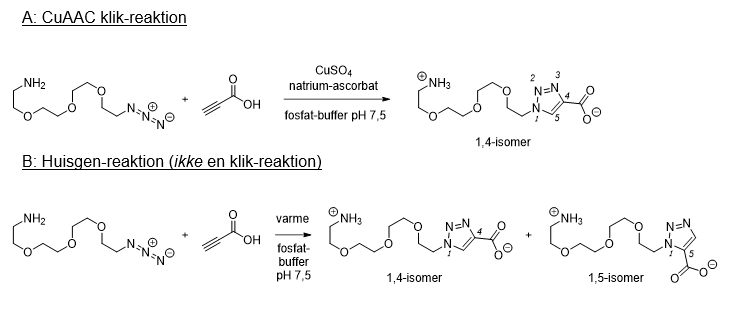
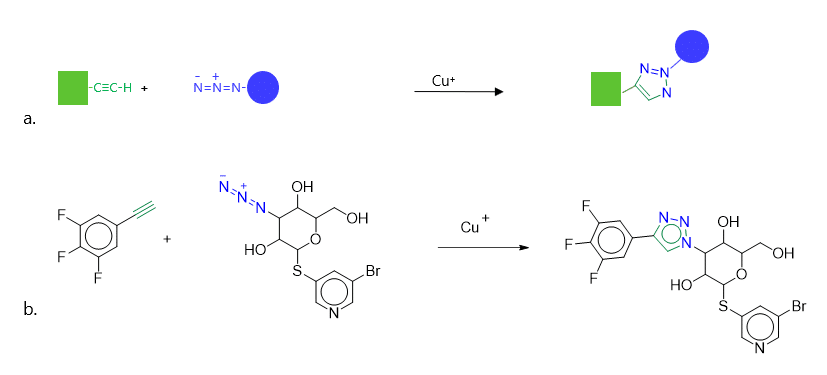
Kemisk kan man beskrive figur 2 lidt mere uddybende, som det er gjort i figur 3: De funktionelle grupper, alkynen (en carbon-carbon tripelbinding) og en funktionel gruppe du nok ikke kender, som hedder et azid (en funktionel gruppe, der udgøres af en lineær zwitter ion med tre nitrogenatomer: -N=N+=N−), gav ét produkt
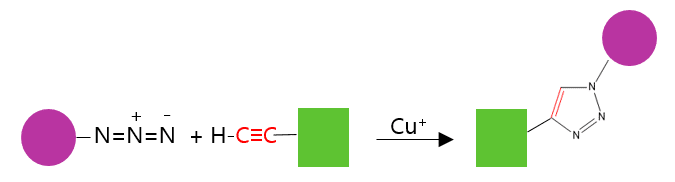
Den brede anvendelse af klikkemi viser at ’kemi er helt centralt i at løse nutidens og fremtidens globale udfordringer, herunder klimakrisen og bidrager til den grønne omstilling’ som Morten udtaler. Han modtog Nobelprisen sammen to andre forskere Barry Sharpless og Carolyn Bertozzi. Morten er den tiende forsker fra Københavns Universitet, der modtog Nobelprisen.
Se mere