Glæd dig til dette nye tema er klar! Materialet er under udarbejdelse og lægges løbende ud i løbet af foråret, når det er klart.
1 Er der kemi i luften?
Ja, for alt er kemi! Men vi kender ikke al kemi – langt fra! Og al den kemi, vi kender, forstår vi ikke det hele af! Så der findes stadig en masse kemiske gåder, som vi som mennesker endnu ikke har løst. Måske bliver du en af dem, der hjælper med at løse nogle af de kemiske gåder. I dette tema møder du en af gåderne. Og du møder nogle forskere, der forsøger at løse dele af den. Prøv at kigge op! Atmosfæren er en stor samling af molekyler og partikler, som reagerer med hinanden og sollyset. Vi ved stadig meget lidt om disse kemiske reaktioner. Men ved at blive klogere på den grundlæggende atmosfærekemi kan vi bedre forstå, hvordan menneskers aktiviteter påvirker atmosfæren og måske på sigt forudsige og mindske de kemiske ændringer, der påvirker klimaet og luftkvaliteten.
2 Atmosfærens kemiske sammensætning
I figur 1 kan du se et udvalg af, hvilke gasser der findes i atmosfæren, og i hvilke koncentrationer.
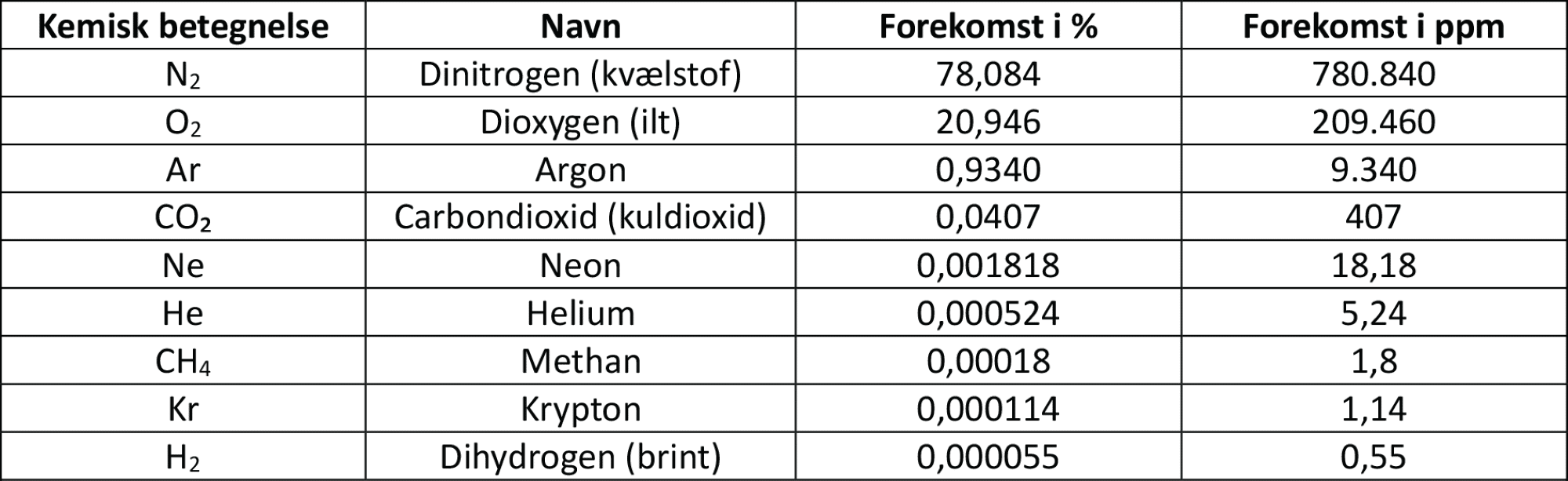
Nogle af gasserne er reagerer nærmest ikke eller slet ikke pga. deres stabile elektronstruktur, andre reagerer lettere. Nogle af gasserne har flere roller afhængig af de omgivelser, de befinder sig i. Nedenfor kan du læse mere om udvalgte gasser i atmosfæren, hvor du blandt andet lærer om deres opbygning og elektronstruktur. Her vil du også møde nogle drivgasser, som ikke er med i figur 1.
Navn:
Dinitrogen er navnet, du bruger i kemi, for det siger noget om molekylets opbygning. Molekylet kaldes i daglig tale også for kvælstof, da man fandt ud af, at dyr blev kvalt, hvis de opholdt sig i en beholder uden dioxygen men med et stort indhold af dinitrogen.
Bindingstyper:
Elektronparbindinger, også kaldet kovalente bindinger, holder atomerne sammen.
De to nitrogenatomer er bundet sammen med en trippelbinding. I figur 2 ses det i elektronprikformlen, at hvert nitrogenatom deler 6 elektroner med det andet nitrogenatom, og da der netop skal to elektroner til for at danne en binding, svarer det til en trippelbinding. Dermed opfyldes oktetreglen for begge atomer i molekylet.
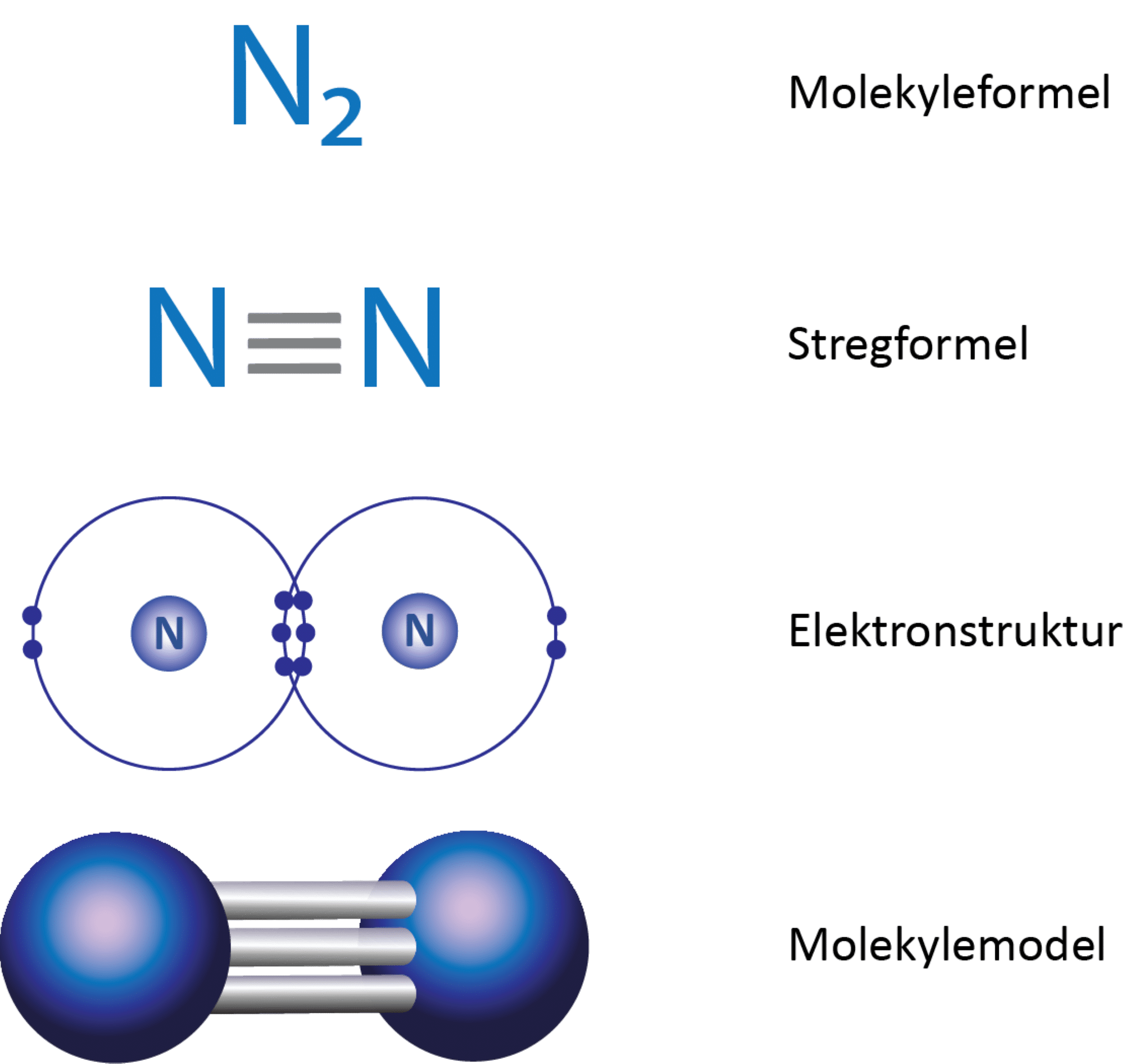
Opbygning:
Dinitrogen er et diatomigt molekyle og er derfor lineært. Molekylet er upolært, da atomerne er ens og derfor har samme elektronegativitet. Dermed bliver forskellen i elektronegativitet nøjagtigt 0:
EN(N) = 3,0
ΔEN = 0,0
Fysiske og kemiske egenskaber:
I figur 3 ses forskellige fysiske egenskaber for dinitrogen. Da molekylet er upolært, opløses der ikke meget af gassen i vand ved stuetemperatur. Jo højere temperatur vandet har, jo mindre dinitrogen kan der opløses deri.

Elektronstrukturen for dinitrogen er meget stabil, og derfor er molekylet ikke særlig reaktivt.
Fun facts:
Flydende nitrogen (som selvfølgelig hedder dinitrogen i kemitimerne i gymnasiet) fascinerer, fordi det kombinerer ekstrem kulde med spektakulære virkninger og praktiske anvendelser. Når det udsættes for luft eller varme, skabes dramatisk ’røg’, der er en synlig påmindelse om fysisk og kemisk vekselvirkning. Samtidig anvendes flydende nitrogen i gastronomi for at skabe nye teksturer og smagsoplevelser, og på hospitaler, hvor vævsprøver fryses ned og kan opbevares i meget lang tid. Her kan du læse og se et par eksempler på nogle sjove anvendelser af flydende nitrogen:
1. Ekstremt koldt
Flydende nitrogen har en temperatur på ca. –196 °C. Det er koldt nok til at fryse blomster sprøde som glas på få sekunder. Og hvis du putter en oppustet ballon ned i den flydende nitrogen, klapper den helt sammen, fordi luften indeni bliver så kold, at den fylder meget mindre. Når du så tager ballonen op igen, puster den sig selv op, efterhånden som den bliver varmere. Dette sker, fordi volumen af en gas er omvendt proportional med temperaturen. Du kan søge på YouTube og finde sjove film af dette.
2. ’Magisk’ damp
Når man hælder flydende nitrogen ud, ser det ud som om der kommer røg. Men det er faktisk ikke dinitrogen men vanddamp fra luften, der kondenserer i kulden. Du kan her se Peter Hald, sikkerhedsleder på Institut for Kemi, AU, hælde flydende nitrogen op i en beholder, hvor vanddampen er tydelig. Endnu mere tydeligt bliver det, når han hælder kogende vand ned til den flydende nitrogen.
3. Biologi og medicin
Flydende nitrogen bruges til at opbevare biologiske prøver meget koldt, fx sædceller, ægceller og væv, fordi den lave temperatur stopper alle biologiske processer. Måske har du som i figur 4 også prøvet at få fjernet en fodvorte hos lægen, hvor de har brugt flydende nitrogen.

4. Gas fylder mere end væske
Hvis flydende nitrogen opbevares i en lukket beholder, kan trykket stige voldsomt, fordi væsken fordamper hurtigt, og det kan ende i en eksplosion. Derfor bruges specielle beholdere. Her kan du se Peter Hald, som viser, hvad der sker, når flydende nitrogen bliver til gas.
Du har fået forskellige oplysninger om dinitrogen ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
Se mere
Navn:
Dioxygen er navnet, du bruger i kemi i gymnasiet, da navnet siger noget om, hvilke atomer molekylet er opbygget af. Molekylet kaldes i daglig tale også for ilt, fordi det nærer ild.
Bindingstyper:
Elektronparbindinger holder atomerne sammen.
De to oxygenatomer er bundet sammen med en dobbeltbinding. I figur 5 ses det i elektronprikformlen, at hvert oxygenatom deler 4 elektroner med det andet oxygenatom, og da der skal to elektroner til for at danne en binding, svarer det netop til en dobbeltbinding. Dermed opfyldes oktetreglen for begge atomer i molekylet.
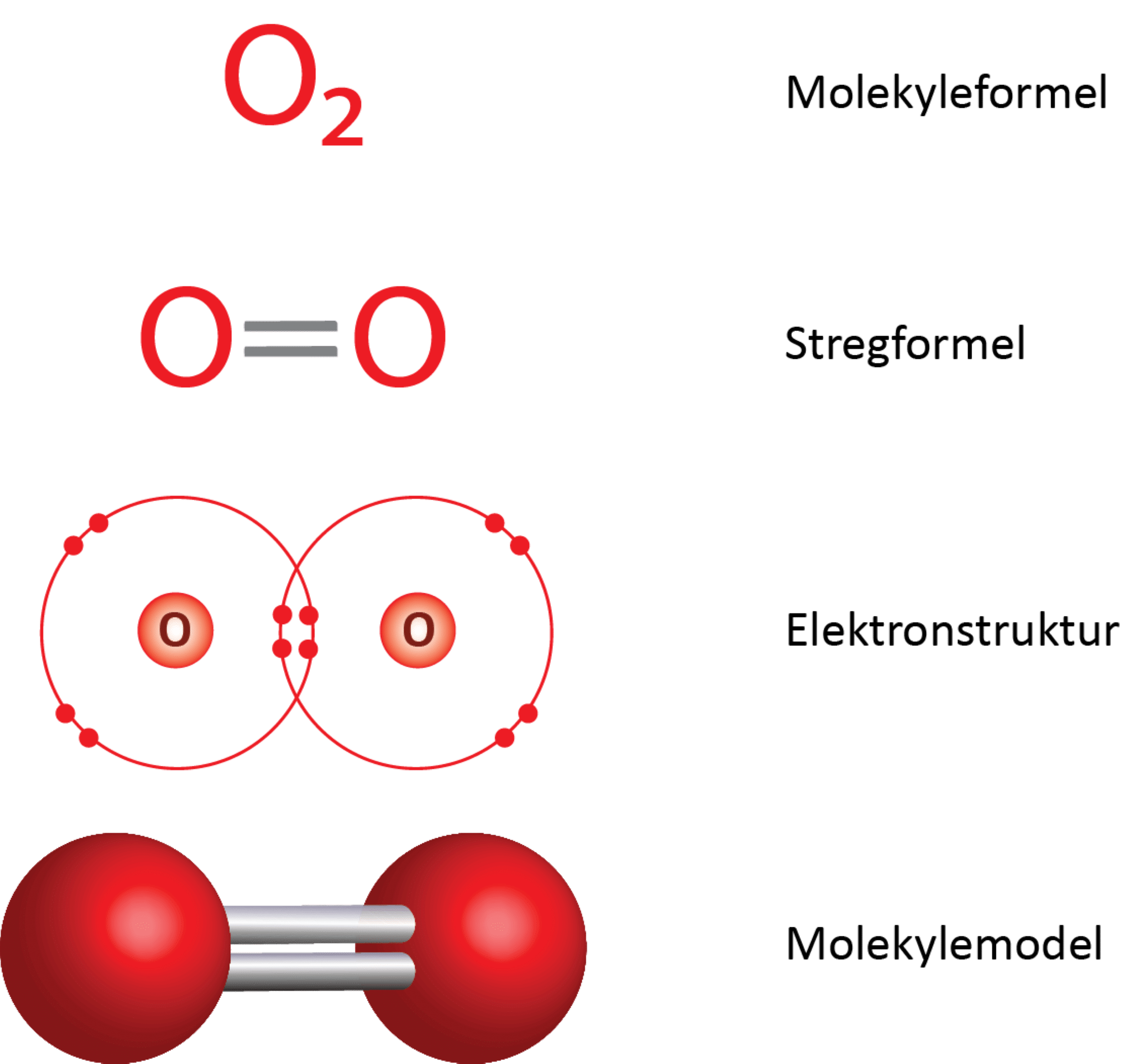
Opbygning:
Dioxygen er et diatomigt molekyle og er derfor lineært. Molekylet er upolært, da atomerne er ens og derfor har samme elektronegativitet. Dermed bliver forskellen i elektronegativitet 0:
EN(O) = 3,5
ΔEN = 0,0
Fysiske og kemiske egenskaber:
I figur 6 ses forskellige fysiske egenskaber for dioxygen. Da molekylet er upolært, opløses der ikke meget af gassen i vand ved stuetemperatur. Men der opløses tilstrækkeligt af gassen i rent vand til, at dioxygen-krævende organismer som dyr og planter kan leve i havet. Jo højere temperatur vandet har, jo mindre dioxygen kan der opløses deri.

Dioxygen er i modsætning til dinitrogen temmelig reaktivt. Hvorfor den store forskel? På B-niveau lærer du om forskellen mellem de to molekyler ud fra deres bindinger: Dinitrogen har en stærk trippelbinding og er derfor meget stabilt, mens dioxygen har en dobbeltbinding og nogle uparrede elektroner, hvilket gør det mere reaktivt.
Hvis du senere får kemi på A-niveau eller læser kemi på universitetet, udvider du din forståelse af atommodeller. Her lærer du om orbitaler og hvordan de overlapper og danner molekylorbitaler. Med den viden kan man forklare mere præcist, hvorfor dioxygen er så reaktivt, mens dinitrogen ikke er.
Fun facts:
1. Uden dioxygen ingen brand!
Før noget kan brænde, kræver det tre ting, som du kan se i brandtrekanten i figur 7.

Fjerner du enten brændstoffet, varmen eller dioxygenen, stopper branden. Når du lægger låg på en gryde, hvor der er gået ild i olien, eller du lukker for vinduerne ved en ildebrand, fjerner du dioxygenen, og ilden går efterhånden ud.
2. Hvorfor trækker vi vejret?
Dioxygen er livsvigtigt for mange levende organismer på jorden. Nu tænker du måske, at det er, fordi vi skal bruge det til at trække vejret. Det er rigtigt nok, men hvorfor trækker vi vejret? Det er, fordi vi skal bruge dioxygenen til at forbrænde vores mad i kroppen, så vi kan få energi ud af det, vi spiser. Det handler om redoxreaktioner, som du kan læse mere om i temaet ’Fremtidens batterier – C-niveau’ eller senere i de reaktioner, der sker i atmosfæren.
3. Ilt skifter farve
Du kan danne flydende dioxygen ved at køle det tilstrækkeligt langt ned ved hjælp af flydende nitrogen, som du kan se her. Selvom det ikke er tydeligt i filmen, er både flydende og fast dioxygen lyseblåt, mens gassen er farveløs.
4. Hvorfor har bjergbestigere brug for iltflasker?
Som du kan se i figur 1 ovenfor, er der ca. 21 % dioxygen i atmosfærisk luft. Det er en koncentration, som vores kroppe har tilpasset sig til, når vi trækker vejret. Men bjergbestigere, som bestiger verdens højeste bjerge som Mount Everest, har som regel iltflasker med, fordi koncentrationen af dioxygen falder, jo længere op i atmosfæren, du kommer. Du kan læse her, hvorfor det som regel er nødvendigt.
Du har fået forskellige oplysninger om dioxygen ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
Se mere
Ædelgasserne befinder sig i 18. gruppe svarende til 8. hovedgruppe i det periodiske system. På nær helium, der har 2 elektroner i yderste skal, har ædelgassernes atomer 8 elektroner i yderste skal. Derfor er de meget stabile og indgår som regel ikke i kemiske reaktioner i luften. Du kan i denne film lære om ædelgasserne og deres anvendelser:
Måske har du lagt mærke til, at elektronerne, der er tegnet i elektronstrukturerne i figur 2 og 5, tegnes parvist sammen. Elektroner tegnes som par, fordi de normalt findes to og to i samme orbital, som du kan lære mere om på A-niveau i kemi. Men i nogle atomer, fx carbon med fire elektroner i yderste skal, er nogle elektroner uparrede, indtil de danner bindinger med andre atomer. Prøv at se starten af filmen igen og se, hvordan elektronstrukturen blev tegnet for ædelgasserne.
Se mere
I Danmark kender de fleste nok bedst helium, som er velegnet til at puste balloner op, som holder sig svævende, fordi helium er lettere end atmosfærisk luft (se figur 8). Nogle mennesker indånder lidt af gassen fra en oppustet ballon som underholdning og får en sjov, lys stemme. Men det frarådes at prøve det, for selvom helium ikke er giftigt, fortrænger det dioxygenen, du har brug for, og dermed kan du blive svimmel og besvime.

Ædelgassen radon er radioaktiv, som du så i filmen. Når man bor i hus, er der risiko for, at radon, som findes i vores undergrund, siver op gennem revner og sprækker bygningernes fundament. Gassen er farveløs og lugter ikke, du ville ikke lægge mærke til den. Radon er den næsthyppigste årsag til lungekræft, og man ved, at omkring 300 i Danmark dør pga. radon om året. Der er heldigvis krav om radonsikring ved bygning af nye boliger, og bor man i en ældre bolig, kan man også få lavet radonsikring, hvis ens bolig ligger i et område af Danmark, der er udsat.
En drivhusgas er en gas i atmosfæren som carbondioxid og methan, som absorberer og udsender varmestråling også kaldet infrarød stråling. Længere nede kan du læse mere om drivhuseffekten, og hvorfor nogle gasser absorberer og udsender varmestråling, mens andre ikke gør. Blandt de mere almindeligt kendte drivhusgasser er carbondioxid og methan. Methan udledes bl.a. fra køer, når de bøvser og prutter, da de har mikroorganismer i deres fordøjelsessystem, som netop producerer denne gas. Blandt mindre kendte drivhusgasser er vand og ozon. Herudover er der dinitrogenmonoxid, som er bedre kendt som lattergas, og CFC-gasser, som er carbonforbindelser med fluor og chlor.
Navn:
Carbondioxid eller kuldioxid er navnet, du bruger i kemi. I gamle dage kaldte man det kultveilte (’tve’ og ’di’ refererer begge til de to oxygenatomer).
Bindingstyper:
Elektronparbindinger, også kaldet kovalente bindinger, holder atomerne sammen.
Hvert oxygenatom er bundet til det centrale carbonatom med dobbeltbindinger. I figur 9 ses det i elektronprikformlen, at hvert oxygenatom deler 4 elektroner med carbonatomet, og da der netop skal to elektroner til for at danne en binding, svarer det til en dobbeltbinding.
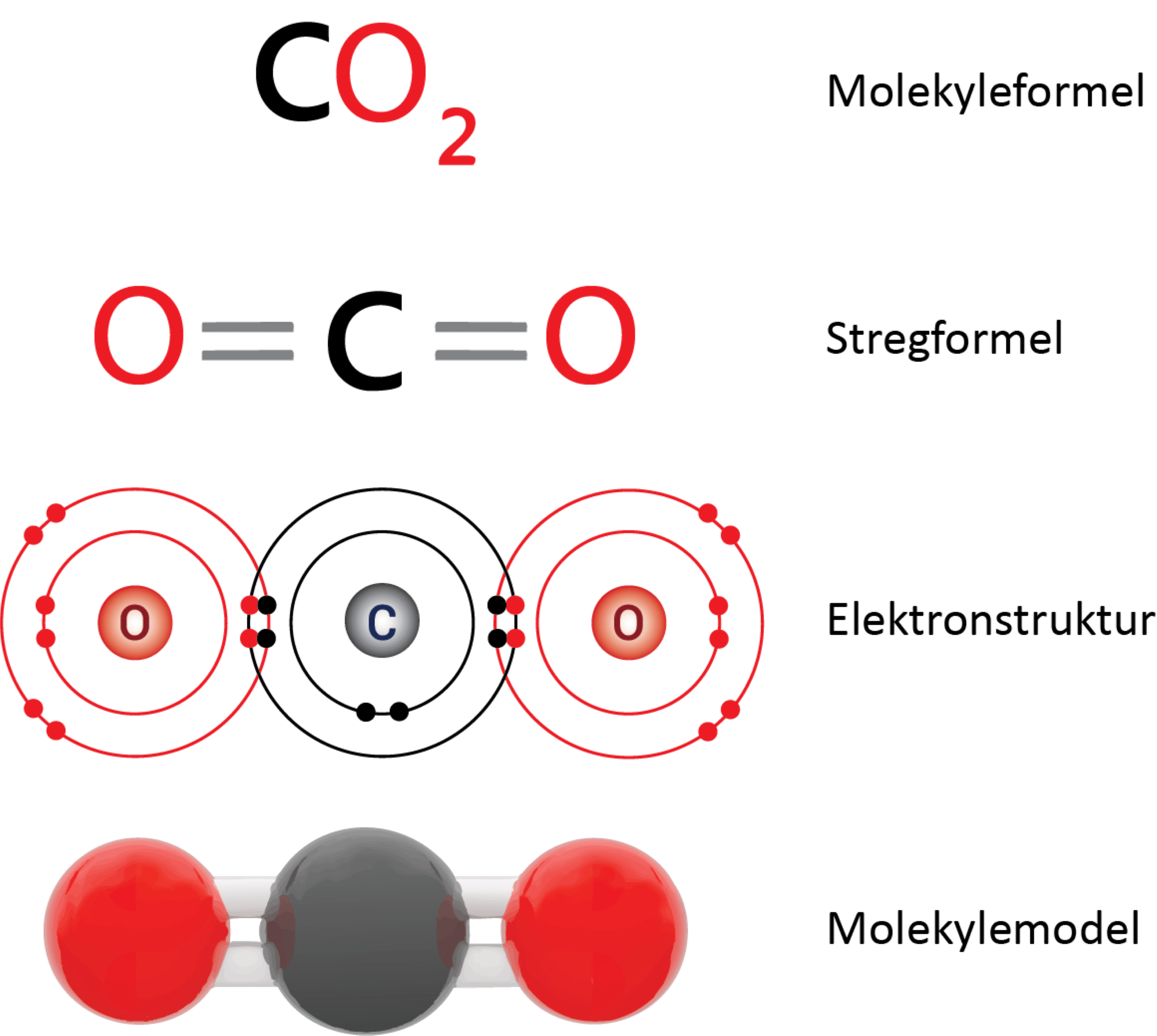
Opbygning:
Molekylet er lineært, hvilket betyder, at alle tre atomers centrum ligger på en ret linje. Herudover er molekylet symmetrisk (se figur 10) og dermed upolært, selvom begge dobbeltbindinger hver især er polære. Det bliver tydeligt, når forskellen i elektronegativitet beregnes:
EN(C) = 2,5
EN(O) = 3,5
ΔEN = 1,0
Fra beregningen kan det konkluderes, at dobbeltbindingerne hver især mellem carbon- og oxygenatomerne er polære.
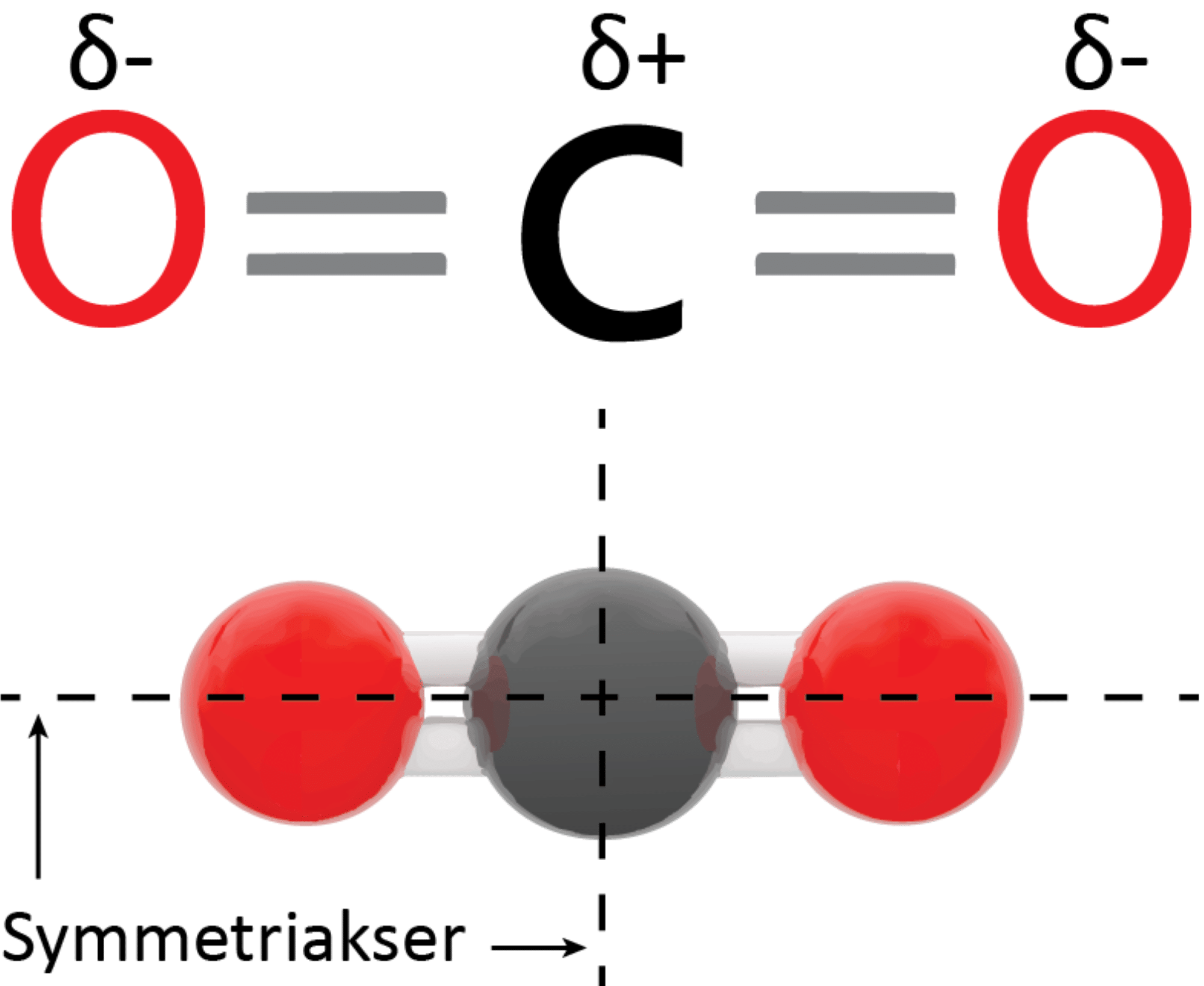
Fysiske egenskaber:
I figur 11 ses forskellige fysiske egenskaber for carbondioxid. Da carbondioxid sublimerer, dvs. går fra fast form direkte til gas uden at være på flydende form, har stoffet ikke et smeltepunkt ved normalt tryk (1 atm.). Koncentrationen af carbondioxid i atmosfæren har været målt i mange år, og her kan du se, hvordan den er steget gennem de sidste cirka 60 år. I år 2000 var koncentrationen af CO₂ i atmosfæren fx 369,71 ppm (parts per million). Opløseligheden af CO₂ i vand afhænger blandt andet af vandets vandets temperatur og er meget højere end for dinitrogen og dioxygen.

Fun facts:
Når carbondioxid er på fast form, kaldes det for tøris. Dette hænger sammen med, at carbondioxid ikke smelter og bliver ’vådt’ ligesom is bliver til vand, før det fordamper. I stedet for sublimerer det. Da det samme antal molekyler på gasform fylder væsentlig mere end på fast form, kan man lave en mekanisk eksplosion, som du kan se Peter Hald fra Aarhus Universitet, udføre her:
Tøris har mange funktioner ifølge et firma, der sælger det:

Du har fået forskellige oplysninger om carbondioxid ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
1. Forklar, hvorfor hvert oxygenatom i carbondioxidmolekylet er bundet til carbon med en dobbeltbinding.
2. Molekylet har to polære bindinger. Hvorfor er CO₂ alligevel upolært?
3. I figur 11 er koncentrationen af carbondioxid i luften angivet 424,61 ppm (volumenkoncentration). Denne værdi skal du omregne til koncentrationsenheden g/L, så du kan sammenligne med opløseligheden af carbondioxid i vand ved 25 °C, der er 1,45 g/L. Til dette skal du bruge idealgasligningen.
Idealgasligningen viser sammenhængen mellem tryk, volumen, stofmængde og temperatur, lyder:![]()
p er gassens tryk i atm, V er gassens volumen i L, n er stofmængden af gassen i mol, T er gassens temperatur i K, og R er en proportionalitetskonstant kaldet gaskonstanten. Den har samme værdi for alle gasser:
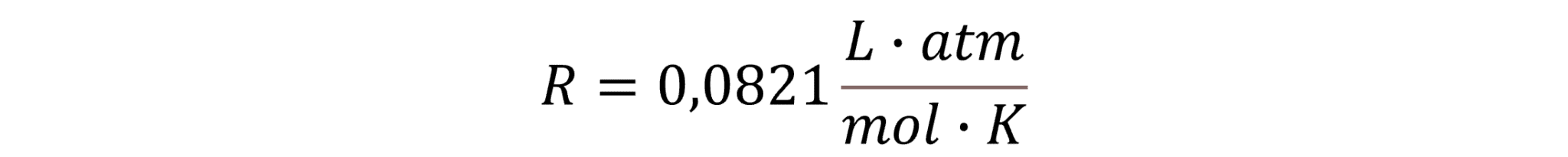
a. Omskriv formlen
![]()
så du har et udtryk for n og indsæt det i idealgasligningen i stedet for stofmængden.
b. Isolér massen, m, i ligningen.
c. Molarmassen, M, for carbondioxid er 44,01 g/mol. Antag at trykket er 1 atm og temperaturen er 25 °C. Omregn temperaturen til enheden K.
d. Koncentrationen af carbondioxid i luften er 424,61 ppm, hvilket betyder, at der er 0,00042461 L CO₂ i 1 L luft. Beregn massen af carbondioxid i 1 L luft.
e. Er koncentrationen af carbondioxid i luft større eller mindre end 1,45 g/L, som er opløseligheden i vand?
4. Hvad fortæller udviklingen i CO₂-udledning i perioden 1940-2024 dig om menneskers påvirkning af atmosfæren? Kan du se en effekt af COVID 19-pandemien?
Se mere
Navn:
Methan er navnet, du bruger uanset om det er i kemitimerne eller udenfor.
Bindingstyper:
Elektronparbindinger holder atomerne sammen.
Det centrale carbonatom har fire enkeltbindinger til hver af hydrogenatomerne. I figur 13 ses det i elektronprikformlen, at hvert hydrogenatom deler 2 elektroner med carbonatomet, og da der netop skal to elektroner til for at danne en binding, svarer det til en enkeltbinding.
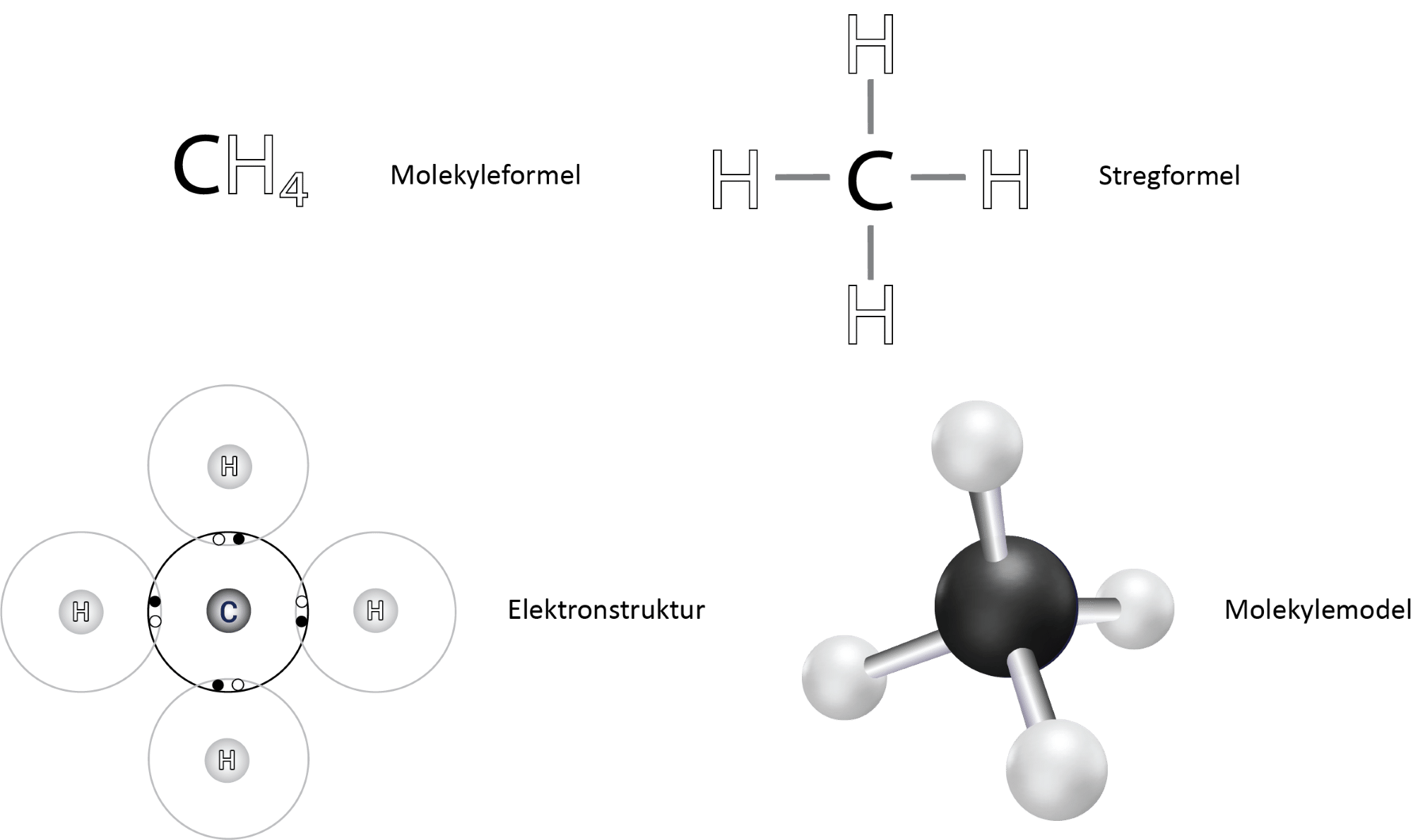
Opbygning:
Bindingsvinklen mellem to bindinger i methan er 109,5°, og med i alt 4 bindinger bliver molekylet et tetraeder. Det betyder, at de fire (tetra) hydrogenatomer danner fire flader. På engelsk er ordet tetrahedron, og hedron er det græske ord for flade. I figur 14 kan du se et tetraeder:

Bindingerne mellem carbon og hydrogen er upolære, da forskellen i elektronegativitet er under 0,5. Du kan læse mere om, hvordan du skelner mellem forskellige typer af kemiske bindinger i temaet ’Den tredje dimension’.
EN(C) = 2,5
EN(H) = 2,1
ΔEN = 0,4
Alle fire bindinger er altså upolære, og herudover er molekylet symmetrisk (se molekylemodellen i figur 13) og dermed bliver molekylet upolært.
Fysiske og kemiske egenskaber:
I figur 15 ses forskellige fysiske egenskaber for methan. Selvom molekylet er upolært, kan der opløses en smule af gassen i vand, men mindre end fx dioxygen. Jo højere temperatur vandet har, jo mindre methan kan der opløses deri.

Methan tilhører gruppen af organiske stoffer, der hedder alkaner, og de er relativt reaktionstræge. De kan dog deltage i en reaktionstype kaldet substitutionsreaktion, som du kan læse mere om i temaet ’Nye lægemidler med et klik’. Herudover brænder stoffet rigtig godt:
CH4(g) + 2 O2(aq) → CO2(g) + 2 H2O(g)
(1)
Når der er dioxygen til stede, dannes der kun carbondioxid og vand ved forbrændingen.
Fun facts:
Døren til helvede
I området Darvaza i Turkmenistan findes ’Døren til helvede’. Det er et stort, brændende krater, der opstod, da man i 1971 borede efter olie og gas i området. I den forbindelse ramte man en stor gaslomme, hvor loftet brasede sammen. Man var bange for, at der kom giftige gasser ud derfra, så man satte ild til det, uden at man havde nogen fornemmelse for, hvor meget gas der var dernede. Lige siden har ilden brændt, men i dag (august 2025) er ilden næsten slukket, da man har tømt gassen ved at bore ned i luftlommen tæt på det åbne krater. Det er godt for klimaet, men landet mister samtidig en stor indtægtskilde, da det brændende krater var landets største turistattraktion. I figur 16 kan du se, hvordan det brændende krater så ud tidligere.

Der er en lang række facts om molekylet, som du sammen med en sidemakker skal finde frem til. I kan finde inspiration her til, hvad I kan søge videre på. I skal finde fem forskellige facts om molekylet, som I bagefter præsenterer for en anden gruppe.
Se mere
Du har fået forskellige oplysninger om methan ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
Se mere
Navn:
Vand er navnet, du bruger uanset om det er i kemitimerne eller udenfor. Hvis du skulle bruge et meget systematisk navn, hedder molekylet også dihydrogenoxid.
Bindingstyper:
Elektronparbindinger holder atomerne sammen.
Det centrale oxygenatom har to enkeltbindinger til hver af hydrogenatomerne. I figur 17 ses det i elektronprikformlen, at hvert hydrogenatom deler 2 elektroner med oxygenatomet, og da der netop skal to elektroner til for at danne en binding, svarer det til en enkeltbinding.
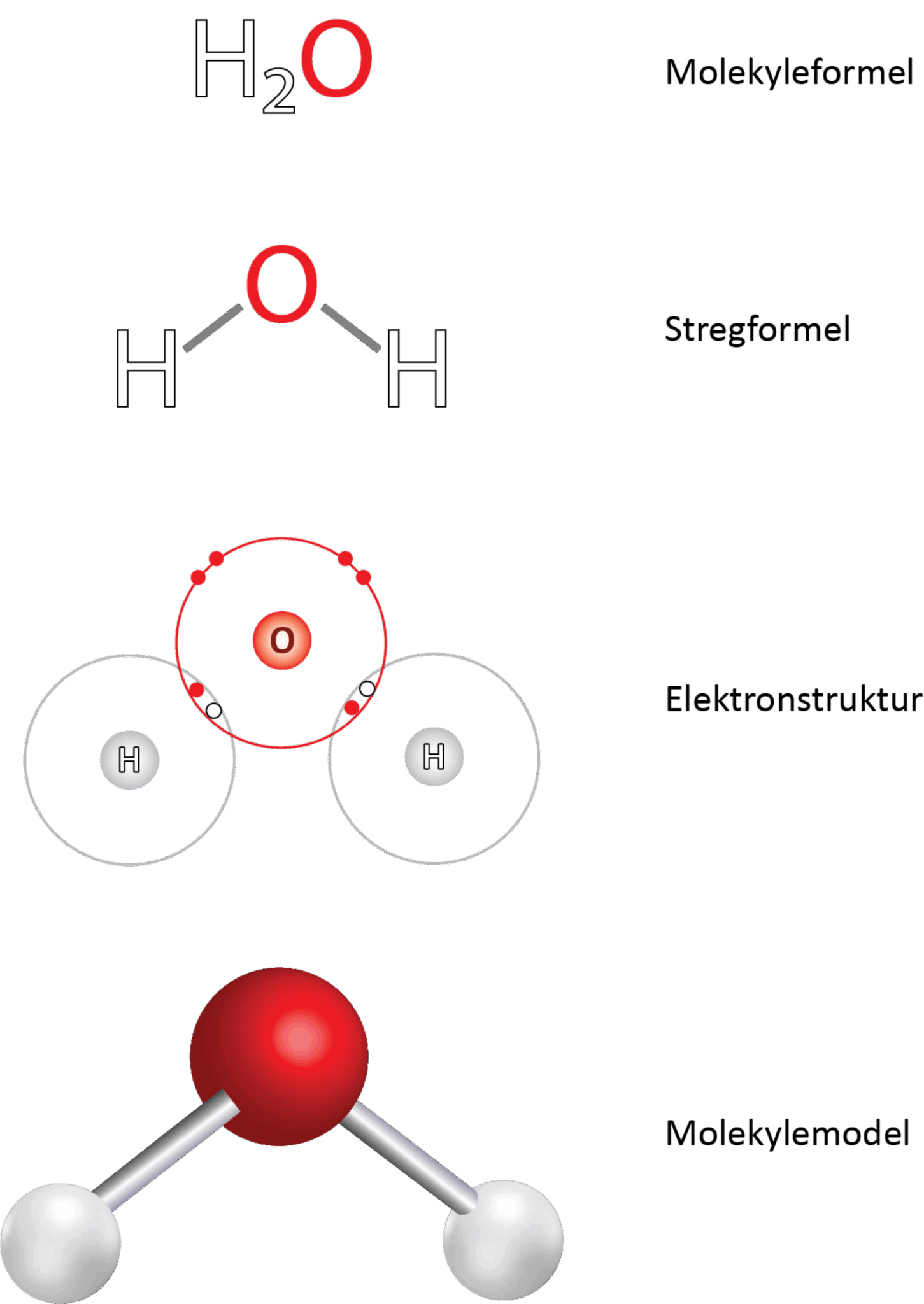
Opbygning:
Bindingsvinklen mellem de to bindinger er 104,5°, så vandmolekylet er vinklet og ikke lineært, som man måske kunne tro. Hvis du har prøvet at bygge molekylet med et molekylebyggesæt, ser det ud til, at molekylet er plant. Et plant molekyle har nemlig alle atomer liggende i et plan. Men oxygenatomet har to frie elektronpar, som du kan se i elektronstrukturen i figur 17, og da elektronpar frastøder hinanden pga. den negative ladning, sidder de længst væk fra de to bindinger til hydrogen som muligt. Elektronskyerne (orbitalerne) for de frie elektronpar er overraskende store, som du kan se i figur 18, og de udgør 2 af de 4 hjørner i et tetraeder, mens de to hydrogenatomer udgør de to andre. Dermed er molekylets opbygning tetraederisk ligesom methan. De to frie elektronpar presser de to enkeltbindinger til hydrogenatomerne lidt tættere på hinanden, så bindingsvinklen bliver en anelse mindre end de 109,5° i methanmolekylet.
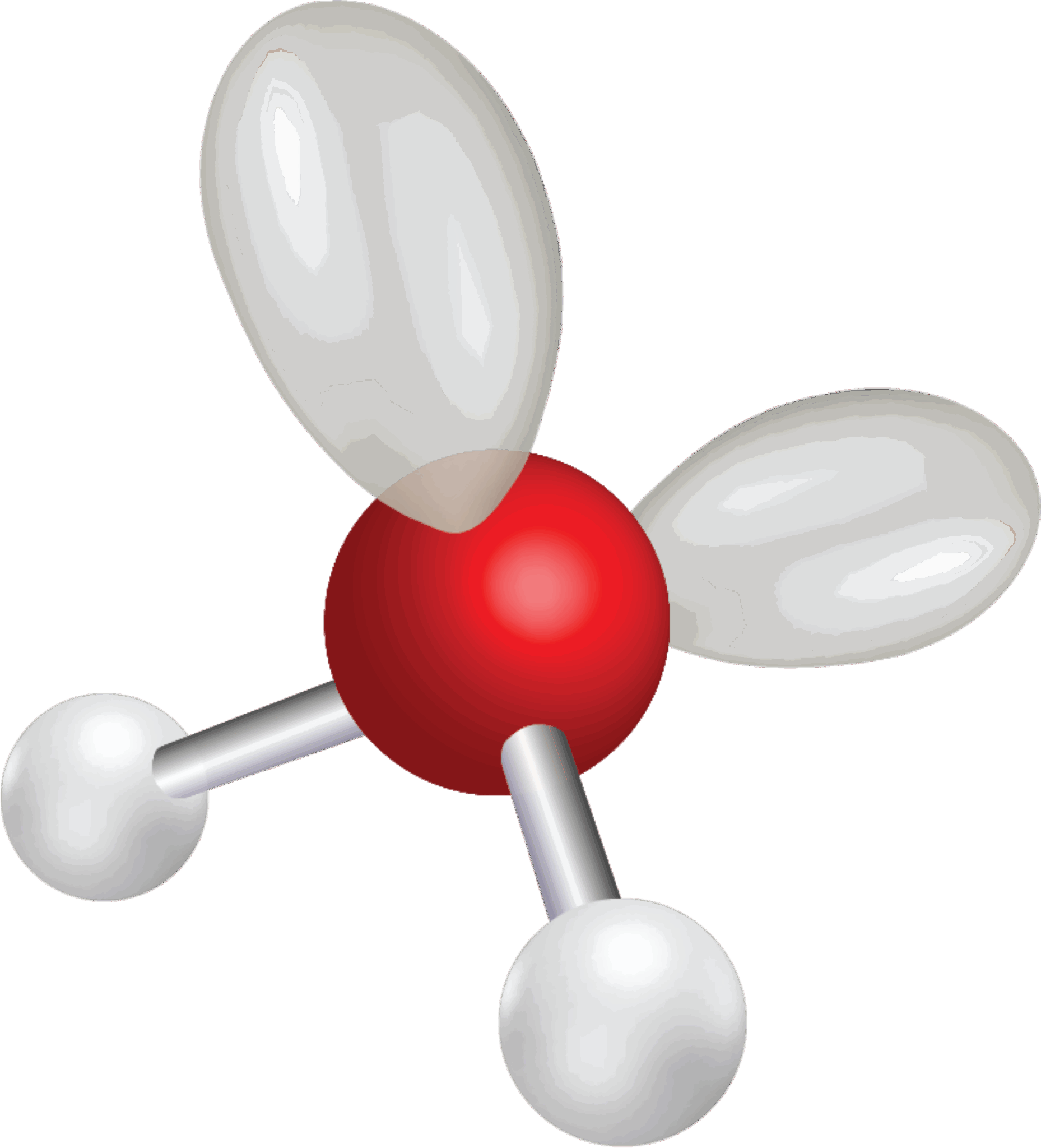
Bindingerne mellem oxygen og hydrogen er polære, da forskellen i elektronegativitet er over 0,5.
EN(C) = 3,5
EN(H) = 2,1
ΔEN = 1,1
Da oxygen har en højere EN-værdi end hydrogen, vil det fælles elektronpar være forskudt mod oxygen for begge hydrogenatomer. Dermed bliver der en øget negativ ladning i den side af molekylet, hvor oxygenatomet er, og der er en øget positiv ladning i den side af molekylet, hvor hydrogenatomerne er. Da der ikke er tale om en hel elektron, men kun en ladningsforskydning, bruger man det græske bogstav, delta (δ), med et plus eller minus bagefter for at angive dette, som du kan se i figur 19.
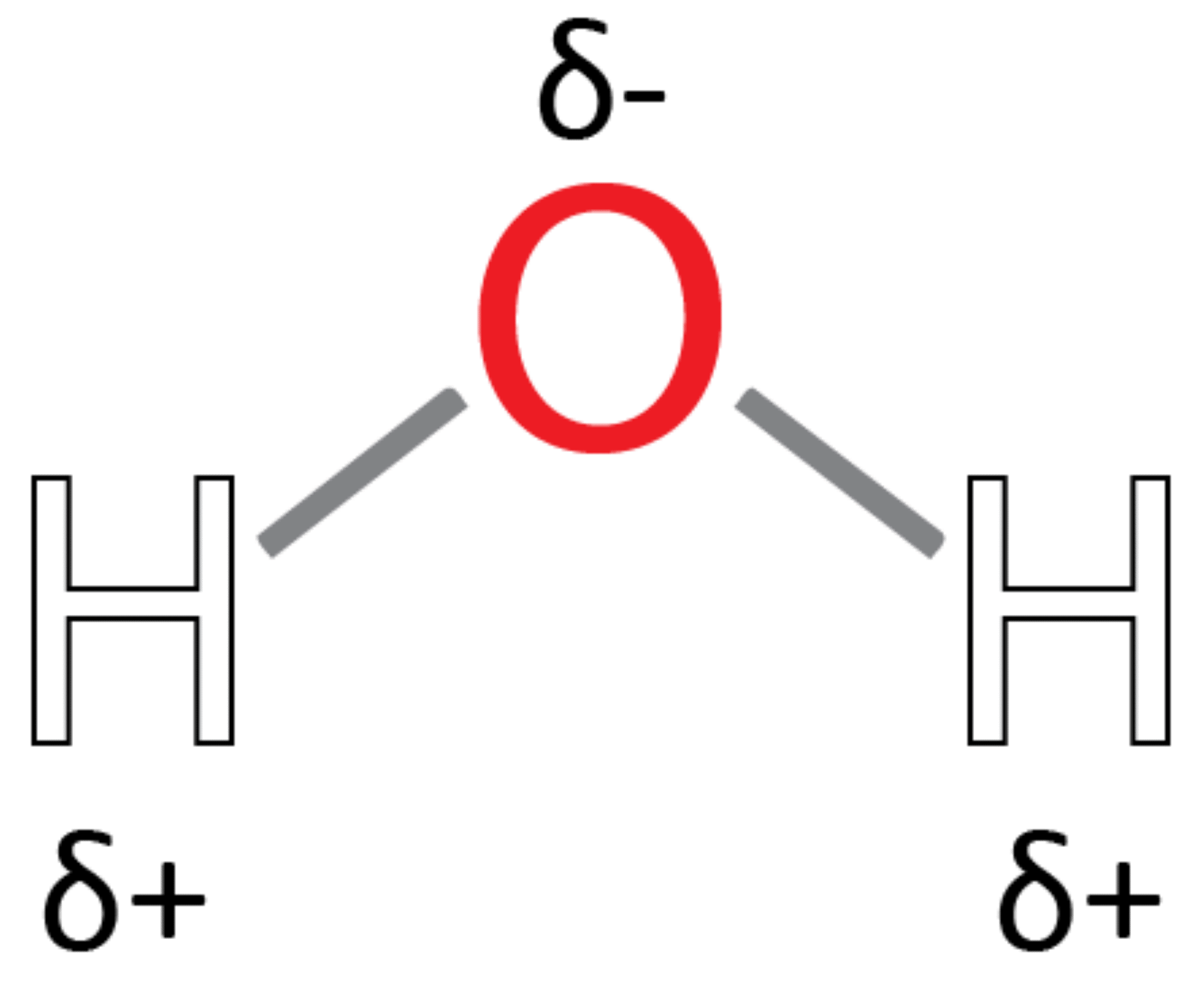
Fysiske og kemiske egenskaber:
I figur 20 ses forskellige fysiske egenskaber for vand. Koncentrationen af vanddamp i atmosfæren afhænger af temperaturen. Jo højere temperatur, jo højere koncentration. Ofte taler man om luftfugtighed, når man taler om vanddamp.

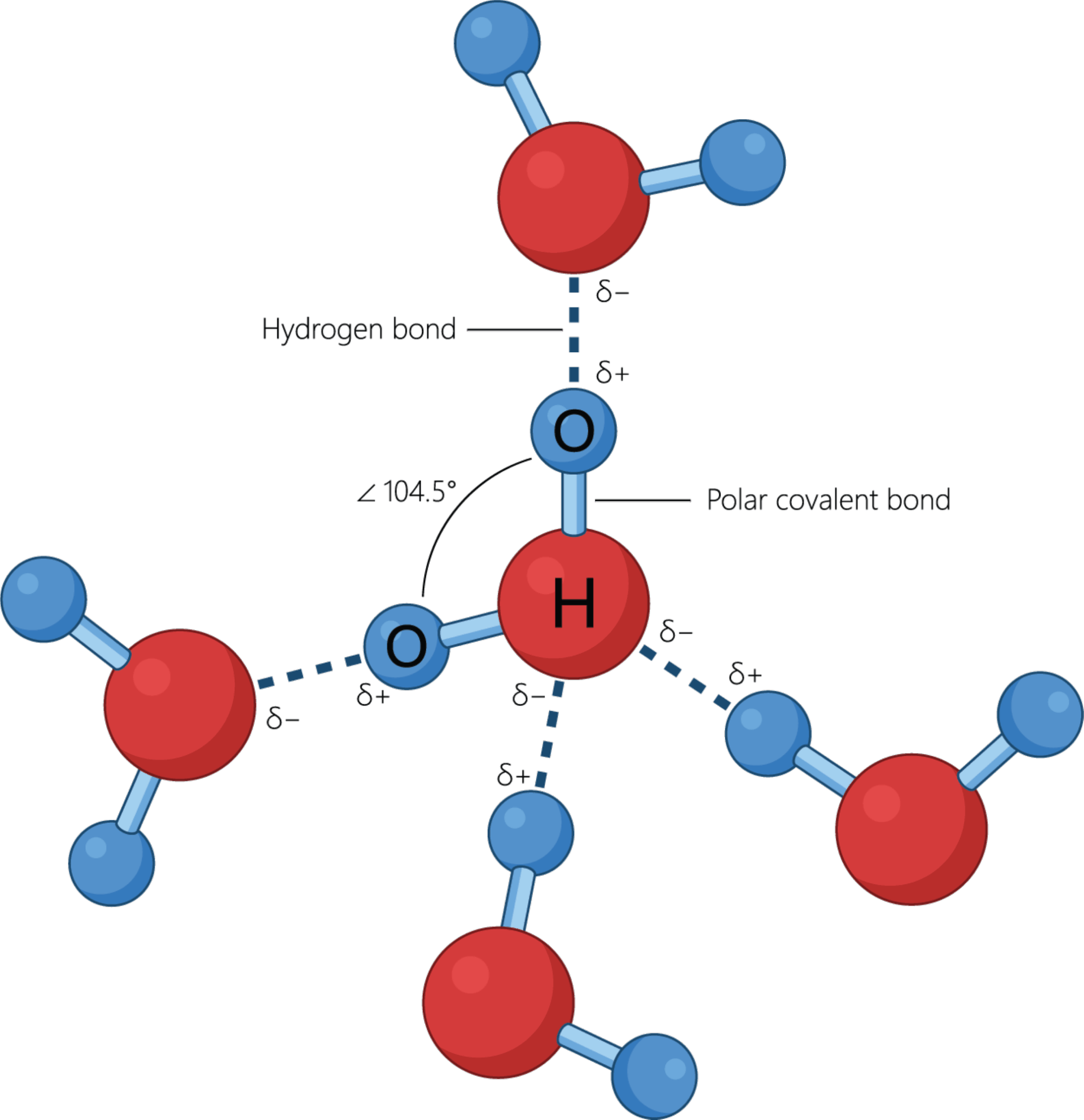
Da molekylet er polært, fungerer det som et godt opløsningsmiddel for andre polære stoffer og ionforbindelser. En anden egenskab ved vandmolekyler er, at danner hydrogenbindinger til hinanden. Hydrogenatomerne i et vandmolekyle er nemlig i underskud på elektroner pga. oxygenatomets høje EN-værdi, og derfor tiltrækkes de af de frie elektronpar på oxygenatomerne i nabomolekylerne. I figur 21 kan du se, hvordan vandmolekyler holdes sammen af hydrogenbindinger.
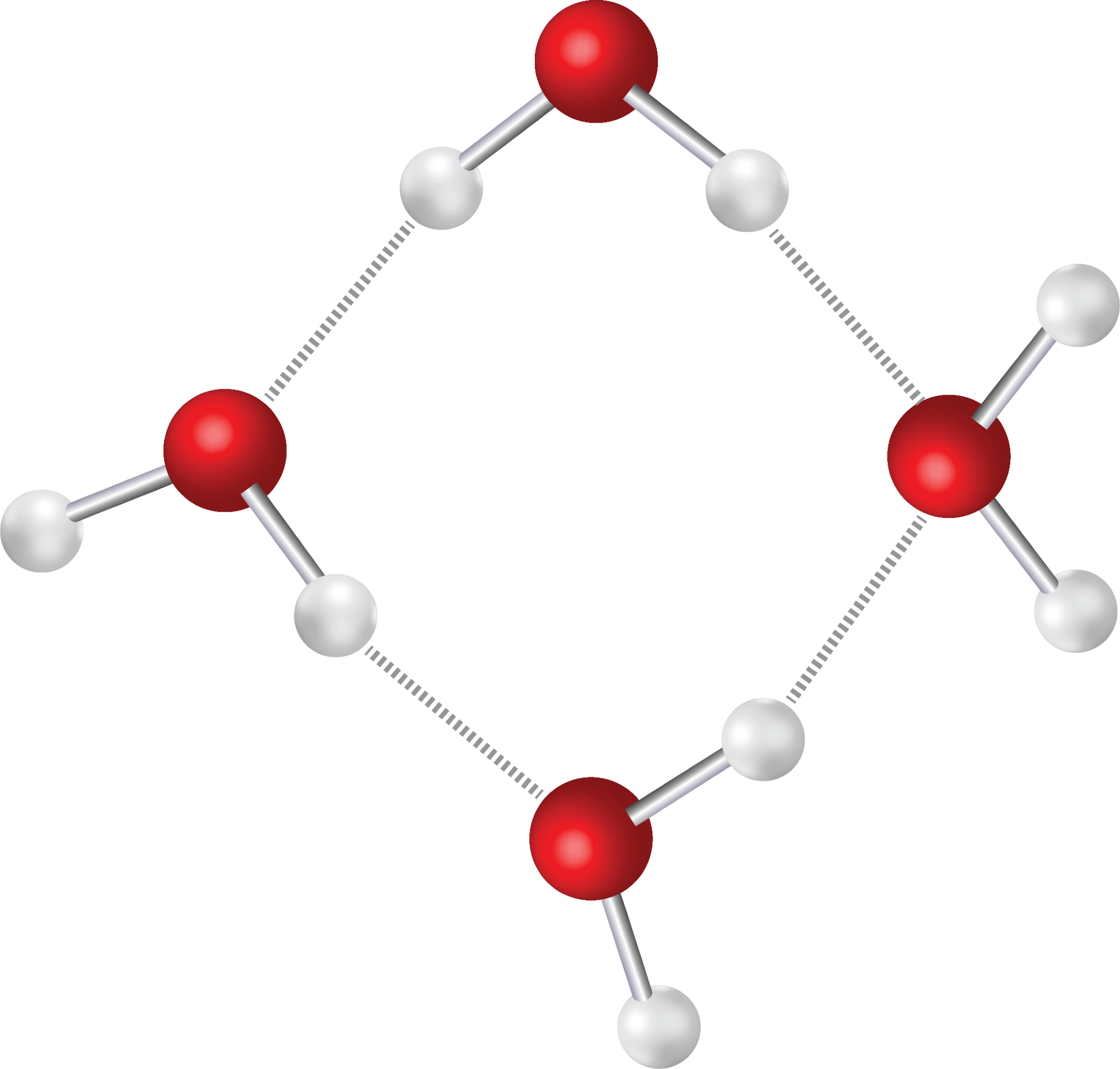
Hydrogenbindinger gør, at selvom vandmolekylet er lille, så er det tiltrukket af nabomolekylet i så høj grad, at både smelte- og kogepunktet for vand er relativt højt sammenlignet med fx dihydrogensulfid (H2S), som er et større men sammenligneligt molekyle. Dihydrogensulfid danner ikke hydrogenbindinger, og derfor er kogepunktet faktisk så lavt som -60,7 °C.
Fun facts:
1. Uden vand – intet liv?
Vand er en betingelse for liv, så vidt vi ved. Det har du nok hørt før, og måske har du også hørt, at når forskere leder efter tegn på liv udenfor jorden – fx på Mars – leder man efter vand. Alle levende organismer, som vi kender, har brug for vand på flydende form, hvilket normalt er mellem 0-100 °C. Vand fungerer som et unikt opløsningsmiddel, hvor de fleste af cellernes kemiske reaktioner kan foregå. Vand transporterer næringsstoffer og affaldsstoffer, stabiliserer temperaturen gennem sin store varmekapacitet og hjælper med at opretholde cellers struktur gennem osmose og hydrogenbindinger. Uden vand ville de biokemiske processer, der opretholder liv, simpelthen ikke kunne finde sted.
2. Is redder livet i søer og hav
Når de fleste stoffer går fra væske til fast form, er deres massefylde som regel større. Fx falder fast jern til bunds i flydende jern. Men når vand fryser til is, flyder det ovenpå vandet. Det sker, fordi vandmolekylerne pakker sig systematisk og har en masse luftkanaler, og dermed bliver isens massefylde lavere end vand. Det kan du se i denne film om vands tilstandsformer. Det er heldigt for livet i søerne og havene, for ellers ville vandet fryse fra bunden, og fisk og andre levende organismer ville dø (se figur 22). Når isen lægger sig ovenpå vandet, isolerer det faktisk, så vandet på bunden ikke fryser.
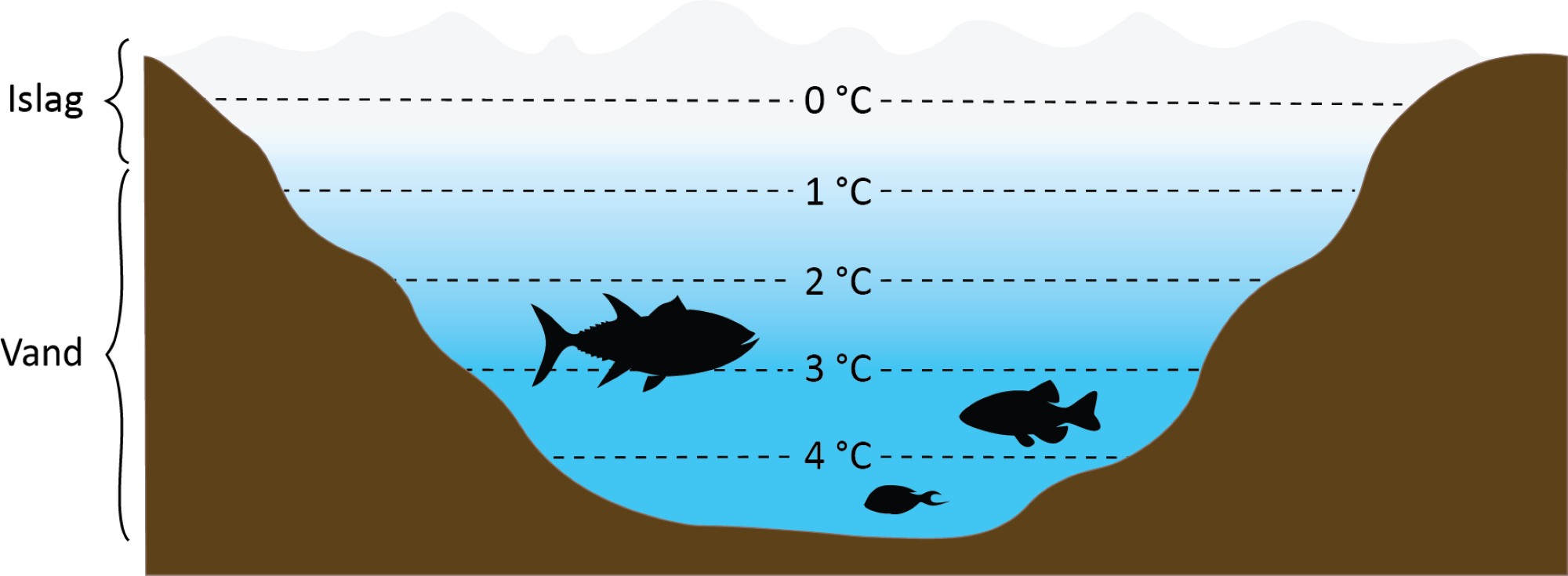
vand er så vigtigt, at man siden 2010 har vedtaget, at adgang til rent vand og sanitet er en menneskerettighed? Denne ret indebærer adgang til tilstrækkeligt, sikkert, acceptabelt, fysisk tilgængeligt og overkommeligt vand til personlig og husholdningsbrug samt sanitet og hygiejne.
Du har fået forskellige oplysninger om vand ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
1. Forklar, hvordan alle atomer i vandmolekylet får opfyldt oktetreglen.
2. Forklar, hvorfor molekylet er vinklet og har en tetraederisk opbygning.
3. Hvilken rolle spiller de frie elektronpar på oxygenatomet for molekylets form?
4. Forklar, hvad en hydrogenbinding er.
Se mere
Når du søger efter figurer på nettet til fx en præsentation i din klasse, skal du huske at være kritisk overfor, hvad den viser og hvor den kommer fra. Diskutér med din sidemakker, hvad problemet er i figur 23.
Se mere
Navn:
Trioxygen er navnet, som viser, hvordan molekylet er bygget op, men det kaldes for ozon.
Bindingstyper:
Elektronparbindinger holder atomerne sammen.
Hvis du skulle bygge ozon med et molekylebyggesæt, ville du hurtigt komme i problemer. Hver røde kugle, som repræsenterer oxygen, har kun to huller. Faktisk ville du kun kunne samle 3 oxygenatomer i en trekant, hvor hvert atom er bundet med en enkeltbinding til de to andre atomer. Men ozonmolekylet ser helt anderledes ud! Det er vinklet, og det centrale oxygenatom er faktisk bundet til de to andre atomer med halvanden elektronparbinding!
I figur 24 er der vist 3 stregformler. De to øverste viser såkaldte resonansformer. Resonansformer er forskellige måder at tegne elektronfordelingen i et molekyle på, når en enkelt struktur ikke kan beskrive elektronernes placering tilstrækkeligt. Molekylets egentlige struktur er en ’blanding’ af disse former, som den nederste stregformel viser. Resonansformerne er også vist i elektronstrukturen.
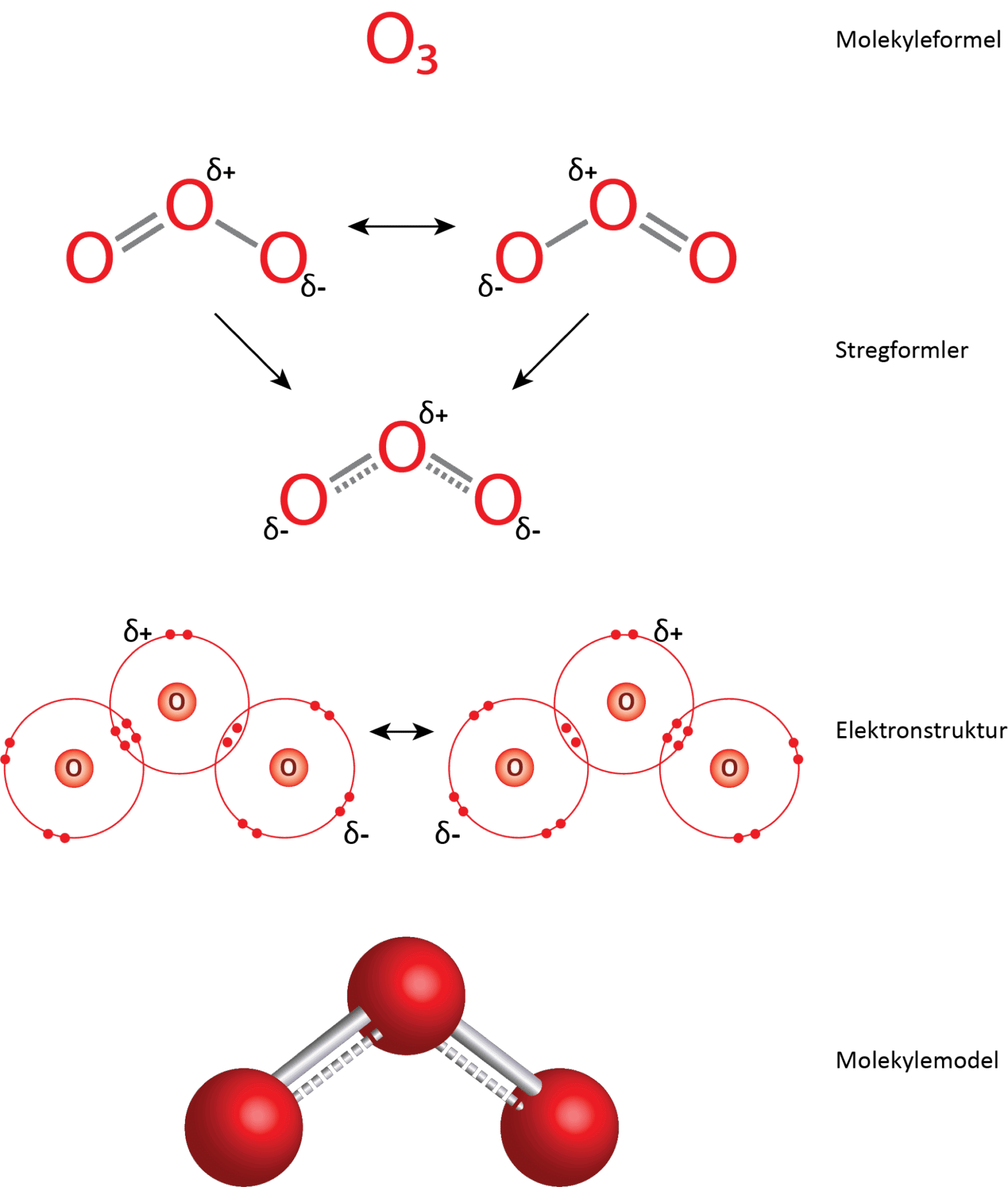
Opbygning:
Ozon er ligesom vand et vinklet molekyle, men bindingsvinklen mellem de to bindinger er 116,8° og derfor større end i vandmolekylet. Hvis du kigger på elektronstrukturen for ozon i figur 24, kan du se, at der kun er et enkelt frit elektronpar på det centrale oxygenatom. De resterende 3 elektronpar indgår i bindingen til de to andre atomer. Dermed vil elektronskyen for det frie elektronpar samt bindingerne til de to andre atomer ligge i et enkelt plan, og molekylet har en plan opbygning omkring det centrale oxygenatom. Hvis det frie og de 3 bindende elektronpar skal placeres længst væk fra hinanden i et plan, burde bindingsvinklen være 120°. Grunden til den er lidt mindre er samme som for vandmolekylet. Elektronskyen for det frie elektronpar presser de bindende elektronpar en smule tættere på hinanden.
Længden af enkeltbindinger er større end for dobbeltbindinger, og det gælder også for bindinger mellem oxygenatomer, som du kan se i figur 5. Forskere har undersøgt bindingslængderne i ozonmolekylet og fundet ud af, at de er et sted midt imellem enkelt- og dobbeltbindinger. De svarer til halvanden binding.
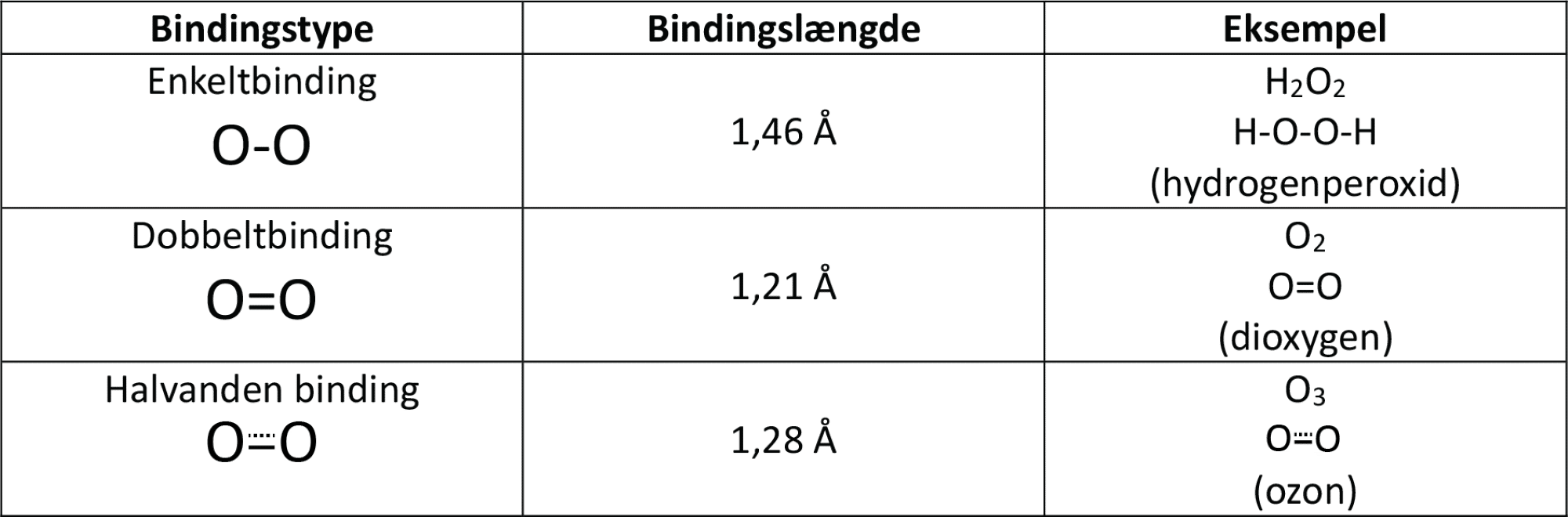
Ozonmolekylet burde være upolært, da atomerne er ens og derfor har samme elektronegativitet. Dermed bliver forskellen i elektronegativitet præcis 0:
EN(O) = 3,5
ΔEN = 0,0
Men molekylet er polært! I opgave 9 længere nede får du en forklaring på det.
Fysiske og kemiske egenskaber:
I figur 26 ses forskellige fysiske egenskaber for ozon. Molekylet er polært og opløseligheden i vand er derfor stor. I stratosfæren mellem 20 og 30 km over jordens overflade topper koncentrationen af ozon i det såkaldte ozonlag, som beskytter os mod en del af solens farlige UV-stråler. Længere nede i troposfæren fra 0-15 km over jordens overflade er ozonkoncentrationen lavere (0,000001 %), men i meget forurenede byer er koncentrationen 7 gange større end dette. Det lyder ikke af meget, men ozon er faktisk sundhedsskadeligt.

Ozon er et meget reaktivt molekyle, fordi strukturen er ustabil. Ozon absorberer UV-strålerne fra solen, og molekylet omdannes til dioxygen og et frit oxygenatom.
O3(g) → O2(g) + O(g)
(2)
Det frie oxygenatom kan reagere med et andet oxygenatom og danne dioxygen, eller det kan gendanne ozon ved at reagere med et dioxygenmolekyle. Herudover er ozon et kraftigt oxidationsmiddel, så det kan reagere med andre stoffer i luften både højt oppe i atmosfæren og tættere på jordoverfladen.
Fun facts:
1. Ozonens dobbelte rolle
Ozon er både godt og skidt for os. Det afhænger af, hvor det befinder sig. Så længe det befinder sig højt oppe i stratosfæren, beskytter molekylet os delvist mod UV-stråling. Men nede ved jordoverfladen kan det dannes pga. forurening, og fordi det er så reaktivt, reagerer det med forskellige stoffer i luften og danner sundhedsskadelige partikler. De kan ende med at give irritation i luftvejene (astma og kronisk bronkitis) og emfysem, som er en kronisk lungesygdom, hvor man har vejrtrækningsproblemer.
2. Ødelæggelse og genopretning af ozonlaget
Måske har du hørt om huller i ozonlaget? Ellers spørg dine forældre, om de har hørt om det. Hvert år dannes der et hul i ozonlaget over Antarktis. Og for 50 år siden fandt man ud af, at udledning af menneskeskabte gasser (CFC-gasser, som du kan læse om længere nede) årtier inden, spillede en stor rolle i at øge størrelsen af hullerne i ozonlaget. På grund af en stor international indsats gennem mange årtier, er der nu godt nyt. Ozonlaget er på vej til at blive genoprettet. Det kan du læse mere om her.
3. Lugten af ozon
Nogle gange kan du lugte, at regn er på vej. Især ved tordenvejr. Det skyldes, at der dannes små mængder ozon. Navnet ozon kommer fra græsk og betyder at lugte. Den dejlige duft, du måske har lagt mærke til efter regnen, skyldes dog, at gas fra de øverste jordlag frigives.
I denne engelske video får du en forklaring på, hvorfor ozon er polært. Når du har set den, skal du sammen med din sidemakker forsøge at forklare på dansk, hvorfor ozon er polært. Du kan med fordel inddrage figur 24.
Se mere
Du har fået forskellige oplysninger om ozon ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
1. Forklar, hvorfor ozonmolekylet ikke kan beskrives med én enkelt strukturformel. Hvad viser resonansformerne?
2. Hvorfor siger man, at bindingerne i ozon svarer til halvanden binding?
Se mere
Navn:
Dinitrogenoxid er navnet, du bruger i kemi, for det beskriver molekylets opbygning. Men i daglig tale kaldes molekylet også for lattergas, da man tidligt fandt ud af, at gassen kunne få folk til at grine.
Bindingstyper:
Elektronparbindinger, også kaldet kovalente bindinger, holder atomerne sammen.
Hvis du skulle bygge dinitrogenoxid med et molekylebyggesæt, ville du få problemer med at få de tre huller i hvert nitrogenatom og de to huller i oxygenatomet fyldt ud. Det skyldes som med ozon, at molekylet findes som resonansformer, som du kan se i figur 27. Molekylets egentlige struktur er en ’blanding’ af disse former.
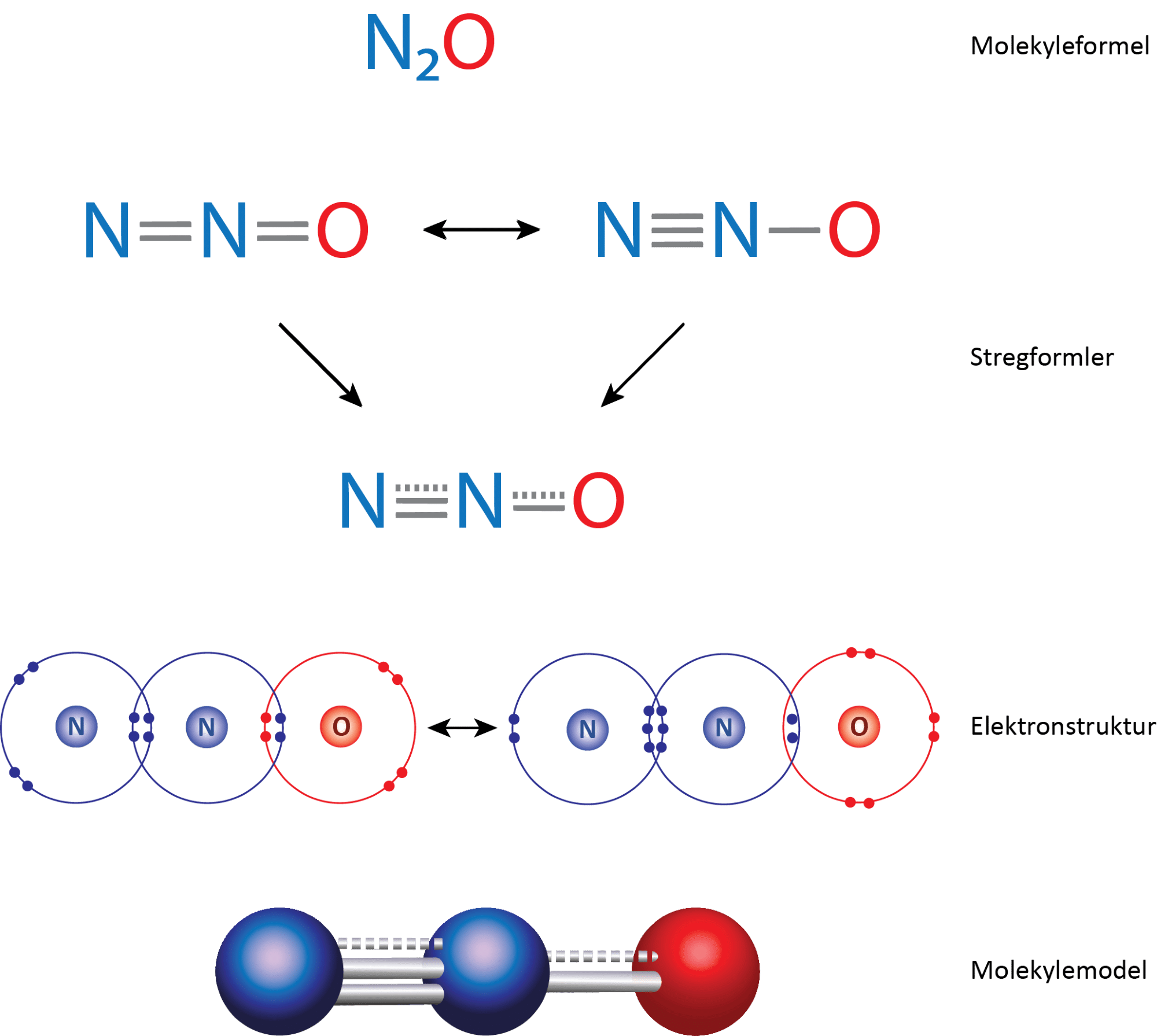
Opbygning:
Dinitrogenoxid er et treatomigt molekyle, hvor alle atomerne er bundet sammen med flere bindinger end enkeltbindinger (henholdsvis 2,5 og 1,5). Derfor er molekylet lineært.
Ligesom du så for ozon, er længden af enkeltbindinger større end for dobbeltbindinger, der er længere end trippelbindinger, og det gælder også for bindinger mellem nitrogenatomer, som du kan se i figur 28. Forskere har undersøgt bindingslængden mellem nitrogenatomerne i dinitrogenoxidmolekylet og fundet ud af, at den er et sted midt imellem dobbelt- og trippelbindinger. Den svarer til 2,5 binding.
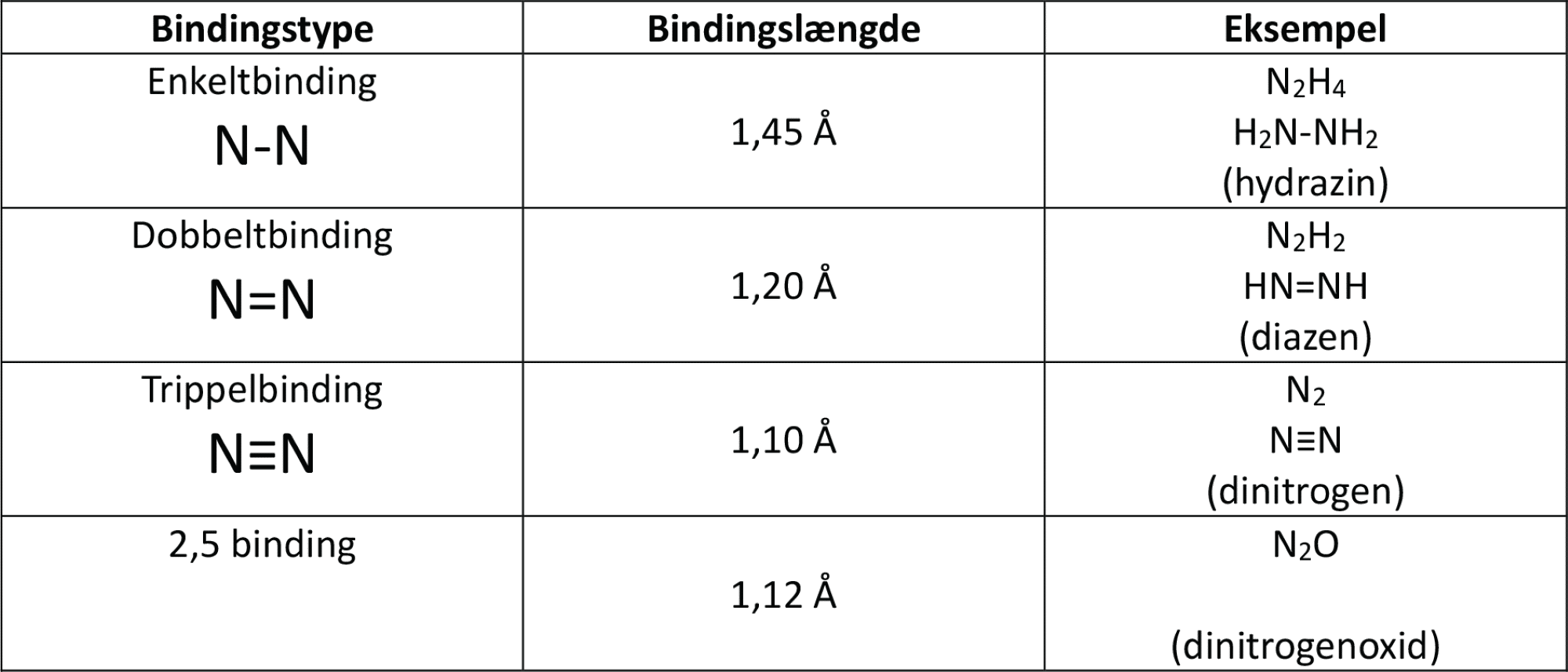
Molekylet er lige på grænsen mellem polært og upolært, da forskellen i elektronegativitet er 0,5 (se figur 4 i temaet ’Den tredje dimension – livets arkitektur’:
EN(O) = 3,5
EN(N) = 3,0
ΔEN = 0,5
Fysiske og kemiske egenskaber:
I figur 29 ses forskellige fysiske egenskaber for dinitrogenoxid. Selvom molekylet er på grænsen mellem polær og et upolær, opløses der relativt meget af gassen i vand ved stuetemperatur. Jo højere temperatur vandet har, jo mindre dinitrogenoxid kan der opløses deri.
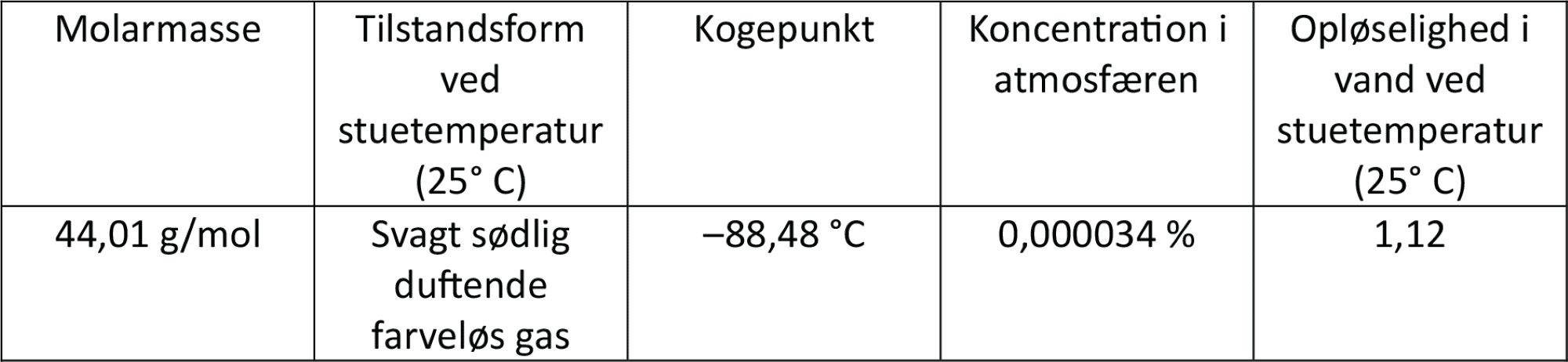
Elektronstrukturen for dinitrogenoxid er meget stabil, og molekylet reagerer praktisk taget ikke i den nedre del af atmosfæren kaldet troposfæren. Længere oppe, i stratosfæren, nedbrydes molekylet af solens UV-stråler, og det sætter gang i en række af reaktioner, der resulterer i nedbrydningen af ozonmolekylerne i ozonlaget.
Fun facts:
Lattergas har haft flere anvendelser gennem tiden, som du kan læse om her.
1. Lattergas finansierede udviklingen af revolveren
I starten efter opdagelsen af lattergas blev den brugt til at få folk til at grine. En god historie er, at opfinderen af Colt-revolveren manglede penge, og han endte derfor med at producere lattergas og tage rundt til velhavende kunder under påskud af at være læge og underholdt dem med lattergas. Herved tjente han nok penge til at kunne udvikle Colt-revolveren, der har en roterende cylinder, som du kan se i figur 30.

Colt producerede sin egen lattergas ved at opvarme ammoniumnitrat til knap 300 °C:
NH4NO3(s) → N2O(g) + H2O(g)
(3)
Colt vidste godt, at hvis han varmede ammoniumnitraten for meget op, ville det udvikle store mængder gasser, der hurtigt ville udvide sig med en eksplosion. Reaktion (4) er den dominerende reaktion ved opvarmning af ammoniumnitrat til højere temperaturer end den, Colt brugte.
NH4NO3(s) → 2 N2(g) + O2(g) + 4 H2O(g)
(4)
2. Bedøvelsesmiddel
I dag anvendes lattergas som almindeligt bedøvelsesmiddel hos både tandlæger og på fødestue. Gassen er relativt hurtigt ude af kroppen igen. Den gives som en blanding af 50% dioxygen og 50% dinitrogenoxid, så der er altså ikke tale om ren lattergas. Lattergassen er et effektivt bedøvelsesmiddel, fordi den er opløselig i fedt, og en del af din krop – især din hjerne – har meget fedt i sig.
3. Lattergas i køkkenet
Når lattergaspatroner i dag bruges i køkkenerne til bl.a. at opskumme fløde med, så er det også, fordi gassen er meget opløselig i fedt. Så den fløde, der kommer ud af sifonen (se figur 31), indeholder meget gas, og når trykket falder udenfor gaspatronen, udvider lattergassen sig meget, og det giver en god opskumningseffekt af fløden.

Den lette adgang til lattergaspatroner har dog skabt store misbrugsproblemer, som du kan læse lidt om i næste afsnit.
Hard facts:
Selvom lattergas har vigtige anvendelser i medicin og industri, bliver det også misbrugt som rusmiddel. Når gassen indåndes, kan den give en kortvarig følelse af eufori og svimmelhed. Men misbruget er meget farligt: indånding af ren lattergas kan føre til iltmangel, og gentagen brug kan skade nervesystemet, fordi gassen nedbryder kroppens B12-vitamin. Derudover kan brugeren miste bevidstheden og komme ud for alvorlige ulykker.

Du kan læse her om en læge, der behandler misbrugere af lattergas. Der kan du også finde et link til DR-serien ’Livsfarlig lattergas’, som gennem tre afsnit undersøger, hvor udbredt misbruget er.
Du har fået forskellige oplysninger om dinitrogenoxid ovenfor. Nu skal du sammen med en makker prøve at se, hvor meget I til sammen kan huske og har forstået om molekylet. I må ikke kigge ovenfor.
1. Forklar, hvorfor molekylet kaldes dinitrogenoxid i kemi.
2. Hvorfor er dinitrogenoxid lineært, selvom der er tre atomer i molekylet?
Se mere
CFC-gasser er en samlet betegnelse for en række af gasser, som indeholder chlor, fluor og carbon. Gasserne er syntetiske og meget stabile og har en række fordelagtige egenskaber. Efter mange års brug, fandt man dog ud af, at de samme fordelagtige egenskaber var skyld i, at ozonlaget blev nedbrudt. En verdensomspændende aftale fik forbudt stofferne, og som du kan læse om under Fun Facts om ozonmolekylet, er ozonlaget godt på vej til at blive gendannet.
I opgave 12 dykker du ned i både strukturen og de fysiske og kemiske egenskaber for CFC-gasser.
På baggrund denne engelske tekst fra Imperial College London skal du forsøge at lave følgende opgaver.
1. Der er vist fire strukturer af forskellige CFC-molekyler. Sammenlign strukturen af disse med strukturen for de andre gasser i atmosfæren længere oppe og giv et bud på, om der er tale om en lineær, plan eller tetraederisk opbygning omkring carbonatomerne.
2. Beregn ΔEN for de enkelte bindinger i alle fire molekyler og kommenter herefter på, om molekylet overordnet er polært eller upolært. Her kan du finde information fra afsnittene om de andre gasser i atmosfæren, som kan hjælpe dig.
3. Den almindelige forbruger havde kontakt med CFC-gasser i mange sammenhænge, før de blev forbudt. Lav en liste over de nævnte anvendelser af CFC-gasser, som står i teksten.
4. Når du sveder, fordamper vandet fra din hud, og du bliver afkølet. Læg mærke til kogepunkterne for gasserne. Kan du gennemskue, hvorfor CFC-gasser med kogepunkt fx omkring 0°C, kan afkøle et køleskab?
5. Når CFC-gasserne når op i stratosfæren, nedbrydes de af UV-strålingen fra solen, og der dannes frie chloratomer, som du kan se i de første to reaktionsskemaer i teksten. Hvis du tænker på, hvor i det periodiske system, chloratomet befinder sig, kan du så forklare, hvorfor det er så reaktivt? Du kan med fordel inddrage ædelgasreglen.
6. Molekylet chlormonoxid har ligesom chloratomet en uparret elektron, og det gør begge meget reaktive. Forklar, hvorfor det er et problem for ozonlaget, at chlor gendannes i den 4. reaktion.
Se mere
Du har nu lært om atmosfærens gasser. Du har mødt de helt almindelige som dinitrogen og dioxygen, og de særlige drivhusgasser som carbondioxid, methan og dinitrogenoxid, der spiller en central rolle i klimaforandringer.
Men atmosfæren rummer mere end gasser. Den indeholder også partikler, som med et fagudtryk hedder aerosoler. De kan stamme både fra naturlige kilder som vulkanudbrud, havsprøjt og skovbrande og fra menneskelig aktivitet som biltrafik og industri. De er meget små faste stoffer eller væskedråber, som svæver i luften. Selv om aerosoler er bittesmå faste stoffer eller væskedråber, kan de have stor betydning for både helbred og klima, bl.a. fordi de fungerer som kim til skydannelse.
3 Partikler i atmosfæren
Aerosoler kan svæve i luften i dage til uger, og de findes overalt – fra byernes udstødningsgasser til støv, der transporteres over kontinenter. Måske har du hørt om fænomenet ’blodregn’, hvor rødligt støv fra Sahara føres helt til Danmark. Når det blandes med regndråber, kan det give en svagt rødlig regn, som du kan se i figur 32. Det giver også helt utroligt flotte solnedgange, fordi støvet bryder lyset. Det er et tydeligt eksempel på, hvordan partikler kan rejse enorme afstande og stadig påvirke vores miljø. Aerosoler er meget mindre end sandkornene fra Sahara og har derfor potentiale til at blive endnu længere i atmosfæren.

Aerosoler varierer meget i størrelse, form og kemisk sammensætning, og derfor også i deres virkning på klimaet. Nogle er naturlige, mens andre stammer fra menneskelig aktivitet. Naturlige kilder til aerosoler omfatter fx havsprøjt, der danner små saltkrystaller, vulkanudbrud, som sender svovlholdige partikler højt op i atmosfæren, og skovbrande, der frigiver sod og organiske stoffer. Andre vigtige naturlige kilder er de biologiske systemer. Planter og mikroorganismer udsender organiske molekyler til atmosfæren, de såkaldte biogene aerosoler, som kan reagere kemisk og danne nye partikler. Menneskeskabte kilder inkluderer biltrafik, industri og afbrænding af fossile brændstoffer. De mindste partikler, især de såkaldte PM2.5 med en diameter på 2,5 µm eller mindre, er mest sundhedsskadelige, fordi de kan trænge dybt ned i lungerne og øge risikoen for luftvejssygdomme og hjerte-kar-sygdomme. Lungen er bygget til at filtrere de større partikler væk, hvorfor disse ikke er så farlige. I figur 33 kan du få en fornemmelse for størrelsen af aerosoler.
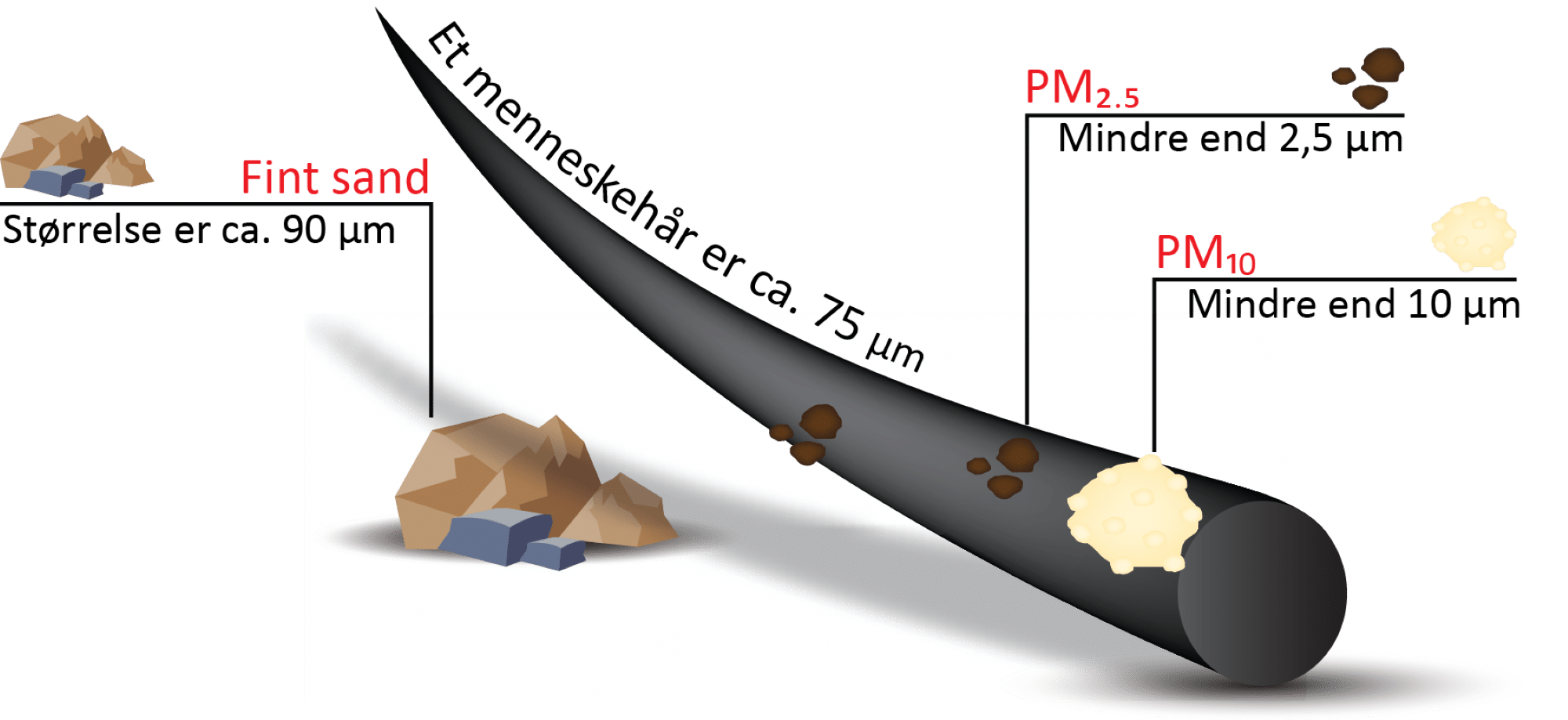
Aerosoler påvirker klimaet på komplekse måder. Nogle partikler som sod absorberer sollys og varmer atmosfæren op, mens andre som sulfataerosoler reflekterer sollys og virker afkølende. Derudover spiller aerosoler en central rolle i skydannelse, fordi de fungerer som små overflader, som vanddamp kan kondensere på. Antallet, størrelsen og den kemiske sammensætning af partikler afgør, hvor let skyer dannes, hvor reflekterende de bliver, og hvor længe de lever. Derfor har selv meget små mængder aerosoler en stor betydning for vores klima.
For at forstå skydannelse og aerosolernes rolle i klimaet endnu bedre forsker danske kemikere i de helt grundlæggende processer, der sker på molekylært niveau. Det arbejde foregår blandt andet i Center for Chemistry of Clouds, som du kan læse om i faktaboksen herunder.
Forskning i skydannelse på molekylært niveau
’På trods af skyernes rolle for menneskers dagligdag gennem tusindvis af år, ved vi forbavsende lidt om, hvordan de dannes’, siger centerleder for Center for Chemistry of Clouds, (C3), Merete Bilde.

C3 er et grundforskningscenter på Institut for Kemi på Aarhus Universitet med fokus på skydannelse og kemien bag. Centeret er finansieret af Danmarks Grundforskningsfond. Om forskningen, siger Merete Bilde:
’Vi forsker i de helt grundlæggende molekylære byggesten til skydannelse.
Skyer dækker to tredjedele af himlen, spiller en vigtig rolle i vandkredsløbet på jorden
og påvirker i høj grad vores klima.
Derfor er det vigtigt at forstå skydannelse og skyers påvirkning af klimaet,
især for at kunne forudsige fremtidens klima.’
For at der kan dannes skyer, skal der være en overmætning af vand i atmosfæren og en overflade, som vandet kan kondensere på. Aerosoler er bittesmå partikler, der er til stede over alt, og netop er den overflade, vandet har brug for. Forskerne i C3 arbejder fra før aerosolerne er dannet til de kan blive skydannelseskerner. Merete fortæller:
‘I vores laboratorium kan vi simulere dannelsen af aerosoler i luften i en skov,
i en forurenet by eller over havet og måle mange af de egenskaber,
der er vigtige for, om de kan virke som kim for dannelsen af skyer.
Men hvis partiklerne er mindre end 2 nm, har vi brug for kvantekemi
for at undersøge, hvordan de dannes fra gasfasemolekyler,
og hvordan de vokser, indtil de når en størrelse, vi kan måle.’
I figur 34 kan du se en størrelsesskala for partikler, der kan vokse sig store og blive til skydannelseskerner. De allermindste byggesten til aerosoler er molekylære klynger, som består af nogle få molekyler, der holdes sammen af tiltrækningskræfter. De er større end enkeltmolekyler, men stadig for små til at blive betragtet som egentlige partikler.
Når partiklerne når over 2 nm, kan deres egenskaber undersøges i laboratoriet. Her vokser de enten ved kondensation af organiske oxidationsprodukter eller ved optag af vand, afhængigt af deres overflade og kemiske sammensætning.
Partikler omkring 50 nm kan begynde at fungere som skydannelseskerner, men det kræver, at de også har de rette kemiske egenskaber. Det er derfor ikke størrelsen alene, der afgør, om en partikel kan aktiveres som en skydannelseskerne.
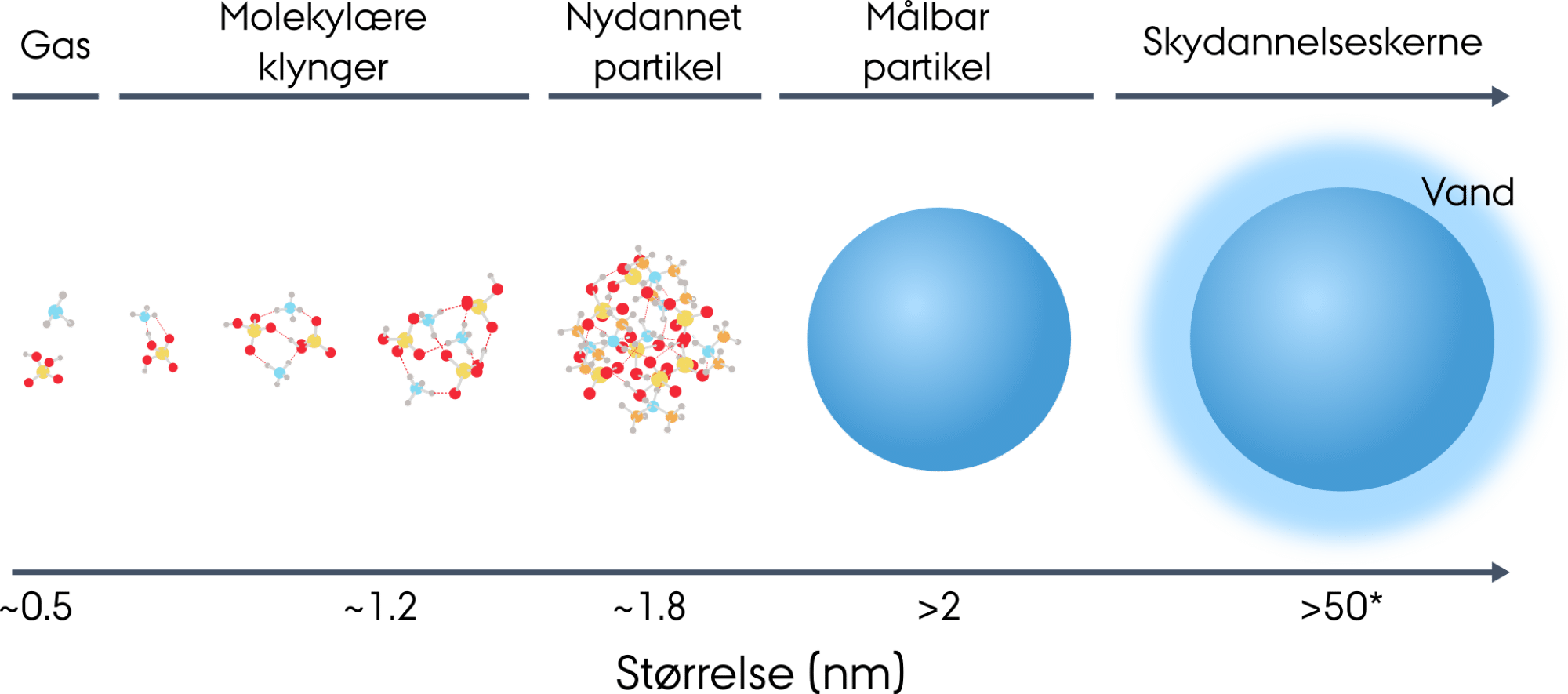
Derudover undersøger forskerne aerosolernes overflade, og hvordan molekyler interagerer med overfladen og måske optages i aerosolpartiklerne. Overfladen betyder meget for om partiklerne kan optage vand og vokse sig store nok til at være en skydannelseskerne.
C3 består af seks forskere med hver deres ekspertiseområde:
1. Professor Merete Bilde er atmosfærisk fysisk kemiker. Hun forsker i aerosolers dannelse og egenskaber som fx deres viskositet, flygtighed og hvor gode de er til at danne skyer.
2. Professor Ove Christiansen er kvantekemiker. Han bidrager med kvantekemisk metodeudvikling og brug af machine learning til at løse komplekse problemstillinger.
3. Lektor Marianne Glasius er analytisk miljøkemiker. Hun udvikler analysemetoder til at måle den kemiske sammensætning af aerosoler for at studere deres dannelse og kilder.
4. Lektor Tobias Weidner er laserkemiker. Han bidrager med at måle hvordan stoffer orienterer sig ved aerosolers overflade, hvilket kan have stor betydning for deres egenskaber i atmosfæren.
5. Lektor Jonas Elm er kvantekemiker. Han forsker i, hvordan man går fra gasfasemolekyler til molekylære klynger og helt nydannede partikler. Han arbejder i størrelsesområdet af partikler, før man kan måle aerosolerne.
6. Adjunkt Fabian Mahrt er atmosfærisk fysisk kemiker. Han forsker i de kemiske og fysiske egenskaber af aerosoler, blandt andet hvordan aerosolpartikler med komponenter på forskellige tilstandsformer påvirker skydannelse.
Som du kan se, bidrager kemikere inden for vidt forskellige områder helt fra analytisk kemi og atmosfærisk fysisk kemi til kvantekemi og laserkemi til en samlet forståelse af, hvordan aerosoler dannes, vokser og påvirker skydannelse og klima.
Om C3s overordnede mål med forskningen siger Merete Bilde:
’Vi håber på at kunne bidrage med vigtig viden om aerosolers
dannelse, vækst, vandoptag og tilstandsformer.
Det er alt sammen viden, der kan forbedre klimamodeller
og dermed vores muligheder for at forudsige fremtidens klima’.
Se mere
Forskningen i C3 giver vigtig indsigt i de allerførste byggesten til aerosoler og skydannelse fra molekylære klynger til partikler, der vokser sig store nok til at blive skydannelseskerner. Men selvom forskerne kan undersøge de helt små molekylære processer, kræver det også, at man kan genskabe atmosfæren i større skala for at forstå, hvordan skyer faktisk dannes. Derfor arbejder atmosfærekemikere også med simulationskamre som AURA, hvor temperatur, fugtighed og lys kan styres præcist for at efterligne forholdene i atmosfæren.
Inden du læser videre om AURA, skal du prøve noget af det mest grundlæggende inden for skydannelse. Du skal lave din egen sky i en flaske! I ’Forsøg 1: Flaskeskyen’ får du mulighed for at se, hvordan vanddamp, tryk og en smule aerosoler tilsammen kan få små dråber til at kondensere præcis som det sker i atmosfæren. Forsøget giver dig en hands-on forståelse for nogle af de samme processer, som forskerne i C3 og AURA arbejder med på et langt mere avanceret niveau.

Lav din egen sky! Når der er en overmætning af vand og en overflade, vandet kan kondensere på, kan du lave en sky.
Øvelsesvejledningen er på vej.
I forskningsboksen ’AURA – Simulering af atmosfærekemi’ kan du blive klogere på, hvordan forskerne undersøger atmosfæren i laboratoriet. Her kan du møde lektor Marianne Glasius, der undersøger aerosolpartikler med teknikken massespektrometri (MS), og de to studerende, Nan Normann Jakobsen og Martine Rasmussen, der til dagligt arbejder med AURA i deres forskning.
Hvordan kan du undersøge de små aerosolpartikler?
For at kunne undersøge, hvordan aerosoler dannes og udvikler sig i atmosfæren, har forskerne brug for et sted, hvor de kan genskabe atmosfæriske forhold på en kontrolleret måde. Det gør de i AURA (Aarhus University Research on Aerosol), som er et 6 m³ stort atmosfærisk simulationskammer på Aarhus Universitet (se figur 35). I AURA kan forskerne styre centrale parametre som temperatur, luftfugtighed og mængden af UV-lys, så reaktionerne kan foregå under forhold, der minder om den virkelige atmosfære.

AURA bruges især til at studere sekundære aerosoler, som er de partikler, der ikke udledes direkte, men dannes gennem kemiske reaktioner i luften. Et af de molekyler, forskerne arbejder meget med, er α-pinen, som bl.a. er med til at give nåletræer deres karakteristiske duft (se figur 36). Når α-pinen kommer ud i atmosfæren fx fra skovene og møder ozon eller andre reaktive stoffer, dannes der nye stoffer med lavere flygtighed. Det er stoffer, som ikke så let kommer på gasform, men i stedet foretrækker at være på fast eller flydende form. Netop af den grund samler de nye stoffer sig lettere sammen og danner små partikler og bidrager på den måde til aerosoler.
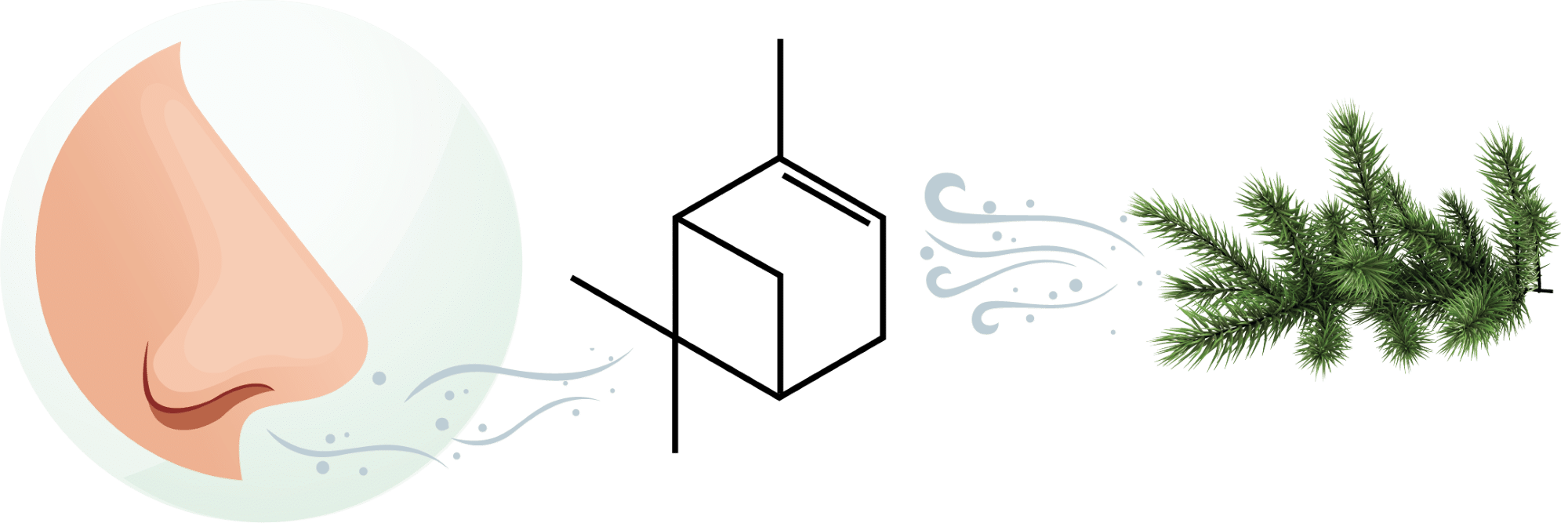
Men partiklerne skal ikke blot dannes. De skal også vokse, før de kan spille en rolle i skydannelse. Derfor undersøger forskerne i AURA, hvilke betingelser der får partiklerne til at optage vand og blive til skydråber. Det afhænger både af deres størrelse og deres kemiske sammensætning. Fx består partikler fra havsprøjt næsten udelukkende af salt, som let optager vand, mens partikler dannet i atmosfæren kan indeholde mange hundrede forskellige stoffer, og derfor kan deres vandoptagelse være mere kompleks. I AURA kan forskerne udsætte partiklerne for høj luftfugtighed og måle, hvor meget vand de optager, og hvordan de ændrer sig.
I figur 37 kan du se de to ph.d.-studerende, Martine og Nan, som er i gang med at samle data fra AURA og starte analysen af dannede partikler. Martine forklarer her, hvorfor lige præcis forskning i atmosfærekemi har fanget hendes interesse:
’Atmosfærekemi er superrelevant! Især lige nu,
hvor vi mærker effekten af global opvarmning i vores nærmiljø
med store oversvømmelser og ekstrem varme i Sydeuropa.
Jeg synes, det er vigtigt, at vi forstår, hvad der sker udenfor,
hvordan vi selv har indflydelse på klimaet,
og hvordan vi kan hjælpe med at forstå fremtidens klima.’

Når partikler er i luften, skal de vokse for at kunne blive en skydannelseskerne. Lektor Marianne Glasius fra C3 siger:
’Før vi får dannet en sky, skal partiklerne optage vand og blive til skydråber.
For at en partikel optager vand, skal den have nogle bestemte egenskaber.
Her er især dens kemiske sammensætning og størrelse vigtig.
Derfor udvikler vi analysemetoder til at undersøge
de tusindvis af kemiske forbindelser, partikler består af.’

Partikler i skumsprøjt fra havet består næsten udelukkende af salt, og da salt er letopløseligt i vand, er en saltpartikel netop god til at optage vand. En partikel, der derimod er dannet i atmosfæren, består af mange forskellige molekyler, som man ikke kender den fulde sammensætning af. Derfor er det svært at forudsige, hvordan sådan en partikel vil optage vand.
Når forskerne har dannet partiklerne i AURA, kan de måle, hvordan partiklerne optager vand, fx ved at udsætte dem for høj luftfugtighed og se, om de optager vand. Samtidig er det vigtigt at undersøge, hvad partiklerne faktisk består af. Til dette bruger Marianne teknikken massespektrometri (MS).
MS er en analytisk kemisk teknik, der gør det muligt at bestemme massen af molekyler i en prøve og dermed få information om den kemiske sammensætning. I C3 anvendes MS både til at analysere prøver fra AURA-forsøgene og til at undersøge molekyler i luft fra omgivelserne.
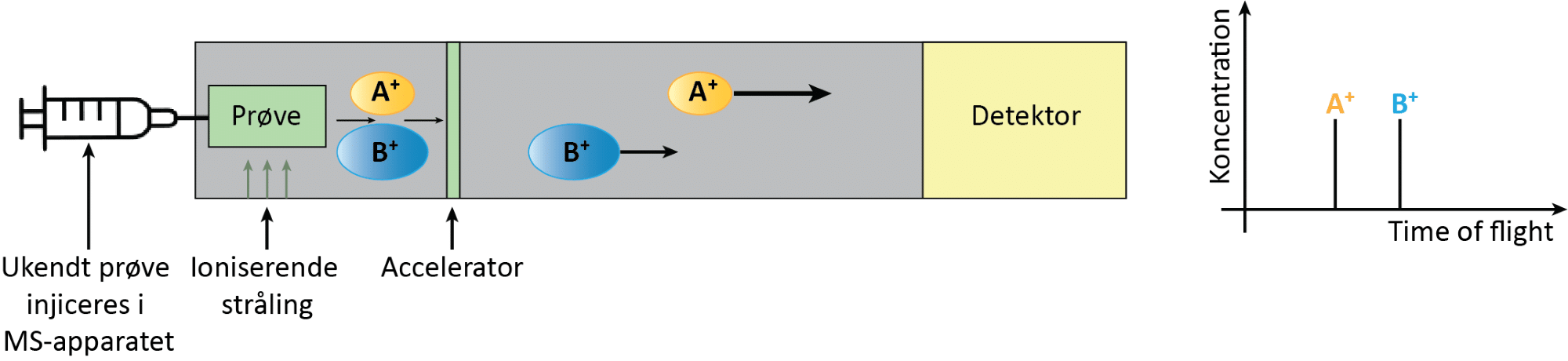
Når forskerne tager en prøve fx fra AURA, føres den ind i et massespektrometer (se figur 38). Her ioniseres molekylerne, så de mister en elektron og bliver elektrisk ladede. De ladede partikler accelereres derefter i et elektrisk felt. Hvor hurtigt de bevæger sig gennem apparatet, afhænger af deres masse: lette ioner får højere fart end tunge ioner. Det kan sammenlignes med at kaste to bolde med samme kraft, hvor den letteste bold får den højeste hastighed.
I et såkaldt time-of-flight-massespektrometer måles den tid, det tager for ionerne at bevæge sig fra acceleratoren til detektoren. Ud fra denne tid kan apparatet beregne ionernes masse og fremstille et massespektrum. Det er en graf, hvor hver top svarer til et bestemt molekyle. Der findes mange forskellige typer massespektrometre, som kan være mere avancerede og bygge på andre principper end det, der er vist her. Fælles for dem er dog, at en prøve analyseres i apparatet, og resultatet er et massespektrum, som kan fortolkes til at afgøre, hvilke stoffer prøven indeholder og i hvilke mængder.
Ved at kombinere MS med de kontrollerede eksperimenter i AURA kan forskerne koble aerosolernes kemiske sammensætning til deres evne til at vokse, optage vand og komme med kvalificerede forudsigelser af, hvilke kemiske reaktioner der kan finde sted i eller på aerosolerne afhængigt af om de er væskedråber eller faste stoffer. Forudsigelsen af de kemiske reaktioner baseres på kvantekemiske beregninger. Du kan senere møde en forsker, lektor Jonas Elm, der arbejder netop med denne del.
Denne kombination af kontrolleret dannelse af aerosoler, detaljerede målinger af deres sammensætning og realistiske atmosfæriske forhold gør AURA til et vigtigt værktøj i forskningen. Viden om, hvordan partikler dannes, vokser og optager vand, er afgørende for at forbedre klimamodeller, fordi skyer påvirker Jordens energibalance og dermed klimaet.
Se mere
Forskningen i aerosoler og skydannelse viser, hvor kompleks atmosfærens kemi er, og hvordan både partikler og gasser påvirker klimaet. Men for at forstå deres samlede betydning er det ikke nok at vide, hvad der reagerer i atmosfæren. Det er også afgørende at vide, hvor hurtigt reaktionerne sker. Nogle stoffer dannes og nedbrydes på få sekunder eller minutter, mens andre, som drivhusgasser, kan opholde sig i atmosfæren i årtier. Hvor længe et stof bliver i atmosfæren, har stor betydning for, hvor stor effekt det har på klimaet.
Derfor er det vigtigt både at forstå atmosfærens energibalance, varmestråling og kulstofkredsløb og at få indsigt i de kemiske reaktioner, der styrer, hvor hurtigt stoffer dannes og nedbrydes i luften.
Men før du dykker ned i reaktionshastighed, kan du vælge at læse de næste afsnit, hvor du bl.a. får svar på: Hvor kommer CO₂ fra? Hvordan fungerer drivhuseffekten? Hvad går kulstofkredsløbet ud på? Og du får mulighed for at afprøve et forsøg, hvor du brænder lightergas af i en hjemmelavet gaskanon.
Når du har styr på disse grundlæggende begreber, er du klar til næste store spørgsmål: Er alle kemiske reaktioner lige hurtige?
4 Atmosfærens betydning for klimaet
Carbondioxiden i atmosfæren er blot en af flere gasser i atmosfæren, og det er en af dem, der er meget lidt af.
1. Hvis du sammenligner koncentrationen af carbondioxid i figur 1 og 11, er de to tal forskellige. Prøv at finde information i figurerne, figurteksterne og teksten omkring figurerne for at finde en forklaring på dette.
2. Brug dette link til at undersøge variationen af CO₂-koncentrationen over tid. Hvad kan du sige helt generelt?
3. Er CO₂-koncentrationen i figur 1 angivet korrekt, hvis du kigger på linket? Hvad kan du aflæse den til?
4. Prøv at give et bud på, hvad forklaringen kan være.
Se mere
Der er desværre ingen tvivl om, at CO₂-koncentrationen i atmosfæren stiger, og at det skyldes os mennesker. Men før du kan læse om, hvorfor det resulterer i drivhuseffekten og øger den globale opvarmning, skal du vide, hvor carbondioxiden i atmosfæren kommer fra. Og den kommer både af naturlige årsager og som resultat af menneskelig aktivitet.
Du skal starte med at se en kort film. Den forklarer, hvorfor carbondioxid er en ressource, som danner grundlaget for alt liv, og som vi derfor ikke kan undvære. Se filmen her.
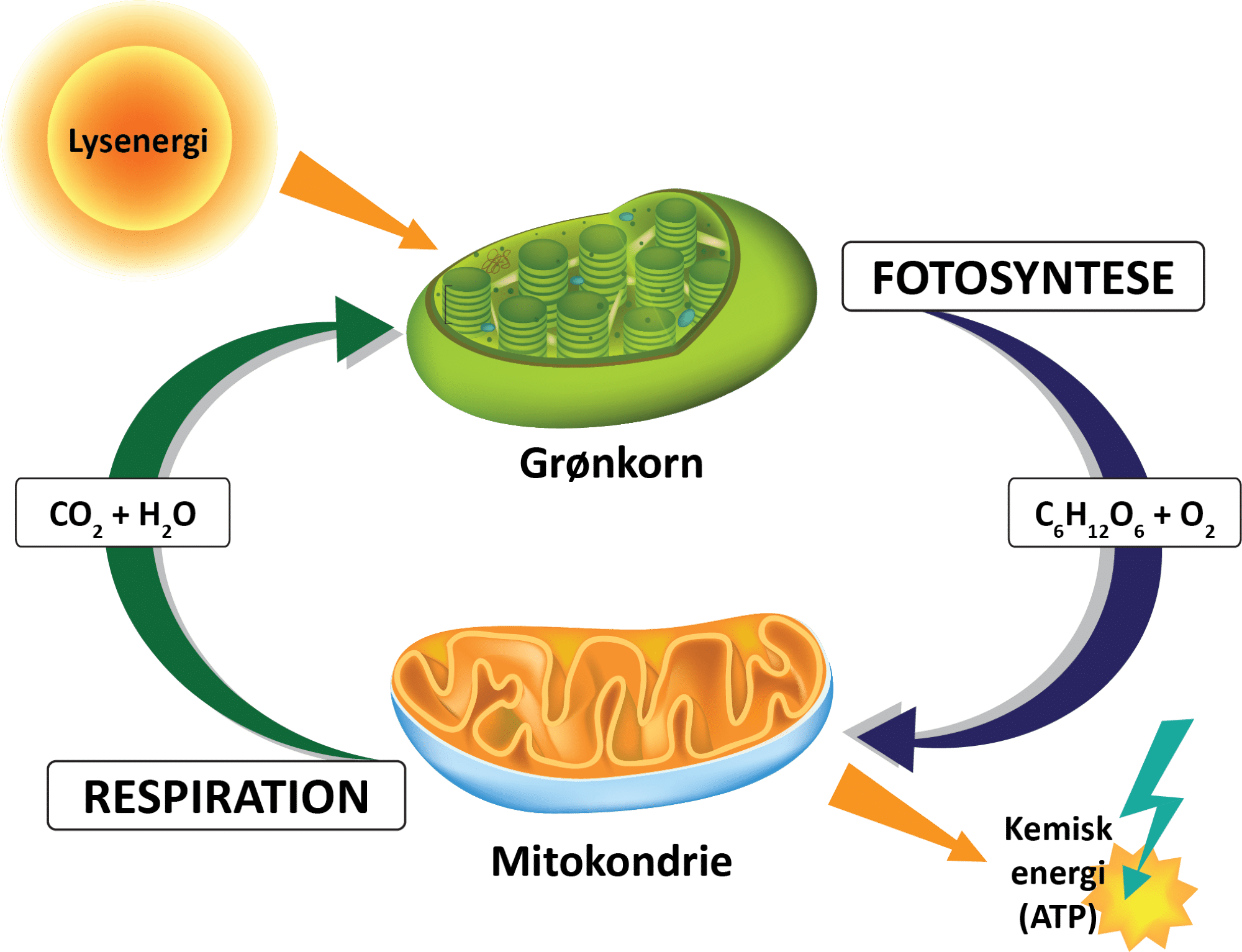
I fotosyntesen, som sker i planternes grønkorn (se figur 39), sker følgende reaktion:
6 CO2(g) + 6 H2O(l) → C6H12O6(aq) + 6 O2(aq)
(5)
Her lagres energi fra solens stråler i organiske forbindelser, der alle stammer fra carbondioxid i atmosfæren. Når de organiske forbindelser nedbrydes igen i cellernes mitokondrier (se figur 39), sker respirationsreaktionen:
C6H12O6(aq) + 6 O2(aq) → 6 CO2(aq) + 6 H2O(l)
(6)
Kig grundigt på reaktion (5) og (6). Kan du gennemskue sammenhængen mellem de to reaktioner og argumentere for, at der er tale om cirkulær kemi? Du kan inddrage figur 39 i din argumentation.
Se mere
I faktaboksen, ’Redox i din hverdag’, kan du læse mere om fotosyntesen og respirationen, som er eksempler på redoxreaktioner.
Systemet bestående af fotosyntesen og respirationen i figur 39 er altså en naturlig cyklus, hvor carbondioxid omdannes til organiske stoffer og frigives igen til luften, når de organiske stoffer forbrændes som mad i vores maver eller når de nedbrydes af fx bakterier og svampe. Du kan se en kort, opsummerende film om denne del af den naturlige udledning af carbondioxid. Systemet er en del af kulstofkredsløbet, som du kan læse mere om senere.
Der er andre naturlige processer, hvor carbondioxid frigives til atmosfæren. Vulkanudbrud er et eksempel herpå, der udleder enorme mængder af carbondioxid og andre gasser som fx svovldioxid. Også naturbrande udleder carbondioxid lige så vel som vådområder, hvor en langsom forrådnelse af gamle træer og andre organiske materialer sker. Her udledes desuden også større mængder af drivhusgassen, methan. I havet er der også bundet en del carbondioxid, men opløseligheden af gassen i vand falder, jo varmere der bliver.
Og så nærmer vi os den menneskelige indflydelse på koncentrationen af carbondioxid i atmosfæren. For med global opvarmning pga. drivhuseffekten (se faktaboksen, ’Drivhuseffekten resulterer i global opvarmning’ nedenfor) stiger temperaturen i havet, og der frigives carbondioxid. Opvarmningen resulterer også i, at store områder, hvor der naturligt har været permafrost (dvs. jorden frossen hele året), tør, og så sker der en enorm omsætning af dødt, organisk materiale. Dette forårsager også en stor udledning af carbondioxid og methan. Så menneskelig aktivitet påvirker klodens temperatur og speeder de naturlige processer yderligere op.
I fotosyntesen omdannes solens energi til kemisk energi, som lagres i molekylet ATP (adenosintriphosphat) og i andre organiske forbindelser. I denne proces bruges atmosfærens carbondioxid (se figur 32), men så snart det organiske materiale forbrændes, frigives carbondioxiden igen sammen med energien.
Nu skal du selv på arbejde! Du skal i opgave 15 undersøge forskellige eksempler på menneskeskabt CO₂-udledning.
Du skal vælge mindst to af nedenstående eksempler på menneskeskabt udledning af carbondioxid. Du skal søge baggrundsinformation på nettet om eksemplerne og finde mindst 3 eksempler på kemiske reaktioner, der viser, at der udledes CO₂.
a. Forbrænding af fossile brændstoffer
b. Industriproduktion som fx cementfremstilling
c. Skovrydning
d. Landbrug som fx dræning af vådområder eller fremstilling/brug af kunstgødning
e. Affaldsforbrænding
Skriv til sidst en halv side om menneskeskabt udledning af carbondioxid, som kunne indsættes efter denne opgave og udgøre en del af dette undervisningsmateriale.
Se mere
Umiddelbart kunne det lyde som om, der ikke sker en stigning i CO₂-koncentrationen, da den CO₂, der bruges i fotosyntesen, frigives igen i alle de mange processer og eksempler ovenfor. Men så simpelt er det ikke, for der er en faktor mere, som du skal tage i betragtning, og det er tid! Hvor lang tid tager det fx at danne fossile brændstoffer i forhold til hvor hurtigt, det kan brændes af? Først skal du afprøve, hvor hurtigt, du kan afbrænde lightergas, som er et eksempel på et organisk materiale, der stammer fra fossile brændstoffer. Det gør du i ’Forsøg 2: Gaskanonen’. Bagefter kan du læse mere om bl.a. dannelsen af fossile brændstoffer i næste afsnit om kulstofkredsløbet.
Du skal bygge en gaskanon. Se hvor hurtigt, man kan afbrænde fossile brændstoffer og se, at der kommer energi ud af det.
Kulstofkredsløbet er et kredsløb, der beskriver, hvordan carbon cirkulerer rundt gennem forskellige kulstofforbindelser på vores planet. Det kan blive meget komplekst at forstå alle dele af det, så i stedet for møder du en forenklet udgave, da du kun skal have et overblik over det.
Hvis du ikke har set den korte film om den naturlige udledning af carbondioxid, er det en god ide at se den, før du dykker ned i kulstofkredsløbet. Du kan se filmen her.
For at forskere kan arbejde på at finde metoder til at fjerne carbondioxid fra atmosfæren, er de nødt til at forstå kulstofkredsløbet, som du kan se en oversigt over i figur 39. Øverst i figuren er carbondioxidmolekyler i atmosfæren vist. Disse fanges og bindes i organiske forbindelser gennem planternes fotosyntese. Gennem planters og dyrs respiration af de organiske stoffer frigives carbondioxiden igen (se figur 39 og 40):
Organisk stof + O2(g) → CO2(g) + H2O(l) + energi
(7)
Energien fra respirationen kan enten være en omdannelse af kemisk energi i det organiske stof til ren varmeenergi eller til en blanding af kemisk energi i andre kemiske forbindelser og varmeenergi.
Carbondioxid er opløseligt i vand, så der vil altid være opløst carbondioxid i havet og i søer. Her reagerer det med vand og danner forbindelsen hydrogencarbonat (HCO3–), som vandplanter (alger og planteplankton) optager og bruger i deres fotosyntese. Når vandplanterne respirerer, udskiller de også CO₂. Når planteplankton spises af muslinger, der filtrerer vandet, og disse spises af fx krabber, vokser dyrene i størrelse og indeholder dermed mere kulstof. Når dyr og planter dør, vil bakterier og andre nedbrydere respirere og omdanne kulstoffet til carbondioxid. Dette kræver, at der er dioxygen til stede, og er der ikke nok af dette, vil det døde, organiske materiale samle sig og med tiden synke ned i undergrunden, hvor det under højt tryk og temperatur kan omdannes til de fossile brændstoffer gas, kul og olie.
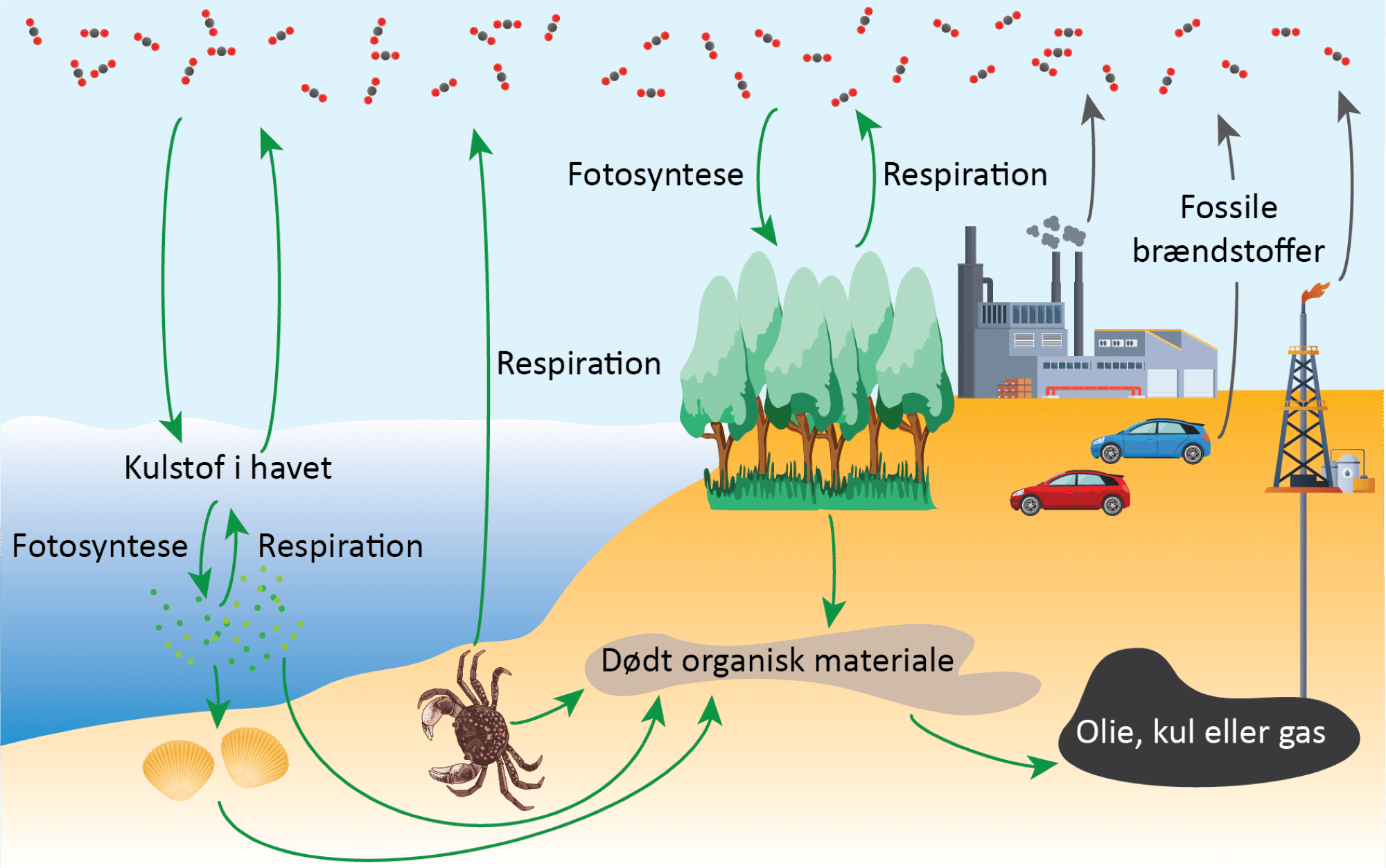
Fotosyntesen og respirationen er to relativt hurtige processer, hvor fx nogle af de ældre træer i Danmark som bøg og eg kan blive hhv. 300 og 1000 år gamle, mens græs vokser hen over sommeren. Når du klipper græsset, nedbrydes det afklippede græs temmelig hurtigt og forsvinder ofte inden du klipper det næste gang, mens et dødt egetræ tager mange år om at blive nedbrudt til CO₂. Nok kan 100 år virke som lang tid, men det er ingenting sammenlignet med omdannelsen til fossile brændstoffer, der tager millioner af år. Omvendt tager det ikke lang tid at udgrave kul eller pumpe olie og gas op fra undergrunden og brænde det af. Du kan se denne korte video om dannelsen af kul, og denne video om dannelsen af olie.
Du skal nu prøve at regne på omdannelsen af dieselolie til carbondioxid og vand.
Et eksempel på en organisk forbindelse i dieselolie kunne være C12H24. Når den afbrændes, sker følgende reaktion:
| C12H24 + O2 → CO2 + H2O | (8) |
1. Først skal du give et bud på tilstandsformer for alle stofferne. Herefter må du gerne prøve at undersøge det nærmere på nettet. Hint: Hvordan vil du normalt beskrive olie?
2. Afstem reaktionsskemaet.
3. Hvis du afbrænder 1 kg dieselolie, hvor meget carbondioxid producerer du så?
Se mere
Flybrændstof består af en blanding af mange organiske stoffer baseret på fossile brændstoffer. Der vil derfor være mange forskellige reaktionsskemaer og ikke kun ét som i opgave 5, og derfor er det svært at lave en nøjagtig beregning på, hvor meget CO₂, du ville udlede, hvis du fx fløj fra Europa til Nordamerika. Men der er alligevel lavet forskellige overslag på det. Her er der lavet en sammenligning af to forskellige flytyper, hvor man beregner udledningen af CO₂ per person og bagefter estimerer, hvor meget ekstra der kommer oveni, når man også tager i betragtning, at olien skal pumpes op fra jorden, den skal transporteres, den skal forbi et olieraffinaderi og omdannes, flyet skal produceres og vedligeholdes, piloter og folk i lufthavnen skal ansættes, lufthavnen skal bygges, vedligeholdes, opvarmes osv.
1. Læs beregning nr. 1 (”Basis 1 for calculation”).
2. Hvor meget CO₂ udleder de to typer af fly i timen per passager?
3. Hvad bliver den samlede CO₂-udledning per passager per time, når alt tages med i betragtning?
4. Kan du gennemskue, om der er nogle usikkerheder i antagelserne, der ligger til grund for beregningerne?
Se mere
ChatGPTs strømforbrug, vedligehold og drift af servere og nedkøling resulterede i 2025 i en CO₂-udledning per måned, der svarer til 260 transatlantiske flyvninger, når man ikke medregner de ekstra udgifter med at pumpe olien op m.m.?
Den enkelte søgning på ChatGPT giver en CO₂-udledning på 1,59 g per side, men fordi der er virkelig mange mennesker, der bruger platformen, resulterer det i så høj CO₂-udledning. Det skyldes blandt andet, at der skal bruges strøm til at holde de store datacentre i gang, der gemmer og behandler billeder, videoer og beskeder. Og de skal også køles ned. Men der er faktisk andre velkendte platforme, der af samme årsager har en høj CO₂-udledning, som du kan se i figur 41.
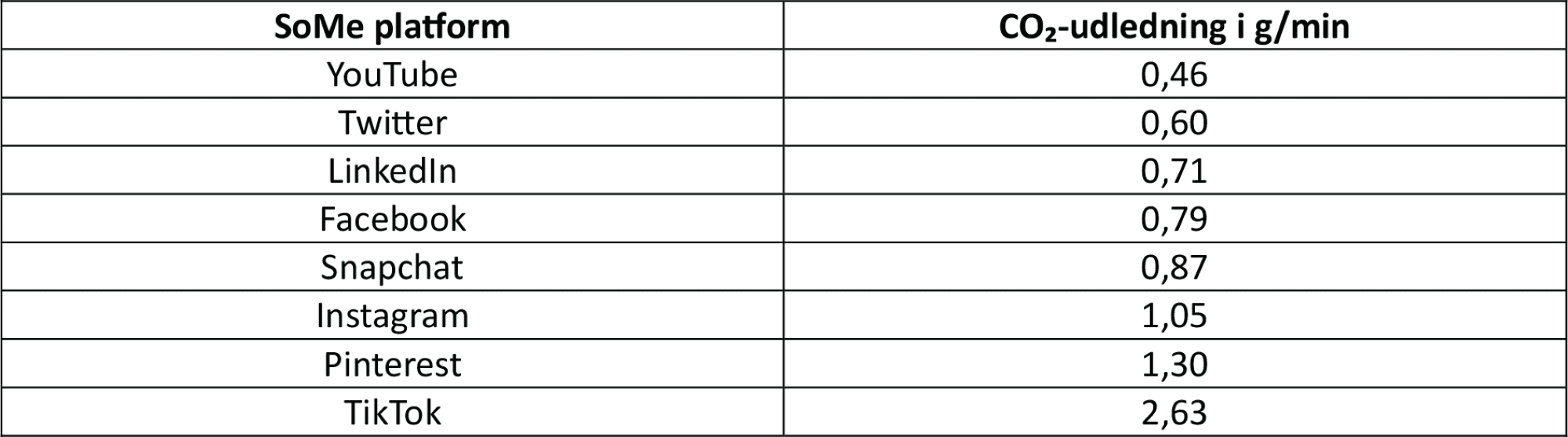
Diskutér i grupper, hvor meget tid I bruger på de forskellige sociale medier per dag, og lav et overslag over, hvor meget CO₂ I tilsammen har udledt den seneste uge.
Se mere
Det er rigtig godt, at du og andre bliver bevidste om jeres påvirkning af klimaet. Klimaaftrykket fra dit individuelle SoMe-forbrug er relativt lille sammenlignet med udledning af carbondioxid fra transportsektoren, tøjforbrug og fødevareproduktion. Herudover er der heldigvis mange tech-virksomheder, der investerer i vedvarende energi og energieffektive datacentre.
Nu ved du mere om, hvor carbondioxiden i atmosfæren kommer fra, og at en del skyldes menneskelige aktiviteter. Men hvad er problemet med, at koncentrationen stiger? Det kan du læse mere om i faktaboksen ’Drivhuseffekten’.
Drivhuseffekten resulterer i global opvarmning
Solens stråler består af en blanding af alle de farver af lys, som du kan se, og også ultraviolet lys, røntgenstråler, gammastråler, infrarøde stråler, mikrobølger og radiobølger (se figur 42), der tilsammen udgør det elektromagnetiske spektrum.
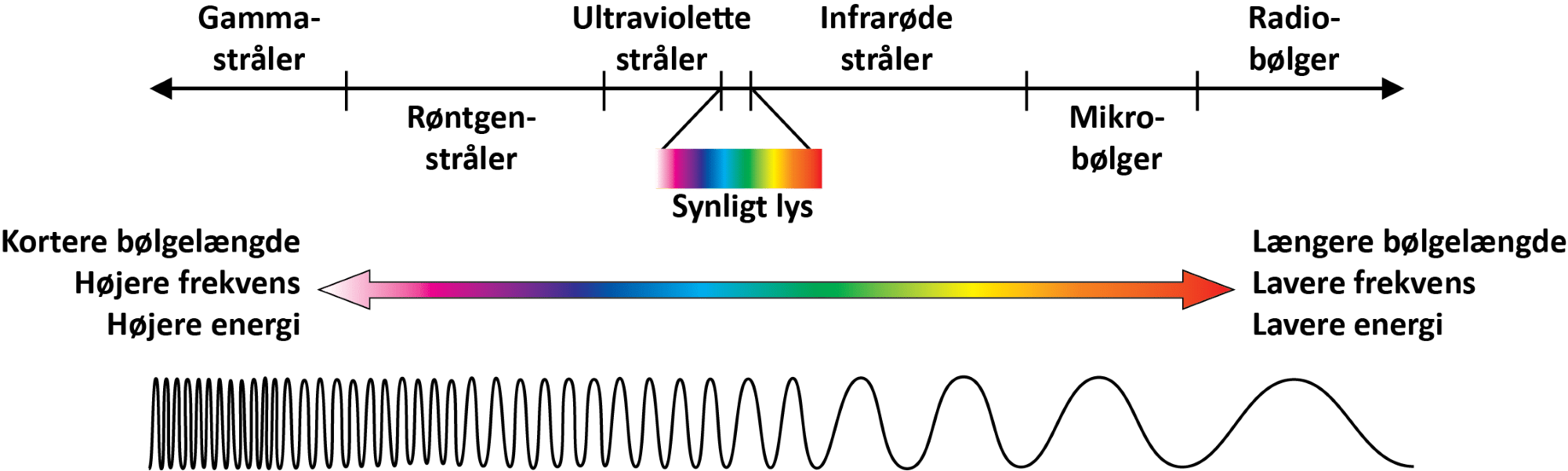
Du kan lære meget mere om bølger i fysik, men også kemikere gør brug af næsten hele det elektromagnetiske spektrum, som er vist i figur 42, til at undersøge molekyler. For at forstå drivhuseffekten er det tilstrækkeligt at vide, at jo større bølgelængden er (afstanden fra bølgetop til bølgetop), jo lavere energi har strålingen.
Når solens stråler rammer jordens atmosfære og især skyerne, vil en del af dem reflekteres og stråle tilbage ud i rummet (se figur 43). Hvis de rammer lyse områder på jordens overflade som fx sne og is, reflekteres sollyset også. Dette kaldes for albedoeffekten. Albedo er et mål for, hvor meget en overflade kan reflektere lys og dermed også den tilhørende energi. Forskellen mellem hvor varmt, det er at have en hvid eller sort t-shirt på i solen en varm sommerdag, kender du sikkert allerede. Dette skyldes albedoeffekten, og at farven i den sorte t-shirt absorberer mere sollys. Du kan se mere om albedoeffekten her.
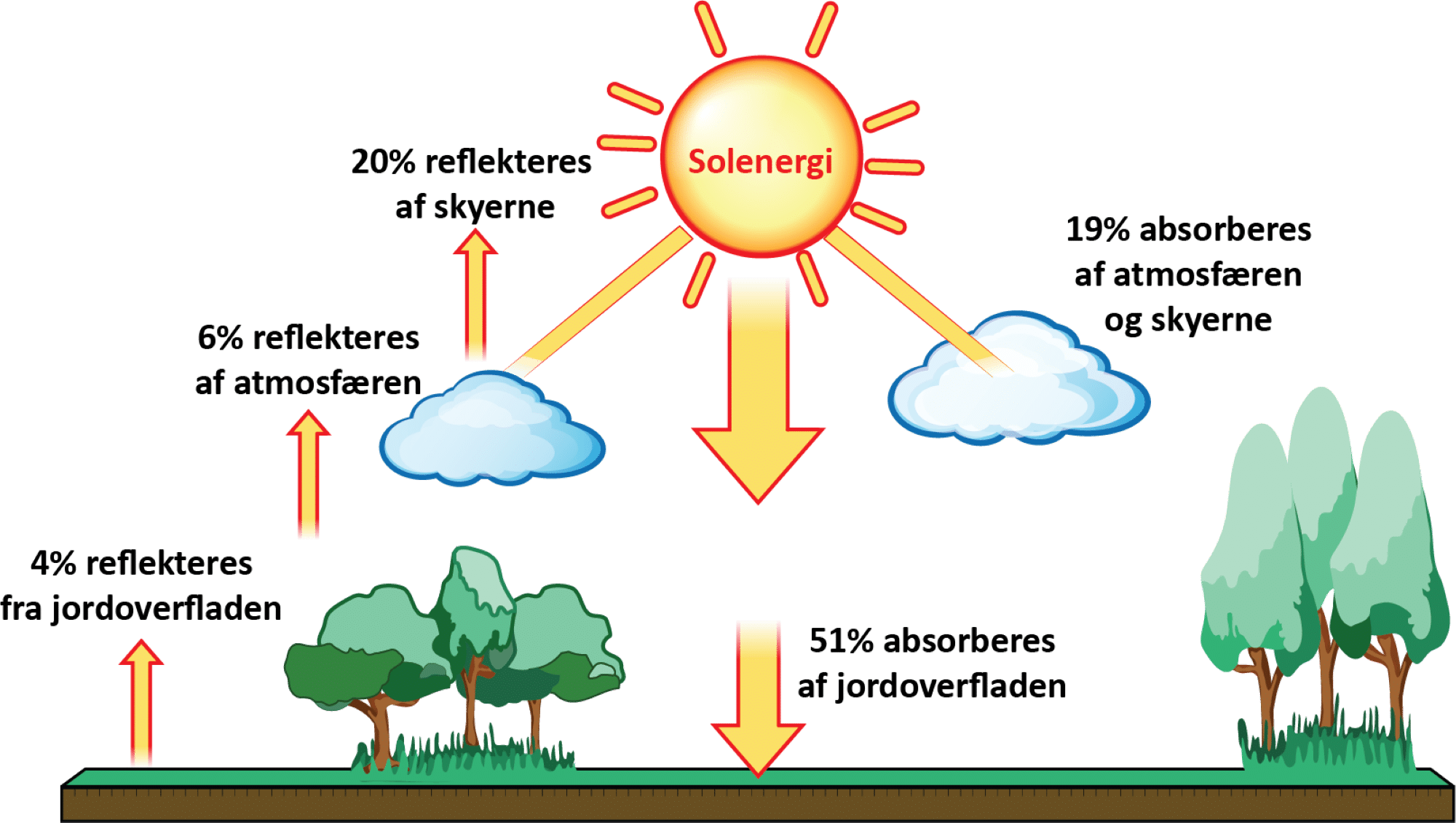
Det er især de kortbølgede, energirige stråler fra solen, der trænger igennem atmosfæren og rammer jordens overflade. Afhængigt af farven på den overflade, som strålerne rammer, som altså styres af albedoeffekten, bliver overfladen mere eller mindre varm. Der overføres altså energi fra de kortbølgede stråler til jordens overflade, som omdannes til varmeenergi, der har en længere bølgelængde. Herefter udsender overfladen varmestråling tilbage mod rummet, og den er i det infrarøde område, og dermed har strålingen lavere energi, og bølgelængden er større (se figur 42 ovenfor).
Den langbølgede varmestråling har en bølgelængde, der passer præcist til, at nogle af atmosfærens gasser absorberer den. Disse gasser er drivhusgasserne, som er vist i figur 44, og de fleste af disse forekommer naturligt i atmosfæren. Drivhusgasserne sender herefter nogle af strålerne ud i rummet og andre tilbage mod jordoverfladen. Det er faktisk ret heldigt, for uden drivhusgasser ville jordens overfladetemperatur være ca. -19°C, mens den nu er ca. 15°C.
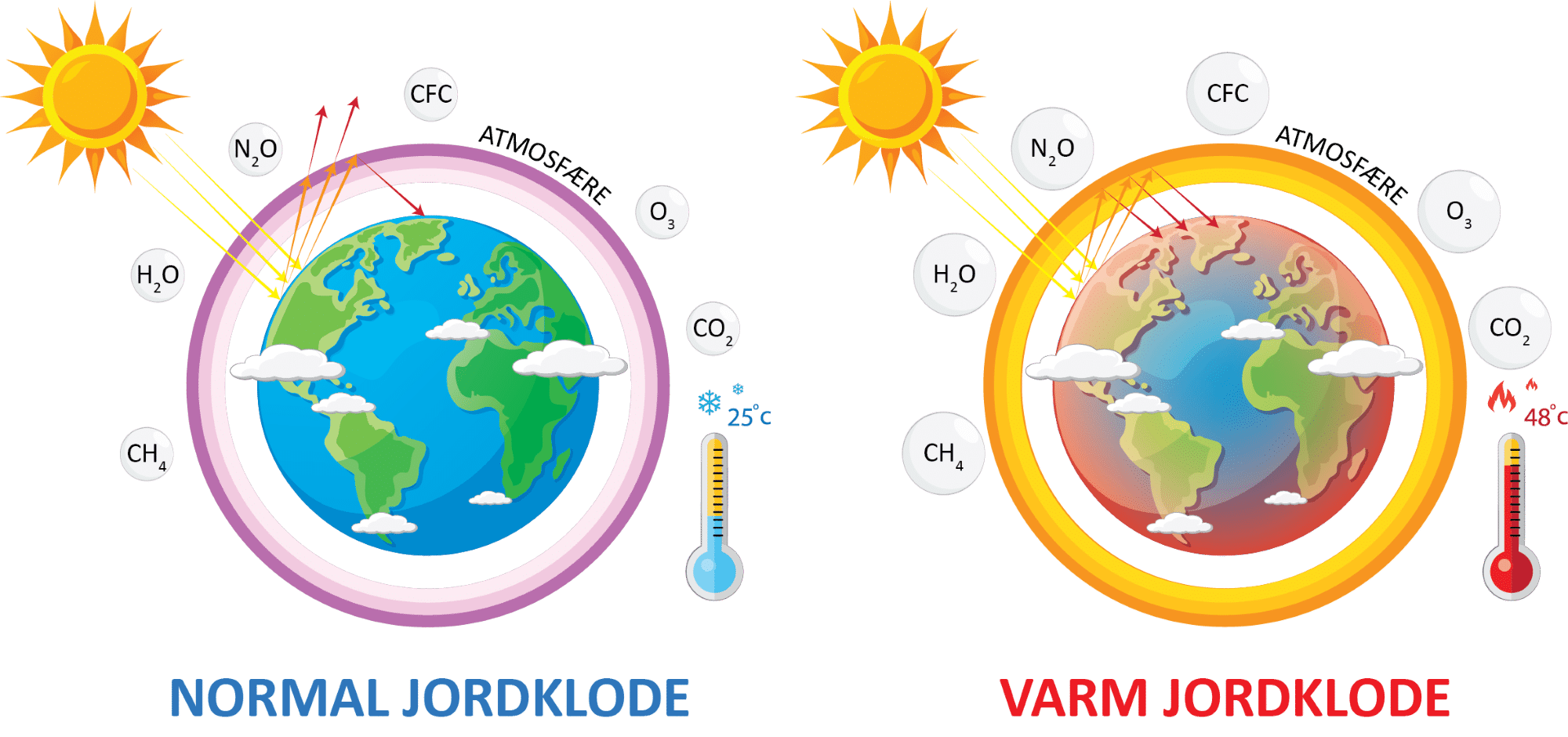
Men nu opstår problemet. Jo højere koncentrationen af drivhusgasser er, jo sværere er det for varmestrålingen fra jordoverfladen at passere forbi og videre ud i rummet. Og som du måske lagde mærke til i opgave 4, så er koncentrationen af drivhusgassen carbondioxid i atmosfæren stigende, og dermed er jordens gennemsnitstemperatur også stigende. Vi er godt i gang med den globale opvarmning. Du kan her se en kort video, der opsummerer drivhuseffekten og konsekvensen heraf.
Se mere
Drivhusgasser absorberer ikke lige meget varmestråling. Og nogle har en længere levetid end andre. For at kunne sammenligne forskellige drivhusgasser bruger man begrebet Global Warming Potential (GWP). GWP angiver, hvor meget varme en gas fanger i atmosfæren i forhold til CO₂ over en bestemt tidsperiode (normalt 100 år).
Carbondioxid får værdien 1 som reference. En gas med GWP på 25 betyder, at 1 kg af gassen varmer jorden 25 gange mere end 1 kg carbondioxid over 100 år.
1. Du skal læse artiklen ’Some Greenhouse Gases Are Stronger than Others’.
2. Brug GWP-værdien til at sammenligne, hvor mange gange ’stærkere’ følgende gasser er sammenlignet med carbondioxid:
a. Methan
b. Dinitrogenoxid
3. Søg på nettet efter GWP-værdier for de andre drivhusgasser, du har mødt. Da CFC-gasser er en gruppe af gasser, kan du ikke finde en enkelt værdi, men du kan måske finde den for CFC-12.
4. Forklar med egne ord, hvorfor nogle gasser er ’stærkere’ end carbondioxid.
5. Diskutér hvilken gas myndighederne bør prioritere at reducere først, hvis der udledes lige meget af dem, men de har forskellig ’styrke’.
Se mere
Når solens stråler rammer Jorden, opvarmes overfladen og udsender varmeenergi i form af infrarød (IR) stråling. For at et molekyle kan absorbere denne energi, skal bindingerne i molekylet kunne vibrere på en måde, der ændrer molekylets ladningsfordeling. Dermed kan symmetriske molekyler uden polære bindinger ikke optage IR-stråling, mens asymmetriske molekyler eller symmetriske molekyler med polære bindinger godt kan. Derfor kan dinitrogen og dioxygen ikke optage IR-stråling, mens vand, carbondioxid og de andre drivhusgasser gennemgået ovenfor godt kan.
Kun molekyler, der er asymmetriske eller indeholder polære bindinger, kan optage IR-stråling. Du skal gennemgå drivhusgasserne carbondioxid, methan, vand, ozon, dinitrogenoxid og CFC-gasserne en ad gangen og forklare, hvorfor de kan optage IR-stråling.
Se mere
Men hvad mon der sker, når et molekyle absorberer IR-strålingen? Du kan opfatte et molekyle som to atomer, der sidder sammen med en fjeder som vist i figur 45. Molekylets atomer vil vibrere i forhold til hinanden, fordi bindingen/fjederen mellem dem enten kan strække sig eller bøje sig. Hvis der tilføres energi i form af IR-stråling, vil disse bevægelser ske hurtigere. Molekylet kan derefter afgive energien igen som varme til omgivelserne, når det kolliderer med andre molekyler i luften. Resultatet er, at varmen ’fanges’ i atmosfæren, fordi strålingen ikke slipper direkte ud i rummet, men i stedet omsættes til varme i luften.
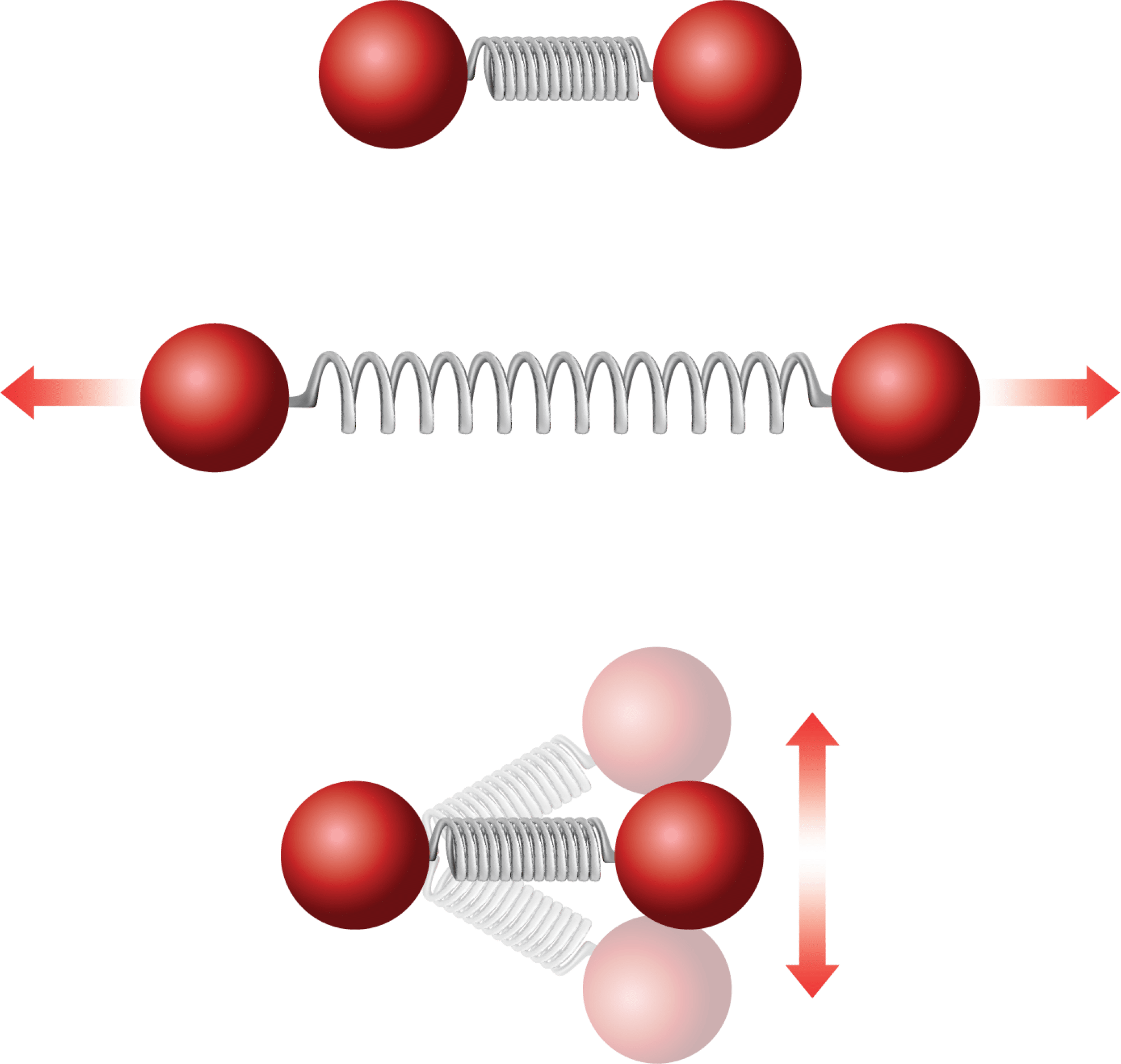
Du vil lære mere molekylers absorption og emission af IR-stråling på A-niveau, hvor du vil lære om IR-spektroskopi. En lille teaser er dog, at et molekyle ikke kan optage IR-stråling i hele spektret men kun med bestemte bølgelængder og dermed energier. Dermed kan du bruge IR-stråling til at lave et ’fingeraftryk’ af et molekyle, så du kan finde ud af, hvilket der er tale om. Det samme sker i atmosfæren: hvert molekyle absorberer nogle bestemte bølgelængder, men ikke dem alle sammen. Det er dog stadig nok til at opvarme hele jorden.
Du har nu fået en introduktion til, hvordan molekyler kan optage og udsende IR-stråling, og hvorfor det er netop drivhusgasserne, der spiller en central rolle i klimaforandringerne. For at forstå den samlede effekt på klimaet er det dog ikke nok kun at se på gasserne. Det kan også være godt for dig at have styr på de centrale begreber, forskere bruger, når de beskriver klimaets udvikling. Derfor får du i figur 46 en oversigt over nogle af de vigtigste klimabegreber, som hjælper dig med at sætte drivhusgassernes virkning ind i en større sammenhæng.

Atmosfæren er ikke bare en blanding af gasser og partikler. Den er et dynamisk kemisk system, hvor stoffer hele tiden reagerer med hinanden. Det gælder både reaktioner mellem forskellige gasser, fx dannelse og nedbrydning af ozon, og reaktioner på overfladen af aerosolpartikler, som kan fungere som små ’kemiske laboratorier’ i luften.
Her er en oversigt over nogle af reaktionstyperne, der sker i luften. Flere af dem kender du måske i forvejen.
1. Syre-basereaktioner:
NH3(g) + HNO3(g) → NH4NO3(s)
(9)
Ammoniak fra landbruget kan reagere med salpetersyre, der dannes i luften ud fra forskellige nitrogenoxider. Det danner ammoniumnitrat, som vha. partikler i luften påvirker luftkvalitet og sundhed.
2. Redoxreaktioner:
SO2(aq) + H2O2(aq) → H2SO4(aq)
(10)
Svovldioxid stammer bl.a. fra forbrænding af svovlholdige fossile brændstoffer, mens hydrogenperoxid dannes ved radikalreaktioner (se punkt 4). Begge gasser kan enten reagere i gasfase eller opløses i vanddråber i luften og reagere.
3. Fotokemiske reaktioner:
N2O(g) → N2(g) + O(g)
(11)
Dinitrogenoxid nedbrydes til dinitrogen og frie oxygenatomer i atmosfæren pga. UV-stråling. Dette er et eksempel på en fotokemisk reaktion, som sker højt oppe i atmosfæren, hvor der er tilstrækkeligt med kortbølget lys.
4. Radikalreaktioner:
Radikaler er atomer, ioner eller molekyler med en uparret elektron. De er meget reaktive. Ozon nedbrydes ved påvirkning af UV-lys til dioxygen og et exciteret oxygenatom. Det exciterede oxygenatom har optaget energi fra UV-strålingen og befinder sig derfor i en højere energitilstand end normalt, hvilket gør det ekstra reaktivt (markeret med en stjerne i reaktionsskema (12)). Det kan derfor reagere med vanddamp og danne to hydroxylradikaler:
O*(g) + H2O(g) → 2 HO∙(g)
(12)
Læg mærke til den lille prik efter O’et i hydroxylradikalet. Det symboliserer den uparrede elektron. Hydroxylradikalet kan reagere i en radikalreaktion og kan fx nedbryde methan:
HO∙(g) + CH4(g) → ∙CH3(g) + H2O(g)
(13)
Herved dannes et nyt methylradikal, som gennem en række reaktioner til sidst ender primært som carbondioxid og vand. På denne måde nedbrydes drivhusgassen methan over tid til drivhusgassen carbondioxid, som har en lavere GWP-værdi, men en længere levetid end methan. Du kan læse mere om hydroxylradikalets vigtige betydning i ’Faktaboks: Den atmosfæriske støvsuger’ (på vej).
Du har nu set eksempler på, hvilke kemiske reaktioner der finder sted i atmosfæren. Men reaktioner foregår ikke alle lige hurtigt. Nogle sker næsten øjeblikkeligt, mens andre kan tage timer, dage eller endnu længere. Netop forskellen i hastighed er afgørende for, hvor stor betydning en reaktion får i atmosfæren, og hvordan vi kan beskrive og forudsige dens effekt. Det er fx vigtigt at vide, hvor længe der går, før en given drivhusgas er nedbrudt og ikke længere bidrager til opvarmning. Derfor ser vi nu nærmere på begrebet reaktionshastighed.
5 Er alle kemiske reaktioner lige hurtige?
For at forstå reaktionshastighed behøver vi ikke blive oppe i atmosfæren. Faktisk møder du reaktionshastighed i din hverdag hele tiden. Selv i noget så simpelt som at lave en kop kaffe eller te. Før vi går i gang med kemien, starter vi derfor med et lille tankeeksperiment, hvor du skal bruge din hverdagsforståelse til at overveje, hvad der kan få noget til at ske hurtigere eller langsommere.
Din kemilærer har akut brug for kaffe efter en lang dag, men hun har brækket benet, og kaffemaskinen er langt væk. En klassekammerat tilbyder at lave en kop instant-kaffe og bringe den hen til hende.
Kaffen skal være rygende varm og med sukker i, og det skal ske så hurtigt som muligt. Inden I går i gang, stopper læreren jer:
’Vent lige. Hvis I vil gøre det hurtigt, bliver I nødt til at tænke kemisk.’
Tænk – og snak kort sammen i gruppen:
1. Sukkerets form
a. Hvad vil opløses hurtigst: løst sukker eller en sukkerknald?
b. Hvad er forskellen på de to, hvis du tænker på overfladeareal?
c. Hvordan kunne noget tilsvarende vise sig i et kemisk forsøg?
2. Omrøring
a. Hvorfor hjælper det at røre rundt i kaffen?
b. Hvad ændrer omrøring ved kontakten mellem sukker og vand?
c. Er omrøring en egenskab ved stoffet eller ved måden, forsøget udføres på?
3. Kopstørrelse
a. Tror du, sukkeret opløses hurtigere i en stor eller en lille kop kaffe?
b. Hvad betyder mængden af vand i forhold til mængden af sukker?
c. Hvordan hænger det sammen med koncentration?
4. Ét valg ad gangen
a. Hvis du ville undersøge, hvad der betyder mest, hvorfor ville det være en dårlig idé at ændre flere ting på én gang?
b. Hvad skal man gøre i stedet, hvis man vil kunne forklare sine resultater?
5. Klassens konklusion
a. Hvordan får I hurtigst muligt lavet koppen med kaffe og sukker til jeres lærer?
Din kemilærer har akut brug for kaffe efter en lang dag, men hun har brækket benet, og kaffemaskinen er langt væk. En klassekammerat tilbyder at lave en kop instant-kaffe og bringe den hen til hende.
Kaffen skal være rygende varm og med sukker i, og det skal ske så hurtigt som muligt. Inden I går i gang, stopper læreren jer:
’Vent lige. Hvis I vil gøre det hurtigt, bliver I nødt til at tænke kemisk.’
Tænk – og snak kort sammen i gruppen:
1. Sukkerets form
a. Hvad vil opløses hurtigst: løst sukker eller en sukkerknald?
b. Hvad er forskellen på de to, hvis du tænker på overfladeareal?
c. Hvordan kunne noget tilsvarende vise sig i et kemisk forsøg?
2. Omrøring
a. Hvorfor hjælper det at røre rundt i kaffen?
b. Hvad ændrer omrøring ved kontakten mellem sukker og vand?
c. Er omrøring en egenskab ved stoffet eller ved måden, forsøget udføres på?
3. Kopstørrelse
a. Tror du, sukkeret opløses hurtigere i en stor eller en lille kop kaffe?
b. Hvad betyder mængden af vand i forhold til mængden af sukker?
c. Hvordan hænger det sammen med koncentration?
4. Ét valg ad gangen
a. Hvis du ville undersøge, hvad der betyder mest, hvorfor ville det være en dårlig idé at ændre flere ting på én gang?
b. Hvad skal man gøre i stedet, hvis man vil kunne forklare sine resultater?
5. Klassens konklusion
a. Hvordan får I hurtigst muligt lavet koppen med kaffe og sukker til jeres lærer?
Se mere
Nu skal du lave et kemisk forsøg, hvor magnesium reagerer med syre. Her gælder præcis de samme tanker som for kaffen: form, omrøring, koncentration og valg af betingelser. Denne gang er det ikke sukker, der opløses, men en kemisk reaktion, der udvikler gas.

Kan du få magnesium til at ‘boble’ hurtigt eller langsomt og finde ud af præcis hvilke ændringer i forsøgsbetingelserne, der styrer reaktionshastigheden?
Øvelsesvejledningen er på vej.
Som du måske har lagt mærke til i forsøgene ovenfor, forløber kemiske reaktioner ikke lige hurtigt. Nogle reaktioner er vi netop glade for er langsomme. Fx når jernskelettet i Storebæltsbroen langsomt ruster, så vi har tid til at opdage og reparere det, eller når insulin til diabetikere er designet til at nedbrydes langsomt og dermed holde blodsukkeret stabilt over længere tid. Andre reaktioner er vi derimod afhængige af sker hurtigt: når tandlægen hærder en plastikfyldning med UV-lys, så den kan bruges næsten med det samme, eller når kroppen lynhurtigt producerer energi, mens vi spurter for at nå bussen. Reaktionshastighed er altså afgørende både i laboratoriet, i kroppen og i hverdagen, og det er derfor et centralt begreb i kemi.
Du kender selv til begrebet hastighed, når du fx kører i bil eller på cykel, løber eller går. Hvis du skal beregne gennemsnitshastigheden af en bil, som kører fra Aarhus til Aalborg, så skal du kende to ting: Afstanden mellem Aarhus og Aalborg og tiden, det tager at køre denne afstand (se figur 47).
Bilen er en time om at køre de 100 km, og derfor kører den med en hastighed på 100 km/t. I hvert fald i gennemsnit, for bilen kan jo godt have kørt hurtigere på dele af strækningen og langsommere på andre dele. Det vender vi tilbage til.
Det er en fordel at stille regnestykket en smule mere matematisk op, for så bliver det lettere for dig nedenfor at forstå, hvordan du kan beregne reaktionshastigheden for en reaktion.
Hastighed (engelsk: velocity) har symbolet v, tid har symbolet t og afstand har symbolet d (engelsk: distance). For at regne gennemsnitshastigheden ud for bilturen ovenfor, kan du stille det sådan op:
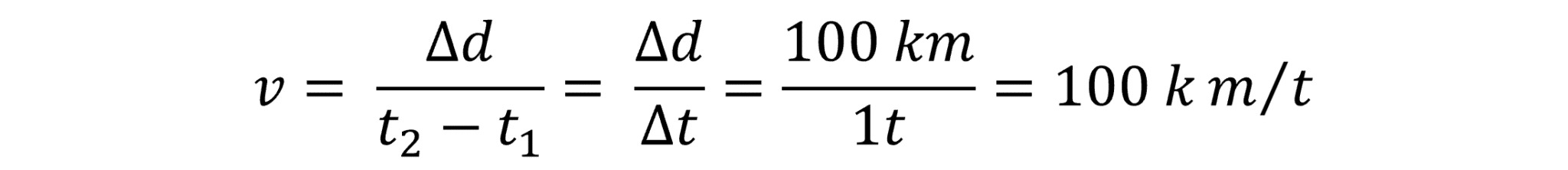
t2 svarer til tidspunktet, du er ved destinationen, dvs. kl. 18.15, og t1 svarer til tidspunktet, du starter din rejse, dvs. kl. 17.15. Symbolet delta, Δ, betyder forskel og dermed to tal, der trækkes fra hinanden.
Reaktionshastigheden siger noget om, hvor hurtigt en reaktion forløber. Symbolet for reaktionshastighed er også v ligesom ovenfor. Her er en generel reaktion fra reaktant til produkt:
![]()
Figur 48 viser, at koncentrationen af produktet stiger over tid, mens koncentrationen af reaktanten falder. På et tidspunkt ændres koncentrationen ikke længere, og så er reaktionen i ligevægt. Du kan læse mere om ligevægte i temaet ’CO₂ – fra klimasynder til byggesten’.
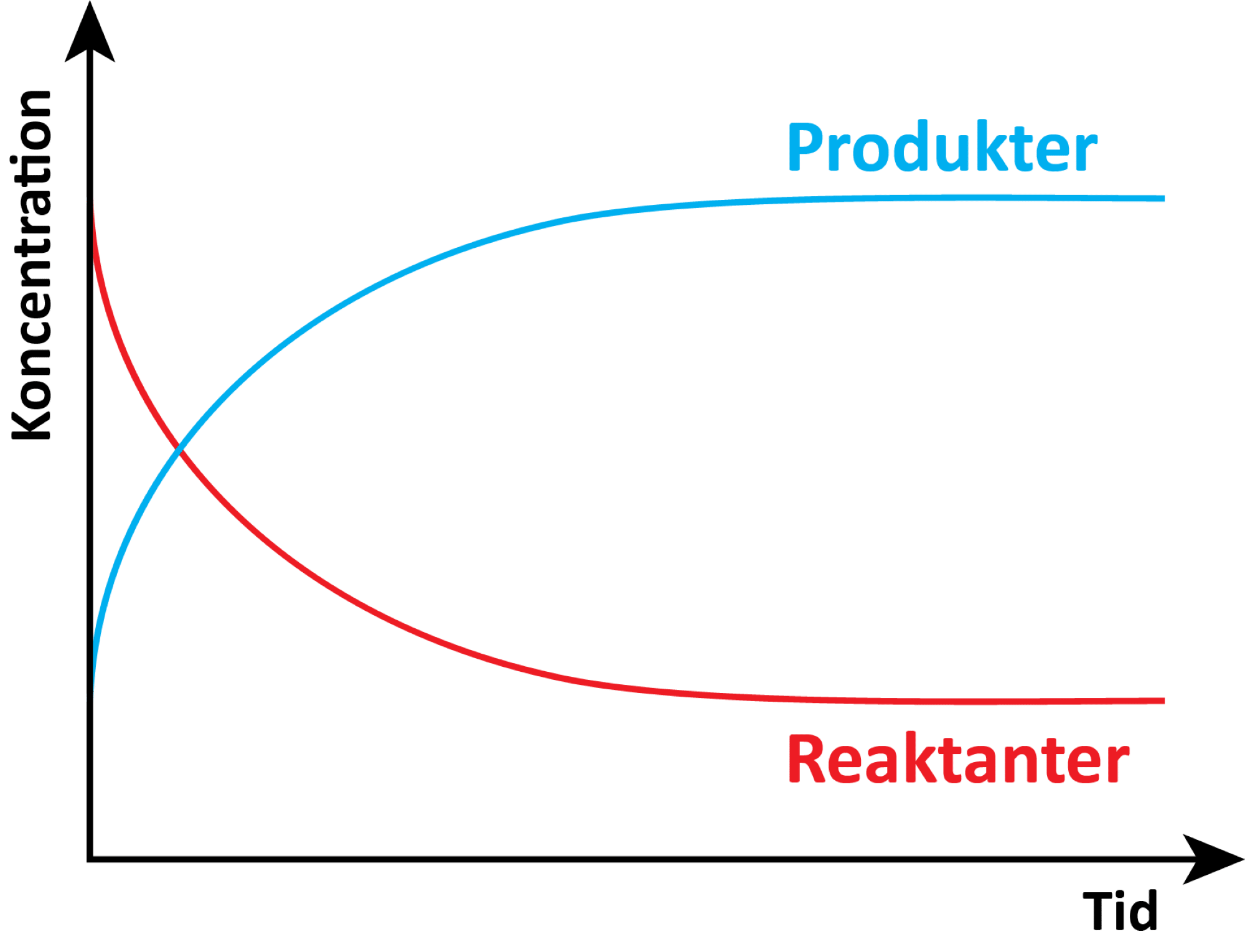
Når du kører fra Aarhus til Aalborg i en almindelig benzinbil, omdannes benzinen til carbondioxid og vand. Reaktanten, der er benzin, forbruges og der bliver mindre af den i benzintanken, mens der bliver mere produktet, carbondioxid, i atmosfæren.
C7H16(g) + 11 O2(g) → 7 CO₂(g) + 8 H2O(l)
(14)
Reaktionshastigheden for en given reaktion kan bestemmes efter samme princip, som da vi ovenfor beregnede gennemsnitshastigheden for bilen. I figur 49 kan du trin for trin se, hvordan man bestemmer reaktionshastighed ud fra koncentrationen af produktet.
I figur 49a kan du se, at koncentrationen af produktet, P, stiger, jo længere tid, der går.
I figur 49b kan du se, at til tidspunktet t1 er der en tilhørende produktkoncentration [P]1.
I figur 49c kan du se, at til tidspunktet t2 er der en tilhørende produktkoncentration [P]2.
I figur 49d kan du se, at der er tegnet en ret linje mellem de to punkter, og ud fra de to punkter kan den gennemsnitlige reaktionshastighed beregnes som hældningskoefficienten for linjen.
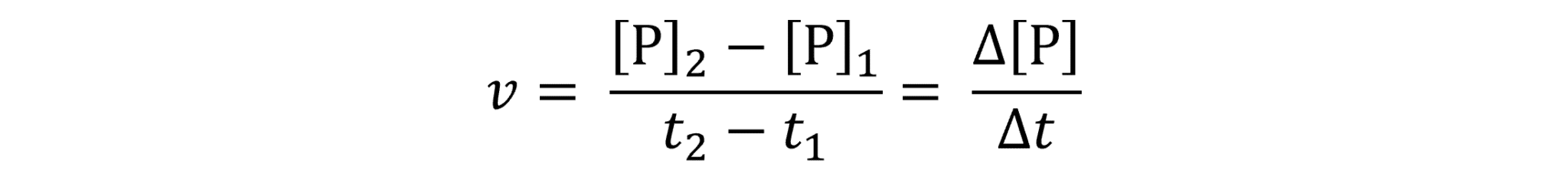
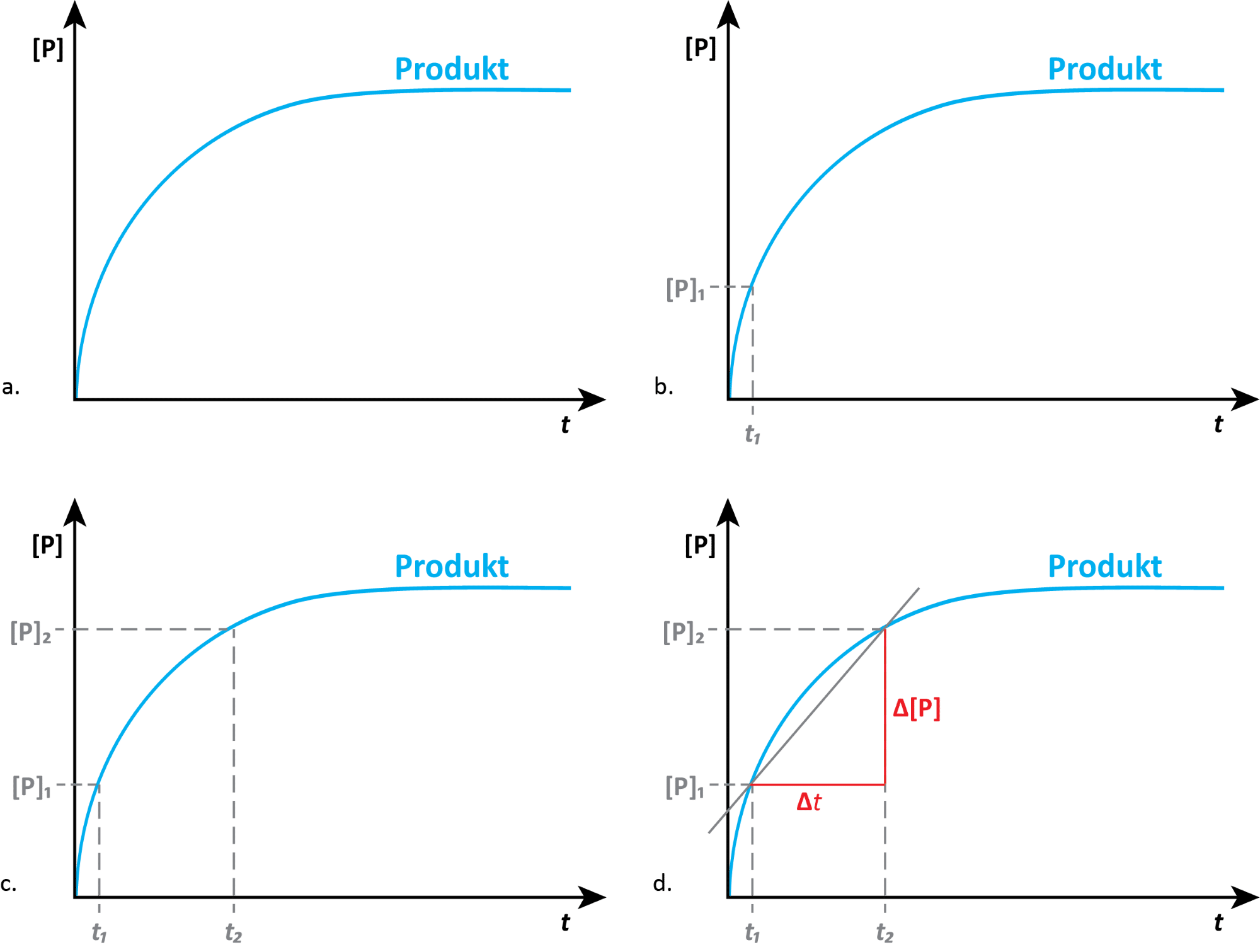
Tilsvarende kan du i figur 50 se, at reaktionshastigheden også kan bestemmes ud fra hvor meget reaktant, der forsvinder. Hvis du tegner den rette linje gennem de to punkter (t1, [R]1) og (t2, [R]2), bliver hældningskoefficienten negativ, og da man altid ønsker, at reaktionshastigheden er en positiv størrelse, sætter man et minus foran. Derfor kan den gennemsnitlige reaktionshastighed beregnes således:
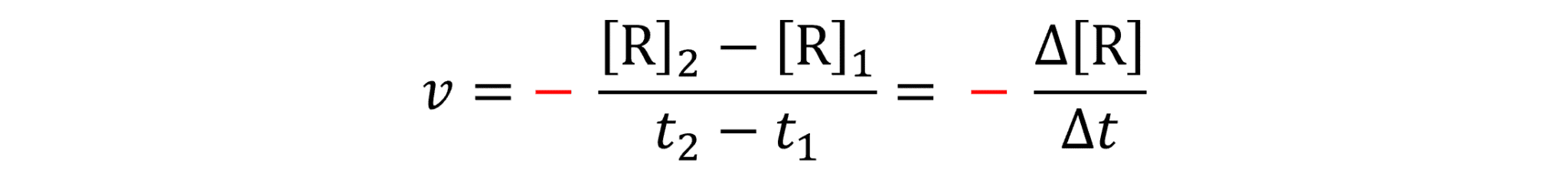
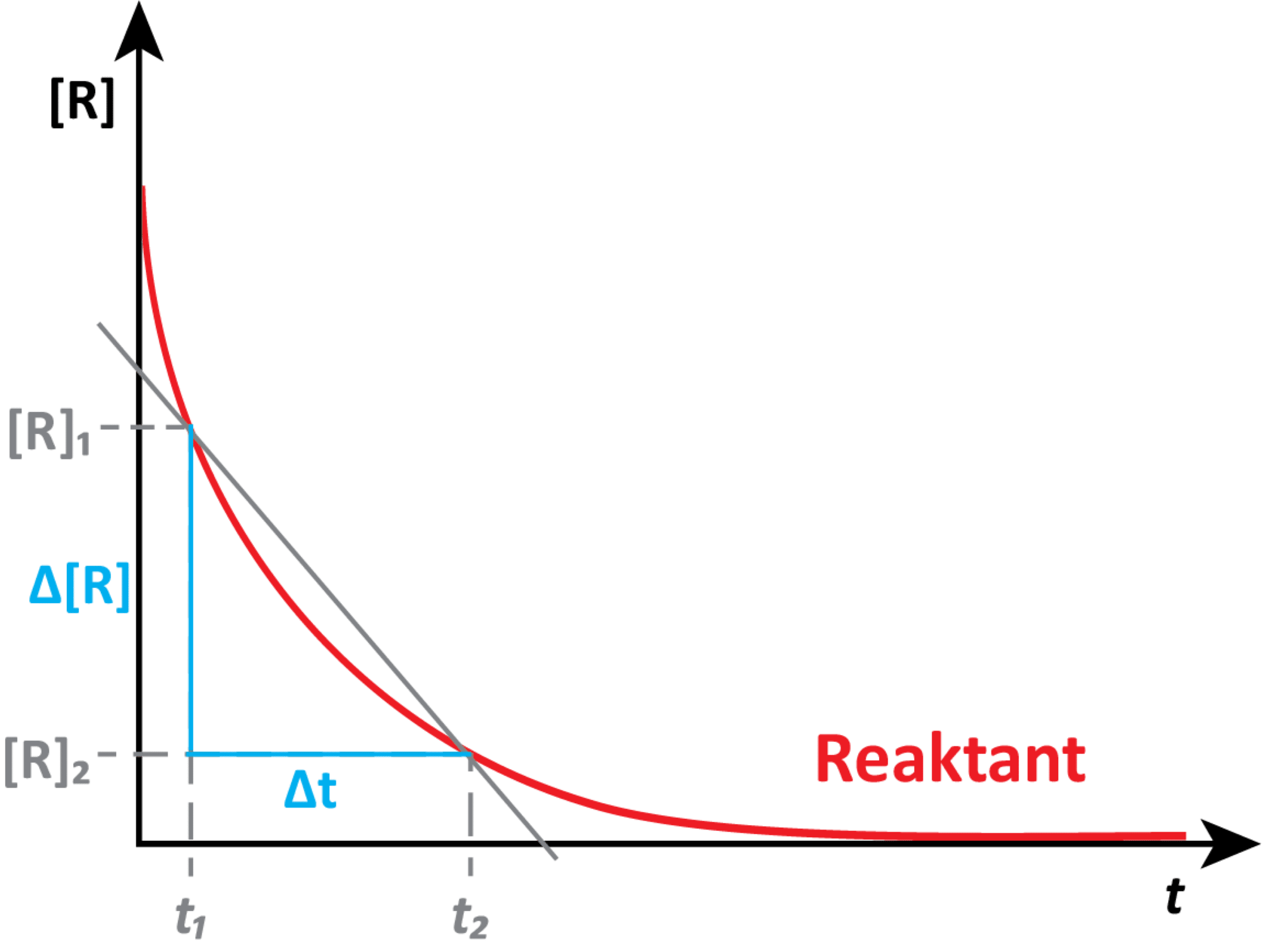
Definitionen af reaktionshastighed lyder:
Reaktionshastigheden, v, defineres som faldet i koncentrationen af en reaktant pr. tid
eller stigningen i koncentrationen af et produkt pr. tid.
Selvom bilen på turen fra Aarhus til Aalborg kørte med en gennemsnitsfart på 100 km/t, så kørte den jo ikke nødvendigvis 100 km/t på alle dele af turen. Den kan have kørt 20 km/t, hvis der var kø, og 130 km/t, når trafikken gled let. Det samme gælder for reaktionshastigheden. For at finde reaktionshastigheden til et bestemt tidspunkt, gør du tidsintervallet, du undersøger reaktionshastigheden for, så lille som muligt, indtil du undersøger en ret linje, der kun rører kurven i et enkelt punkt (se figur 51a). Dette svarer matematisk til at finde differentialkvotienten til koncentrationen pr. tid: v = d[P]/dt eller v = –d[R]/dt. Hvis du undersøger reaktionshastigheden, dvs. tangenthældningen, på flere tidspunkter som vist i figur 51b for produktet, P, så kan du se, at hældningskoefficienten falder, jo længere tid reaktionen har været i gang.
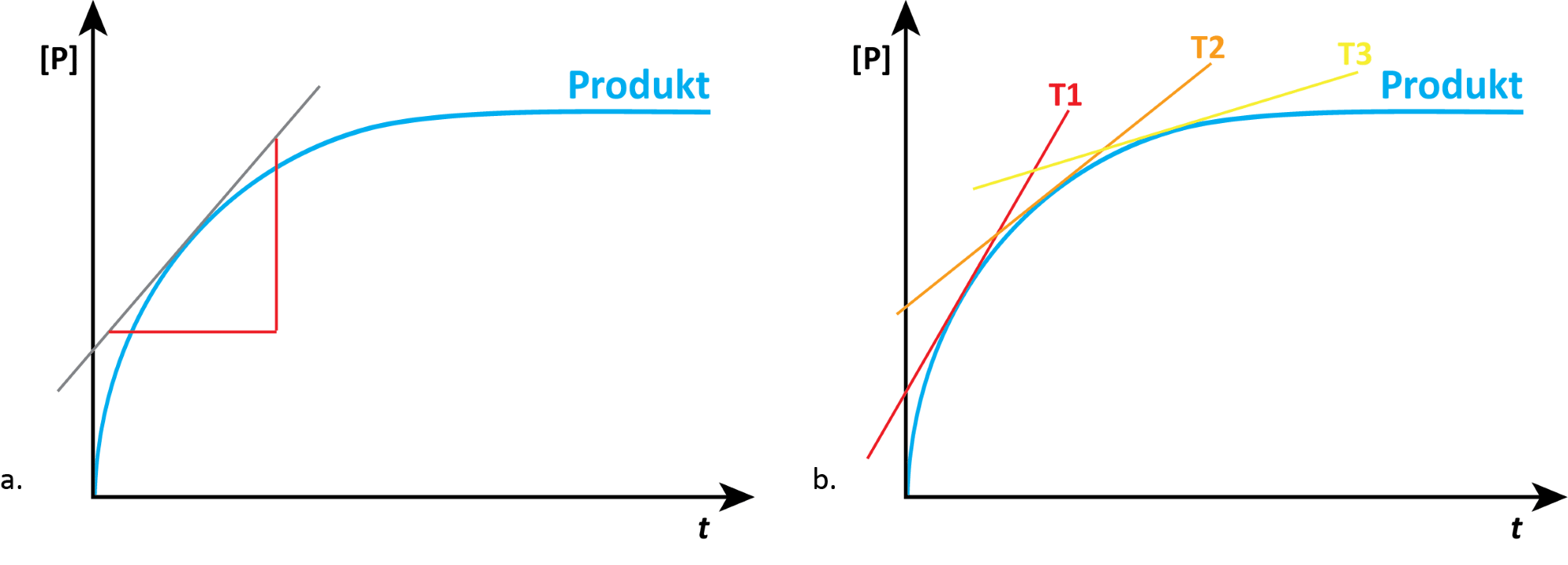
Dermed må reaktionshastigheden for en reaktion falde, jo længere tid den har været i gang. Det eneste, der ændrer sig kemisk, er koncentrationen af stofferne i reaktionen, og dermed må reaktionshastigheden være afhængig af koncentrationen af stofferne.
I en fiktiv kemisk reaktion, hvor en reaktant omdannes til et produkt, fås følgende datasæt:

1. Tegn grafen, der viser koncentration af R som funktion af tiden t, og i samme koordinatsystem tegn også grafen for koncentrationen af P som funktion af tiden t.
2. Beregn den gennemsnitlige reaktionshastighed (hældningskoefficient for den rette linje) i tidsintervallet fra 10 s til 50 s både for reaktant og produkt. Husk fortegn når du beregner hældningskoefficienten for reaktanten.
3. Beregn herefter den gennemsnitlige reaktionshastighed for produktet P i de to tidsintervaller fra 0-20 s og 40-60 s.
4. I opgave c beregnede du den gennemsnitlige reaktionshastighed i et tidsinterval på 20 sekunder på to forskellige tidspunkter i reaktionen. Er reaktionshastigheden ens i de to tidsintervaller? Hvorfor/hvorfor ikke? Brug evt. figur 51 som hjælp.
Se mere
Hvordan påvirker koncentrationen af stofferne i en reaktion reaktionshastigheden, og er der andre ting, der kan påvirke den?
I de tidligere forsøg har du måske lagt mærke til, at kemiske reaktioner ikke altid forløber med samme hastighed. Nogle reaktioner sker hurtigt, mens andre tager længere tid, selv når de involverer de samme stoffer. I forsøg 3 har du allerede fået de første erfaringer med, at koncentrationen af reaktanter kan have betydning for, hvor hurtigt en reaktion forløber, og måske har du også set, at temperatur og overfladeareal spiller en rolle.
I ’Forsøg 4: Kan du styre tiden i et kemisk ur?’ skal du selv undersøge, hvordan reaktionshastigheden kan påvirkes. Her arbejder du undersøgelsesbaseret med Landolts forsøg, hvor du systematisk ændrer koncentrationen af reaktanter og tilsætter syre som katalysator. Din opgave er at planlægge forsøget, gennemføre målinger og analysere dine resultater, så du kan vurdere, hvordan forskellige faktorer påvirker, hvor hurtigt reaktionen forløber.
Efter forsøget gennemgår vi de enkelte faktorer én for én og sætter dine observationer ind i en kemisk sammenhæng. Til sidst zoomer vi helt ind på, hvad der sker på molekylniveau, når stoffer reagerer. Her møder du kollisionsteorien, som forklarer, hvorfor ændringer i fx koncentration, temperatur og katalyse påvirker reaktionshastigheden.

Kan du kontrollere tiden, hvor opløsningen pludselig skifter farve, og bevise at du kan styre et kemisk ur?
Øvelsesvejledningen er på vej.
Lad os overføre din viden om, at koncentrationerne af reaktanterne spiller en rolle for reaktionshastigheden. Prøv denne brain break med din klasse eller brug den som en opgave:
Brain break: Reaktion ’high five’

Formålet er at undersøge reaktantkoncentrationens betydning for reaktionshastigheden. Fire elever står med en snor og danner fire hjørner i en stor firkant – det kan være udenfor eller i midten af klasselokalet, eller hvor der er plads. En af dem har et stopur. Resten af holdet skal inddeles i to hold – hold A og B. A- og B-elever skal finde hinanden og lave en high five. I skal have bind for øjnene eller lukke dem.

Runde 1:
Runde 2:
Refleksion:
Brain break: Reaktion ’high five’

Formålet er at undersøge reaktantkoncentrationens betydning for reaktionshastigheden. Fire elever står med en snor og danner fire hjørner i en stor firkant – det kan være udenfor eller i midten af klasselokalet, eller hvor der er plads. En af dem har et stopur. Resten af holdet skal inddeles i to hold – hold A og B. A- og B-elever skal finde hinanden og lave en high five. I skal have bind for øjnene eller lukke dem.

Runde 1:
Runde 2:
Refleksion:
Se mere
I forsøg 3 tilsatte du magnesiumbånd til forskellige typer syre (ja, vand er også en syre – og en base!), og her så du, at magnesiumbåndet blev hurtigere opløst i saltsyren end i ethansyren.
Diskutér med en makker, hvad det har med reaktantkoncentration at gøre.
Hint: Hvordan reagerer ethansyre og saltsyre hver især med vand, og dannes der lige meget oxonium i de to reaktioner?
Se mere
Lektor Marianne Glasius og professor Merete Bilde fra Aarhus Universitet har undersøgt luftforurening i Kinas større byer. Her har man set en glædelig reduktion af partikelforurening siden 2013 og frem efter indføring af en stram regulering, som du kan se i figur 52. Det er tale om PM2.5, der er partikler med en diameter mindre end 2,5 µm (se evt. figur 33).

Samtidig har man dog opdaget en stigning i ozonkoncentrationen ved jordoverfladen, hvilket kan have sundhedsmæssige konsekvenser for indbyggerne. Lad os kigge nærmere på dette dilemma.
Når bilmotorer forbrænder benzin og diesel, sker det ved høje temperaturer, og luftens dinitrogen og dioxygen reagerer og danner nitrogenmonoxid.
N2(g) + O2(g) → 2 NO(g)
(15)
Nitrogenmonoxid reagerer videre og danner nitrogendioxid:
2 NO(g) + O2(g) → 2 NO2(g)
(16)
Nitrogendioxid nedbrydes i en fotokemisk reaktion og danner nitrogenmonoxid og et oxygenatom.
NO2(g) → NO(g) + O(g)
(17)
De frie oxygenatomer reagerer med dioxygen og danner ozon:
O(g) + O2(g) → O3(g)
(18)
Når færre PM2.5 blokerer sollyset i 2025, som du kan se i figur 52, kommer en større mængde UV-stråler ned til jordoverfladen og giver den fotokemiske reaktion (17) ekstra energi, så dannelsen af de frie, exciterede oxygenatomer går hurtigere. Da det netop er reaktanten i reaktion (18), så forløber denne reaktion også hurtigere, og der dannes mere ozon.
Du har her mødt et eksempel på, at reaktantkoncentration har betydning for reaktionshastighed direkte fra forskning i atmosfærekemi.
Du skal ud fra informationen ovenfor forsøge at besvare følgende spørgsmål:
1. Hvilke forhold giver høje ozonkoncentrationer i byerne?
2. Hvilke forhold giver lave ozonkoncentrationer i byerne?
3. Forklar med egne ord, hvorfor koncentrationen af ozon stiger i byerne. Du skal bruge følgende fagord i din forklaring: Reaktionshastighed, reaktantkoncentration og fotokemisk reaktion.
4. Forklar, hvorfor reaktionerne (15-18) alle sker hurtigere, når der er flere biler i en by?
Se mere
der udover at blive dannet små partikler også dannes nitrogenmonoxid og nitrogendioxid, som vist i reaktionerne (15+16), når du brænder stearinlys hjemme? Nitrogendioxid er en skadelig gas, der i høje koncentrationer kan forværre sygdomme som astma og bronkitis. Men det dannes heldigvis i meget små mængder, så afbrænding af et stearinlys er som regel uproblematisk, især hvis du lufter ud bagefter.

Koncentrationen af reaktanter spiller en vigtig rolle for, hvor hurtigt en reaktion forløber. Men hvad er det egentlig, der sker på molekylært niveau, når en højere koncentration får en reaktion til at gå hurtigere?
I kollisionsteorien (link følger) dykker vi mere ned i detaljerne for at forstå, hvorfor reaktanters koncentration påvirker reaktionshastigheden, men først kan du læse et eksempel på, hvordan produktet i en reaktion også nogle gange kan påvirke en reaktions hastighed i faktaboksen om sædcelleproduktion.
Negativ feedback
I mange kemiske reaktioner afhænger hastigheden af, hvor stor koncentrationen af reaktanterne er. Jo højere reaktantkoncentration, jo hurtigere sker reaktionen. Men hvis produktet af en reaktion ophobes, kan det i nogle systemer få den modsatte effekt og bremse reaktionen. Et eksempel på dette findes i kroppen, hvor koncentrationer hele tiden reguleres, så der er balance.
Et eksempel er dannelsen af sædceller hos mænd. Her udsender hypofysen, en kirtel i hjernen, to hormoner til blodet. Det ene, LH, sætter gang i en række af biokemiske reaktioner, der resulterer i dannelsen af det mandlige kønshormon testosteron i testiklerne. Det andet hormon aktiverer produktionen af receptorer, der er molekyler, som kan binde til testosteron. Sammen sørger de for, at modningen af sædceller går i gang.
Noget af testosteronet sendes dog ud i blodet, og når koncentrationen her bliver høj, hæmmes produktionen af LH i hjernen. Dermed stopper signalet til testiklerne om at danne mere testosteron. Kroppen bruger altså koncentrationen af produktet fra en reaktion til at styre, hvor hurtigt reaktionen foregår. Denne form for selvregulering kaldes negativ feedback og sikrer, at kroppen kun producerer det, der er nødvendigt. Du kan se den negative feedbackregulering af sædcelleproduktion i figur 53.
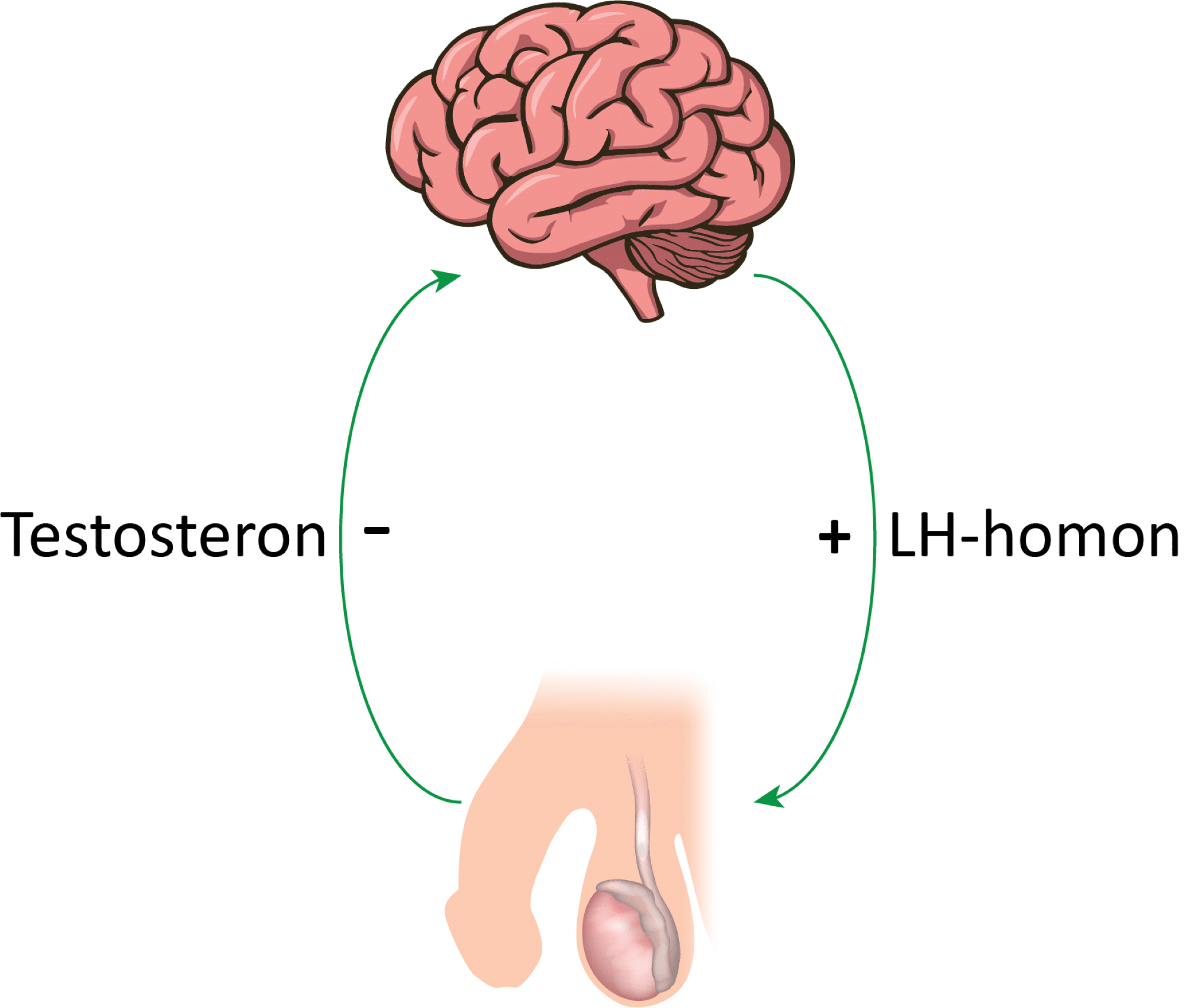
Se mere
Hvis du arbejdede med opgaverne i ’Brain break – den hurtigste kop kaffe’, fandt du måske ud af, at det gik hurtigere at opløse sukkeret frem for sukkerknalden. Det er, fordi overfladearealet er meget større på sukkeret end på sukkerknalden, og det skal du prøve at regne på i næste opgave.
En terning har sidelængden 4 cm.
1. Beregn terningens overfladeareal.
2. Terningen deles nu i 8 lige store terninger. Beregn det samlede overfladeareal af alle de små terninger.
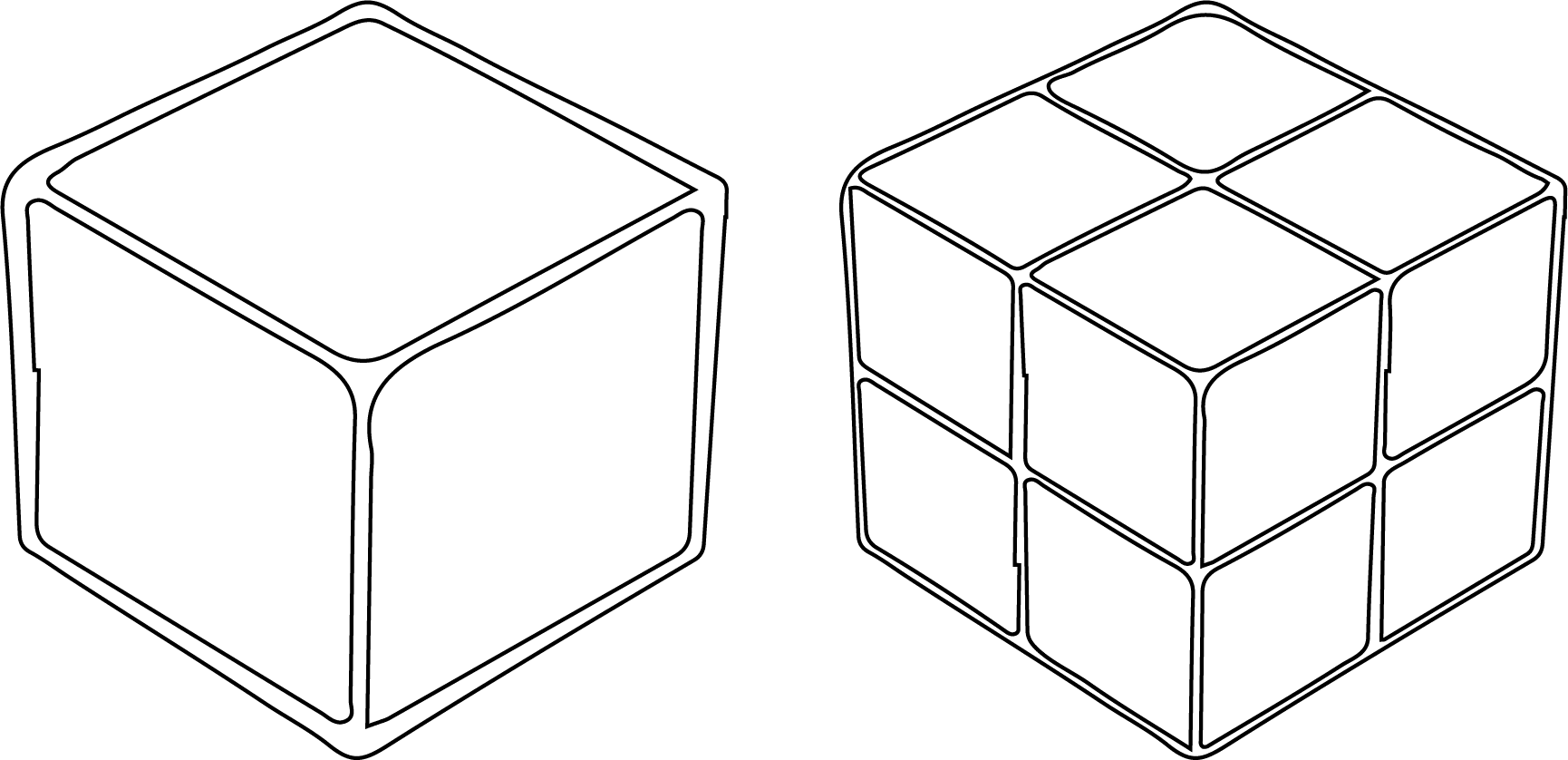
3. Hver af de nye terninger deles derefter igen i 8 mindre terninger. Beregn det samlede overfladeareal af alle disse.
Se mere
Når overfladearealet på sukkerkrystaller er stort, kan vandmolekylerne lettere trække sukkermolekylerne ud enkeltvis af krystallerne, fordi der er flere molekyler, der sidder på overfladen (se figur 54). Du kan selv tælle alle de sukkermolekyler, der er i kontakt med vandet i de to situationer i figuren.
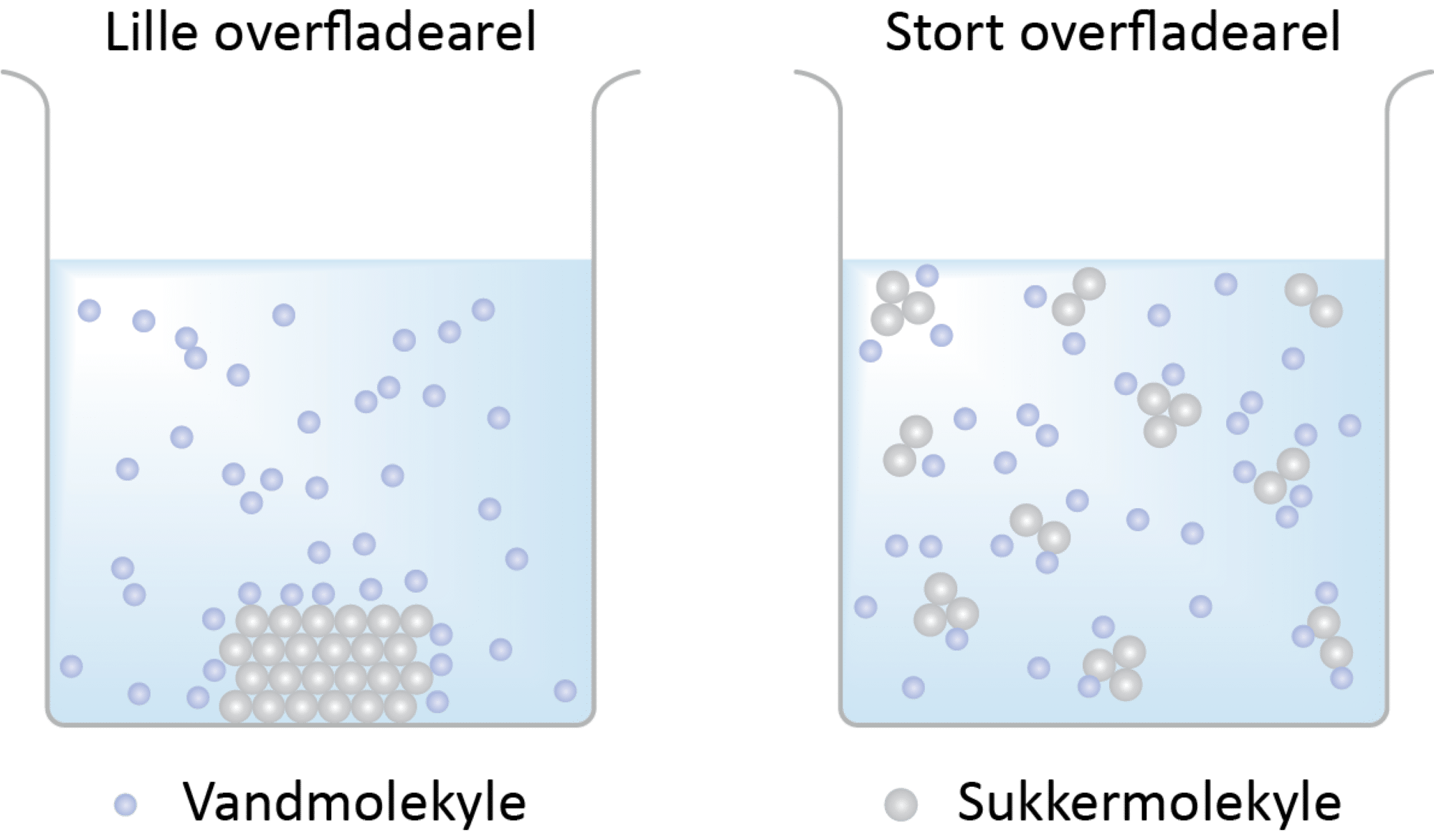
Det med det store overfladeareal kender du måske også fra hverdagen, når du spiser. Hvis du tygger maden grundigt, bliver smagen mere intens, fordi flere af smagsstofferne opløses i spyttet pr. tid. Der er også en grund til, at du skal tygge maden: når maden findeles, får den et større samlet overfladeareal, og det gør det lettere for fordøjelsesenzymerne i maven og tarmen at komme i kontakt med føden og nedbryde den effektivt. I figur 55 kan du se et eksempel på, hvordan enzymer i dit fordøjelsessystem nedbryder kulhydrater i din mad fra store, komplekse stivelsesmolekyler til mindre molekyler som maltose og glukose. Først når kulhydraterne er på monosaccharidform, optages de i kroppen, men før enzymerne kan gå i gang, har du tygget den stivelsesholdige mad i små nok stykker og øget overfladearealet, så amylaseenzymet kan gå i gang.
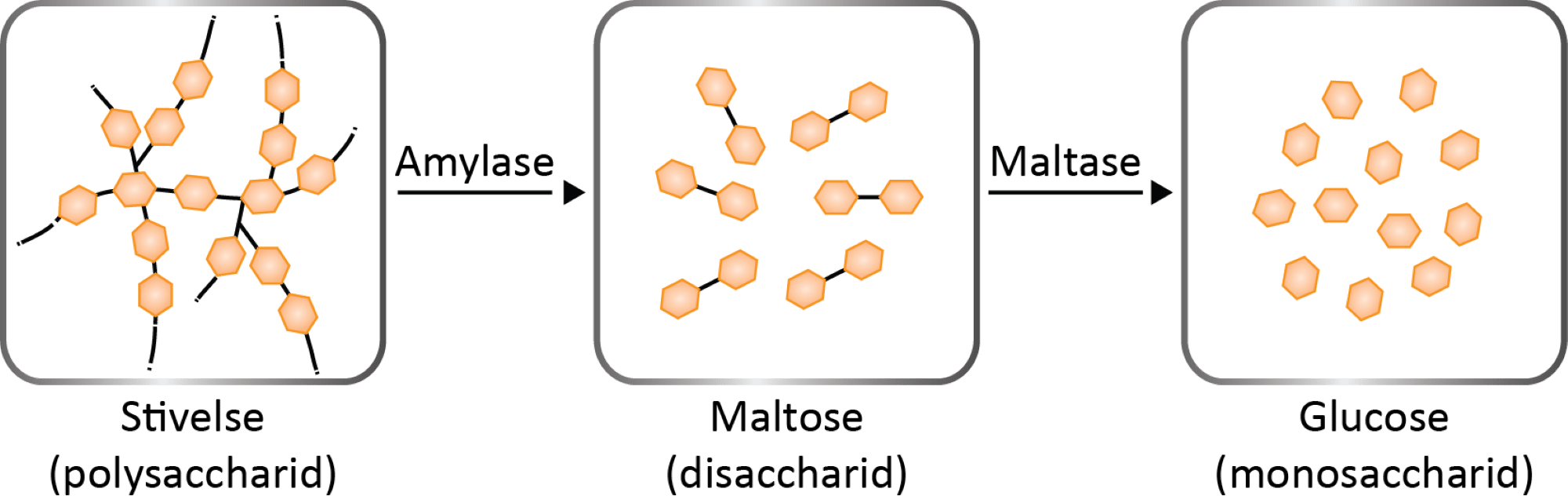
Det samme princip kan du opleve helt konkret med din egen krop. Når du spiser, handler smagsoplevelsen ikke kun om, hvad du spiser, men også om hvordan du spiser det. Når maden findeles i munden, øges overfladearealet, og flere smagsstoffer kan opløses i spyttet pr. tid. Det betyder, at smagen frigives hurtigere og opleves mere intenst.
I ’Forsøg 5: Chokolade’ kan du selv mærke, hvordan overfladeareal påvirker hastigheden af en proces.

Hvordan spiser du chokolade, og hvad betyder det for smagen?
I dette sanselige miniforsøg undersøger du, hvordan måden du spiser chokolade på kan frigive smagen hurtigere.
Overfladeareal har også betydning for en række kemiske reaktioner i luften.
Når du ser skyer på himlen, er de dannet af vanddråber. Størrelsen af vanddråberne er afgørende for hvor meget lys skyerne reflekterer og for deres påvirkning af jordens klima.
En sky kan blive mere hvid på grund af partikelforurening end den ellers ville være. Partikelforureningen giver anledning til flere små skydråber som kan reflektere sollys.
Farveforskellen på skyer med og uden partikelforurening kan man illustrere med knust is og isterninger, som du kan se i figur 56. Når der er et større overfladeareal på isen eller vanddråberne i skyerne, er der flere overflader, som kan reflektere lys, og du vil opfatte farven som hvid.

Eksempel fra atmosfærekemien på overfladearealets betydning følger snarest.
I det tidlige forår kan man være heldig at opleve at se en hugorm ligge på en solbeskinnet plet og suge varmen til sig, som du kan se i figur 57. Hugorme er et af mange vekselvarme dyr, hvis kropstemperatur styres af omgivelsernes temperatur. Hvis hugormen ikke bliver varmet tilstrækkeligt op, bevæger den sig meget langsomt. Dette skyldes, at de biokemiske reaktioner i dens krop forløber ved en lavere reaktionshastighed, når temperaturen er lavere. Det gælder for alle kemiske reaktioner: Når temperaturen stiger, øges reaktionshastigheden.

Men gælder det virkelig for alle kemiske reaktioner? Også dem vi selv kan lave i laboratoriet? I videoen nedenfor kan du se et simpelt forsøg, hvor et magnesiumbånd puttes i 0,1 M saltsyre ved to forskellige temperaturer.
Det, du netop har set i reagensglasset, gælder også i atmosfæren: Temperatur påvirker, hvor hurtigt kemiske reaktioner forløber – og dermed hvor længe drivhusgasser bliver i luften.
Methan er en af de problematiske drivhusgasser, men heldigvis bliver gassen nedbrudt i atmosfæren:
CH4(g) + 2 O2(g) → CO2(g) + H2O(g)
(19)
Begge produkter er også drivhusgasser, men som du har set tidligere, har drivhusgasser forskellig ’styrke’. Vands GWP-værdi er meget lav, mens methans GWP-værdi er 28. Dermed er methan umiddelbart mere skadelig end carbondioxid, så en skadelig drivhusgas nedbrydes til en mindre skadelig drivhusgas. Men helt så enkelt er det dog ikke, for carbondioxid har en markant længere levetid i atmosfæren end methan.
Reaktion (19) er den overordnede reaktion for methan i atmosfæren, men faktisk nedbrydes methan i flere trin, som tidligere vist i eksemplet på radikalreaktioner i atmosfæren:
HO∙(g) + CH4(g) → ∙CH3(g) + H2O(g)
(20)
Pga. en stigning i atmosfærens temperatur, ses nu en øgning af nedbrydning af methan i atmosfæren på ca. 3 % sammenlignet med for 100 år siden.
En højere temperatur betyder nemlig, at methanmolekylerne og hydroxylradikalerne bevæger sig hurtigere og oftere støder sammen med tilstrækkelig energi til at reagere, som du vil lære mere om, når kollisionsteorien gennemgås. Fordi molekylerne reagerer oftere, øges reaktionshastigheden for nedbrydningen af methan, og gassen fjernes hurtigere fra atmosfæren. Eksemplet viser tydeligt, hvordan temperaturen spiller en afgørende rolle for reaktionshastigheden i atmosfæren.
Men igen er det ikke helt enkelt, for der udledes også mere methan fra jordoverfladen pga. temperaturstigningen. Det skal du prøve at forholde dig til i denne opgave.
Du skal starte med at læse denne artikel fra Videnskab.dk: ’Methanudledningen stiger, og det er ikke kun køernes skyld’. Artiklen beskriver, hvordan mængden af methan i atmosfæren stiger, selvom methan samtidig nedbrydes hurtigere i et varmere klima.
1. Nævn mindst to forskellige kilder til methan, som artiklen peger på, og forklar kort, hvordan de hænger sammen med global opvarmning.
2. Artiklen forklarer, at temperaturstigninger både kan øge udledningen af methan og øge nedbrydningen af methan i atmosfæren. Forklar med dine egne ord:
a. Hvorfor udledes der mere methan, når temperaturen stiger?
b. Hvorfor nedbrydes methan samtidig hurtigere i et varmere klima?
3. Artiklen kan give indtryk af, at atmosfæren ”hjælper sig selv”, fordi methan nedbrydes hurtigere i et varmere klima. Diskutér, om dette er en tilstrækkelig løsning på klimaproblemet, eller om der er forhold, som gør situationen mere kompleks.
4. Methan har en kortere levetid i atmosfæren end CO₂, men en langt højere GWP-værdi. Forklar, hvorfor reaktionshastighed og levetid i atmosfæren er vigtige begreber, når man vurderer en drivhusgases betydning for klimaet.
Se mere
Reaktioner, hvor lys øger reaktionshastigheden, kaldes fotokemiske reaktioner. Et eksempel fra hverdagen er, når tandlægen bruger UV-lys til at hærde plastikfyldninger. UV-lyset har netop den energi, der skal til for at sætte gang i en kemisk reaktion, så plastikmaterialet hurtigt bliver hårdt og holdbart (se figur 58). Uden lyset ville reaktionen stadig ske, men meget langsomt.
Et lignende fænomen sker med ozonen, der dannes i den nedre del af atmosfæren kaldet troposfæren. I figur 59 kan du se jordens atmosfære inddelt i forskellige områder. Du kan kigge på reaktionerne (15-18) og figur 52 i afsnittet om koncentration for at få genopfrisket din viden herom.
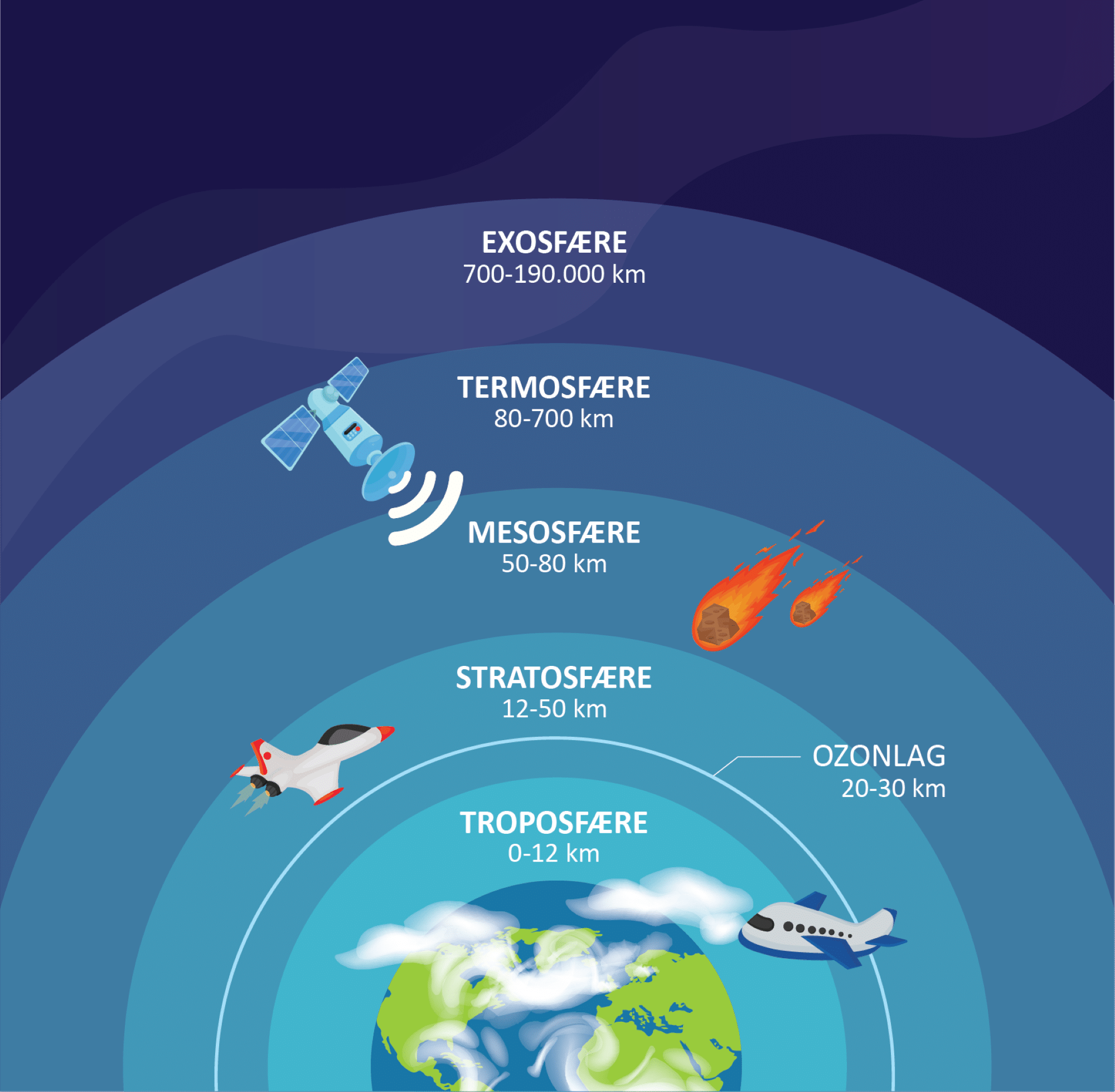
I reaktion (18) så du, at der blev dannet ozon, men den præcist modsatte reaktion er en fotokemisk reaktion, der igangsættes af UV-lys fra solen:
O3(g) → O2*(g) + O*(g)
(21)
Afhængigt af lysets bølgelængde er begge produkter exciterede, hvilket vil sige, at de har ekstra meget energi. Det exciterede oxygenatom kan reagere med et vandmolekyle og danne de meget vigtige hydroxylradikaler. Hvorfor de er så vigtige, kan du læse mere om i faktaboksen ’Den atmosfæriske støvsuger’.
Hydroxylradikalet
Hydroxylradikalet kaldes ofte atmosfærens støvsuger, fordi det konstant fanger og neutraliserer skadelige stoffer, som du kan se i figur 60. Radikalet reagerer med mange forskellige stoffer i atmosfæren, og dermed starter det deres nedbrydning. Selvom hydroxylradikalet selv er meget reaktivt og hurtigt forsvinder, bliver det hele tiden gendannet i atmosfæren gennem flere forskellige reaktioner.
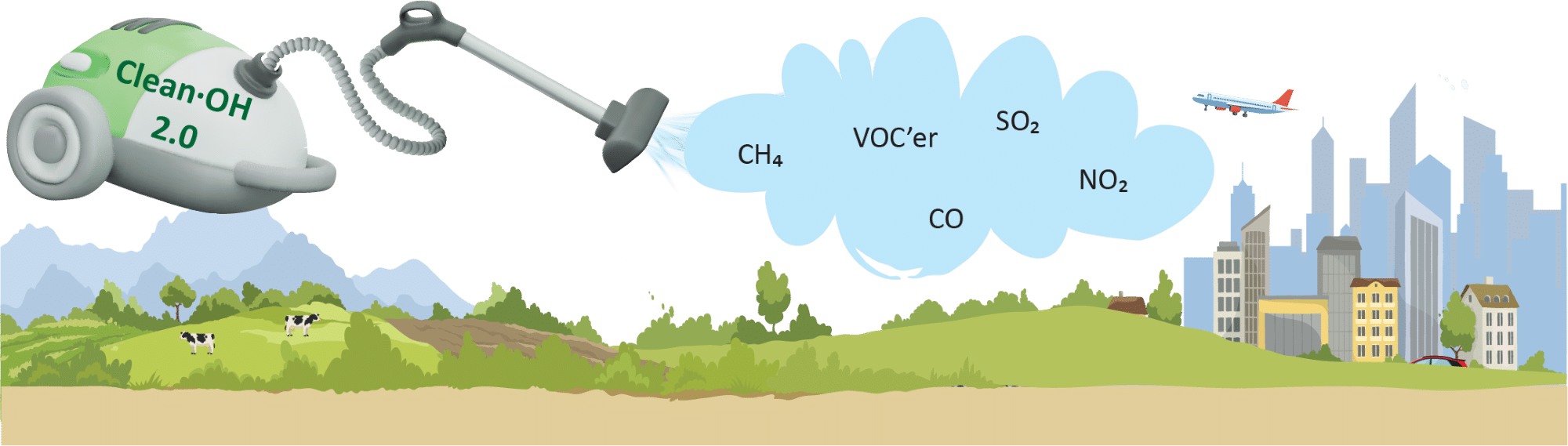
Desværre reagerer hydroxylradikalet ikke med de skadelige CFC-gasser, så de kan frit bevæge sig højere op i atmosfæren og nedbryde ozonlaget. Til gengæld fjerner radikalet mange af de luftforurenende stoffer i troposfæren.
Hydroxylradikalet er meget reaktivt, hvilket skyldes den uparrede elektron. Det er let at forveksle hydroxylradikalet med hydroxidionen, som du kender fra baser som natriumhydroxid. I figur 61 kan du se forskellen på de to. Det er pga. en uparrede elektron i radikalet, at det er så reaktivt.
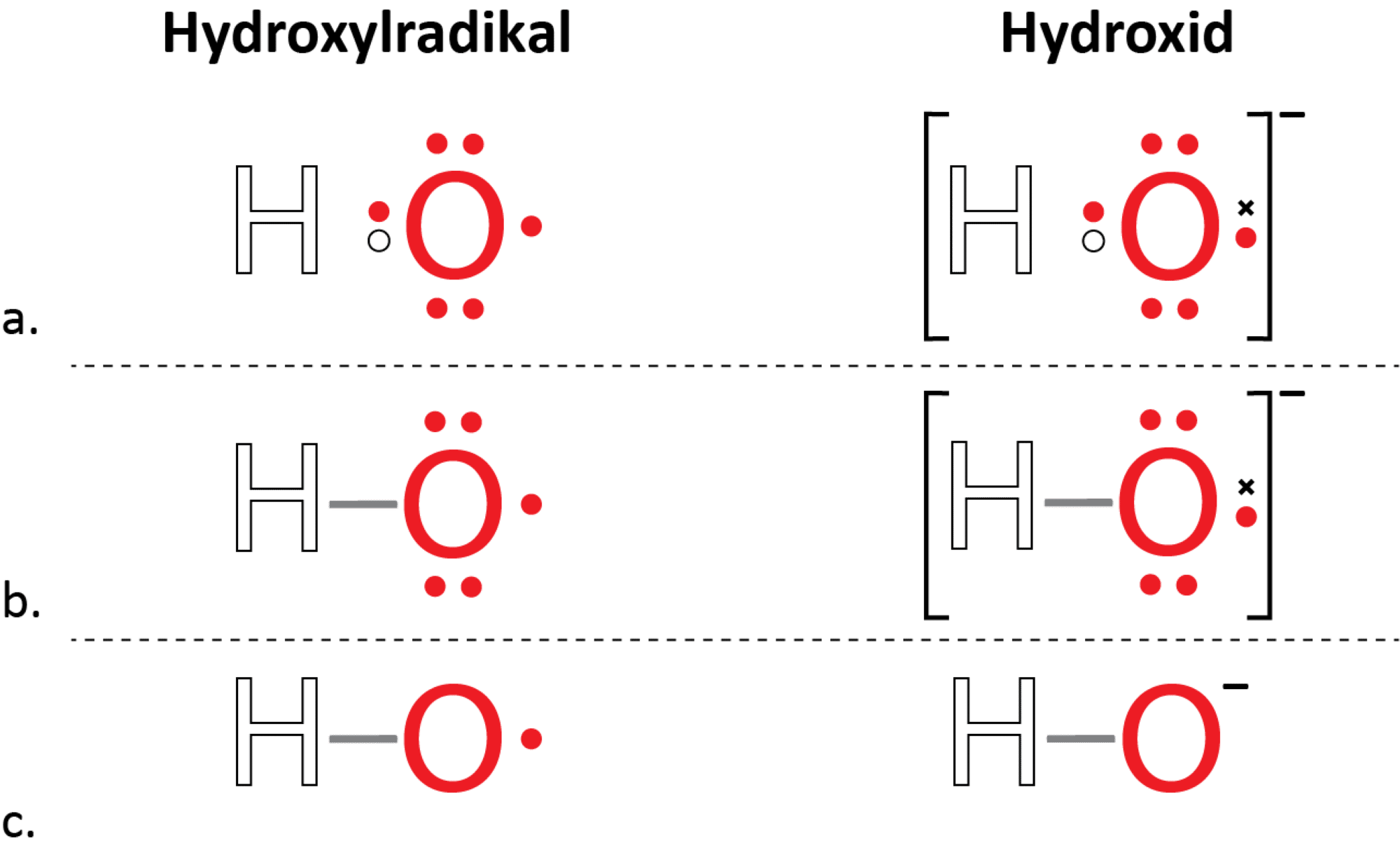
Hydroxylradikalet spiller en helt central rolle i reguleringen af atmosfærens sammensætning og dermed for luftkvalitet, ozonlag og klimaforandringer. Radikalet dannes højt i atmosfæren, hvor sollys spalter ozonmolekyler, som vist i reaktion (21). Når ozon rammes af UV-stråling, nedbrydes det til dioxygen og et frit oxygenatom. Dette oxygenatom reagerer derefter med luftens vanddamp og danner to hydroxylradikaler:
| O(g) + H2O(g) → 2 HO∙(g) | (22) |
Hydroxylradikalet kan også dannes gennem fotokemiske reaktioner med nitrogenoxider og andre stoffer. Når radikalet først er dannet, reagerer det med mange drivhus- og forureningsgasser, især methan, som er den næstvigtigste drivhusgas efter carbondioxid. Reaktionen mellem hydroxylradikalet og methan danner gennem en række reaktioner blandt andet vand og kuldioxid, som du så i afsnittet ’Temperatur’. Både carbondioxid og vand har begge en langt svagere opvarmningseffekt end methan (de har en lavere GWP-værdi, som du kan læse om i afsnittet ’Hvorfor absorberer drivhusgasserne varmestråling?’). Faktisk står hydroxylradikalet for at fjerne omkring 85 % af den methan, der hvert år frigives til atmosfæren, og uden det ville koncentrationen af drivhusgasser hurtigt stige.
Koncentrationen af hydroxylradikalet i atmosfæren er dog ikke konstant. Den påvirkes af sollys, luftfugtighed og udledninger af andre gasser som nitrogenoxider. Det viser, hvor følsomt samspillet mellem atmosfærens gasser er, og hvor vigtig hydroxylradikalet er for atmosfærens naturlige evne til at holde sig selv ren og i balance.
Se mere
Hydroxylradikalet dannes i atmosfæren netop som følge af fotokemiske reaktioner, hvor solens stråling leverer den energi, der skal til for at sætte kemiske processer i gang. Uden lys ville mange af de reaktioner, der styrer atmosfærens sammensætning og drivhusgassers levetid, forløbe meget langsomt eller slet ikke finde sted.
Lys kan altså fungere som en afgørende faktor for reaktionshastigheden, fordi det kan tilføre energi direkte til molekyler og skabe meget reaktive partikler som radikaler.
En katalysator er et stof, der øger reaktionshastigheden for en kemisk reaktion uden selv at blive forbrugt. En katalysator ændrer reaktionsvejen ved at sænke aktiveringsenergien, som er den mindste energi, der kræves for, at reaktanterne kan omdannes til produkter (se figur 62). Den danner ofte midlertidige bindinger med reaktanterne og hjælper dermed med at bryde eksisterende bindinger og danne nye bindinger lettere. Når reaktionen er slut, frigives katalysatoren igen, og den er klar til at katalysere en ny reaktion.
Forestil dig din skolevej til gymnasiet. Højdeforskellen (højde over havets overflade) mellem dit hjem og gymnasiet er den samme uanset hvad du gør, men der findes fx forskellige måder at komme frem. På samme måde som med katalysatoren i en kemisk reaktion, kan din cykel sørge for, du lettere kommer til skole, så du måske kan sove lidt længere og stadig kommer frem i tide.
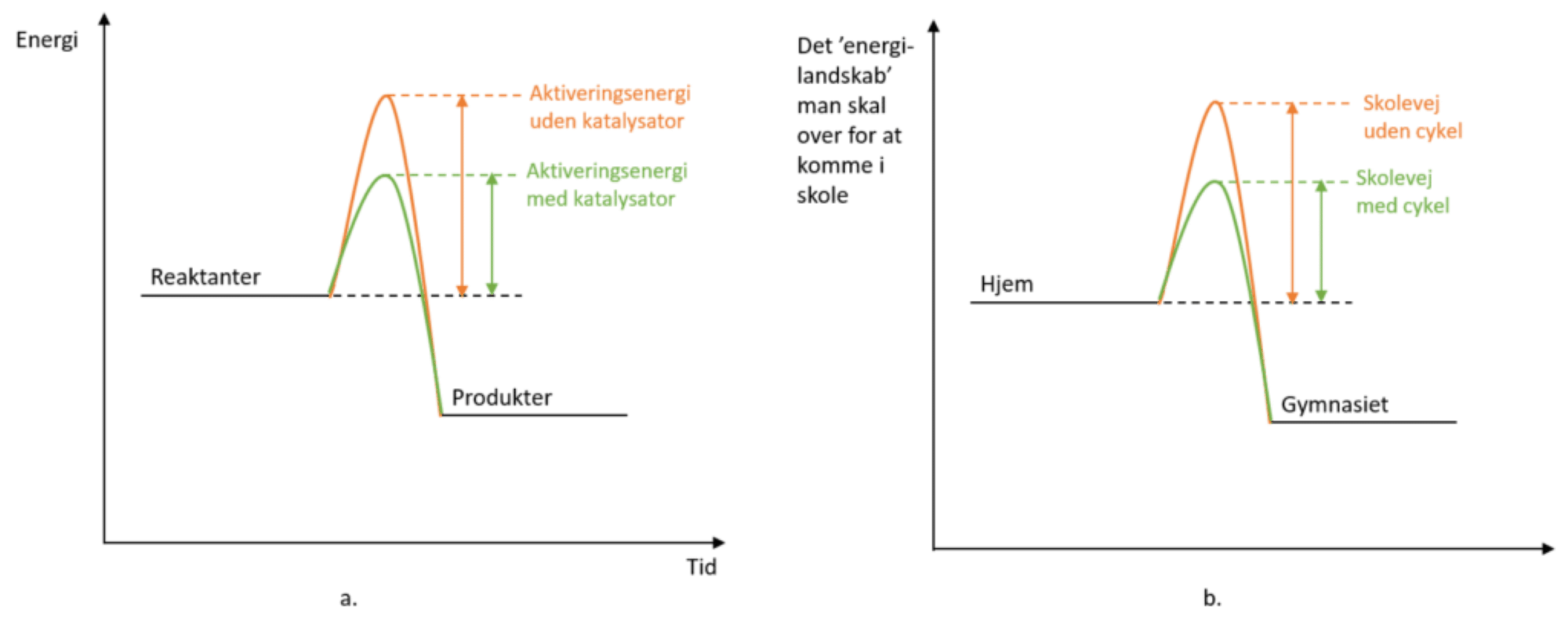
Du kan læse mere om aktiveringsenergi under afsnittet om kollisionsteorien, og er du interesseret i at forstå flere detaljer omkring katalysatorer, kan du læse om det i temaet ’Power-to-X og katalyse’. Men først skal du se et skræmmende eksempel på en katalyseret reaktion i atmosfæren. Frie chloratomer dannes i atmosfæren fra nedbrydning af CFC-gasser, der spaltes, når de udsættes for UV-lys. De frie chloratomer har 7 elektroner i yderste skal og derfor en uparret elektron, og de er derfor radikaler og meget reaktive. I reaktion (23) nedbrydes CFC-12, når solens stråler rammer molekylet:
CF2Cl2(g) → CF2Cl∙(g) + Cl∙(g)
(23)
Herefter følger en række reaktioner, hvor de frie chloratomer fungerer som katalysatorer for nedbrydningen af ozon til dioxygen. Chloratomerne bruges og gendannes igennem en kæderække af reaktioner (24a-24d):
Cl∙(g) + O3(g) → ClO∙(g) + O2(g)
(24a)
Chlormonoxidradikalet reagerer videre med et andet chlormonoxidradikal:
2 ClO∙(g) → ClO-OCl(g)
(24b)
Chlorperoxid nedbrydes herefter videre:
ClO-OCl(g) → ClO-O∙(g) + Cl∙(g)
(24c)
Chlordioxidradikalet frigiver dioxygen og et chloratom:
ClO-O∙(g) → O2(g) + Cl∙(g)
(24d)
Et enkelt chloratom nedbryde tusindvis af ozonmolekyler, fordi det indgår i en kæde af reaktioner (24a-24d). Det bliver altså ikke opbrugt, men genbruges. Denne proces var en væsentlig årsag til dannelsen af ozonhullet over Antarktis.
Der er fest på dit gymnasium. Forestil dig følgende to situationer:
Situation 1 – én lærer ved indgangen
Situation 2 – flere lærere ved indgangen
Refleksion
1. Hvilken situation vil samlet set tage kortest tid? Forklar hvorfor.
2. Du kan drage en parallel til en kemisk reaktion. Overvej hvad følgende svarer til i en kemisk sammenhæng:
a. Eleverne i kø
b. Eleverne til fest
c. Lærerne med stemplerne
d. Tiden, det tager at få alle ind
3. Hvilken ’kemisk’ reaktion er det, der sker?
4. Hvordan kan forskellen mellem de to situationer forklares ud fra begreberne reaktionshastighed og katalyse?
Se mere
Hvis der i opgave 26 kommer flere elever, men der stadig kun er én lærer, vil køen vokse. Hastigheden bestemmes stadig af, hvor hurtigt læreren kan stemple. I en kemisk reaktion svarer det til, at katalysatoren bliver den begrænsende faktor. Reaktionen kan ikke gå hurtigere, selvom der er flere reaktanter.
Reaktionshastighed handler ikke kun om, hvor meget der reagerer, men også om hvordan reaktionerne forløber på molekylært niveau. Katalysatorer som chloratomerne i ozonnedbrydningen ændrer nemlig selve reaktionsvejen, så flere reaktioner kan finde sted på kortere tid, uden at katalysatoren selv bliver opbrugt.
For at forstå, hvorfor faktorer som koncentration, temperatur, overfladeareal, lys og katalysatorer påvirker reaktionshastigheden, kan du i næste afsnit zoome helt ind på, hvad der sker, når molekyler og atomer støder sammen. Her bliver du introduceret til kollisionsteorien, der giver en fælles forklaring på alle de faktorer, du netop har arbejdet med, og du får også en uddybning af begrebet aktiveringsenergi og hvorfor kun nogle kollisioner fører til en kemisk reaktion.
Når du ser på en kemisk reaktion, kan det være fristende at tænke, at reaktanterne bare reagerer, når de blandes. Men i virkeligheden sker der kun en reaktion, når molekylerne støder sammen. Reaktionshastigheden afhænger derfor af, hvor ofte molekylerne kolliderer, og hvad der sker i selve kollisionen.
I kollisionsteorien zoomer du ind på disse sammenstød mellem molekyler og ser på, hvilke betingelser der skal være opfyldt, for at en kollision fører til en kemisk reaktion. Teorien giver dig et fælles udgangspunkt for at forstå, hvorfor nogle reaktioner går hurtigt, mens andre går langsomt.
Du kan nok godt forestille dig, at hvis to biler støder sammen ved lav hastighed, sker der ikke nødvendigvis særlig meget. Måske får de bare en lille bule, og bilerne kan køre videre. Men hvis de rammer hinanden med høj fart og rammer de rigtige steder kan sammenstødet føre til store forandringer af bilerne.
På samme måde gælder det for kemiske reaktioner: Når atomer og molekyler støder sammen, er det ikke alle kollisioner, der fører til en reaktion. For at der kan ske en kemisk reaktion, skal de kollidere med tilstrækkelig energi og i den rette orientering. Det er netop disse betingelser, kollisionsteorien beskriver.
Fortsættelse følger…
Der er 3 forsøg til temaet:
Find dem under fanen Eksperimentelt