Plastik, eller plast, som vi kalder det i kemi, er en del af vores liv og hverdag. Lige fra vi er helt små.

1. Hvad er plast?
Plast er et syntetisk materiale, altså kunstigt fremstillet gennem kemiske processer. Plast er formbart ved opvarmning og består af det, der hedder en polymer. Al plast tilsættes additiver (tilsætningsstoffer) i produktionen, derfor inkluderer man ofte additiver i definitionen af plast.
Plast = polymer + additiver
Hvilke additiver, der tilsættes, afhænger af, hvad man skal bruge plasten til: fx UV-absorbere (fx i tøj), blødgørere (fx i PVC-plast), brandhæmmere (fx i elektronik udstyr) eller farvestoffer.
Se You Tube klippet nedenfor (4:25 min), der kort forklarer, hvad plast er, hvorfor vi bruger så meget plast, og nogle af de ulemper, der er forbundet med plast.
Der er plast næsten alle de steder, hvor vi kigger efter det, også i naturen i form af plastaffald. Og det har store omkostninger, fx når en kaskelothval skyller på land i Nordjylland (februar 2026 Ålbæk strand), fordi den døde af at have spist omkring 12 kg fiskenet. For plast nedbrydes ikke lige i naturen. Heller ikke mikroplast, som er små plaststykker, under 5 mm. Mikroplast er typisk dannet fra mekanisk nedbrydning af plasten. Herhjemme stammer det meste mikroplast fra bildæk.
Også vindmøllevinger og tandfyldninger består af plast, nærmere betegnet epoxyplast, der er meget svært nedbrydelig, når de efter årtiers brug skal udskiftes. Derfor ender vindmøllevinger ofte deres dage med at blive gravet ned, i stedet for at blive genbrugt i nye vindmøllevinger. Det kaldes affaldsdeponi, og er nederst i affaldstrekanten. Hvis ikke der findes en løsning på genbrug af vindmøllervinger, vil vi globalt have ophobet mindst 43 millioner tons vindmøllevingeaffald i 2050! Men der er løsninger på vej, som beskrevet her.
Opgave 1 Hvor er der plast?
Kig dig omkring, hvor du sidder lige nu. Hvad kan du få øje på af plastik?
Se mere
vi i Danmark forbruger omkring 200 kg plast pr. person om året. Og det er næsten dobbelt så meget som resten af landene i EU. Kun ca. 5% af plasten i Danmark bliver genanvendt.
Det store plastikforbrug er forbundet med en række miljøpåvirkninger, udledning af store mængder CO2, og brug af ressourcer, der ikke kan fornys. Kort sagt et stort aftryk på klima og miljø.
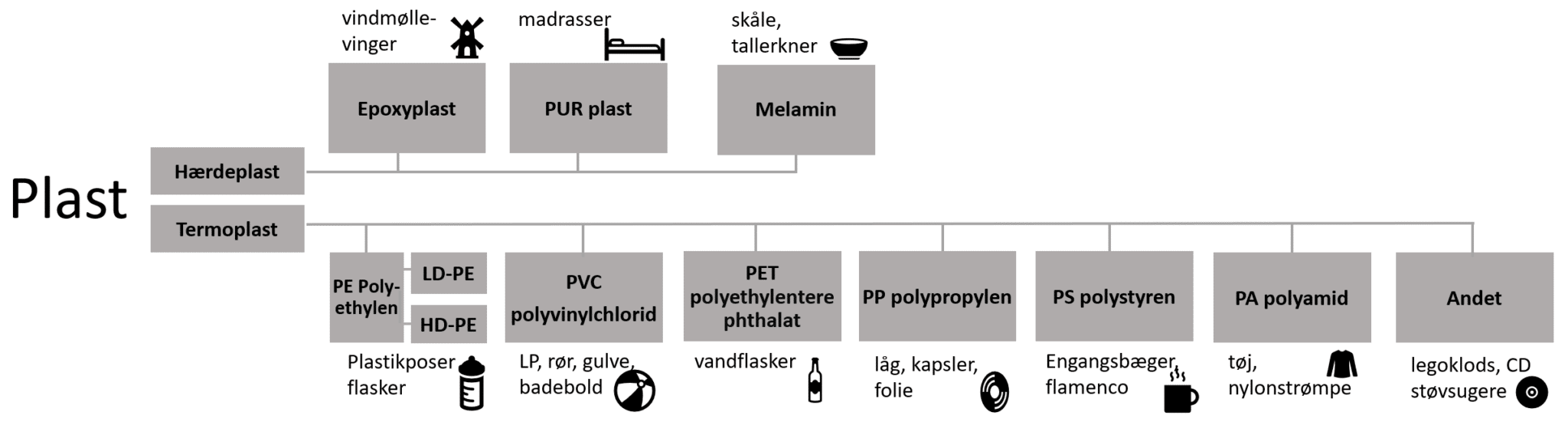
Plast dækker op mod 3000 forskellige plasttyper. Tænk på at så forskellige ting som fleecetrøjer, LEGO, vinyler, madrasser og vindmøllevinger alle er plast, som illustreret i figur 2.

Plast består generelt af grundstofferne carbon og hydrogen. Derfor hører temaet plast til i den organiske kemi, der netop omhandler kemiske forbindelser med bl.a. carbon og hydrogen. Udover carbon og hydrogen indgår forskellige grundstoffer i forskellige typer af plast:
Med afsæt i ovenstående kan vi lave et ”plastens periodiske system”, som vist i figur 3.
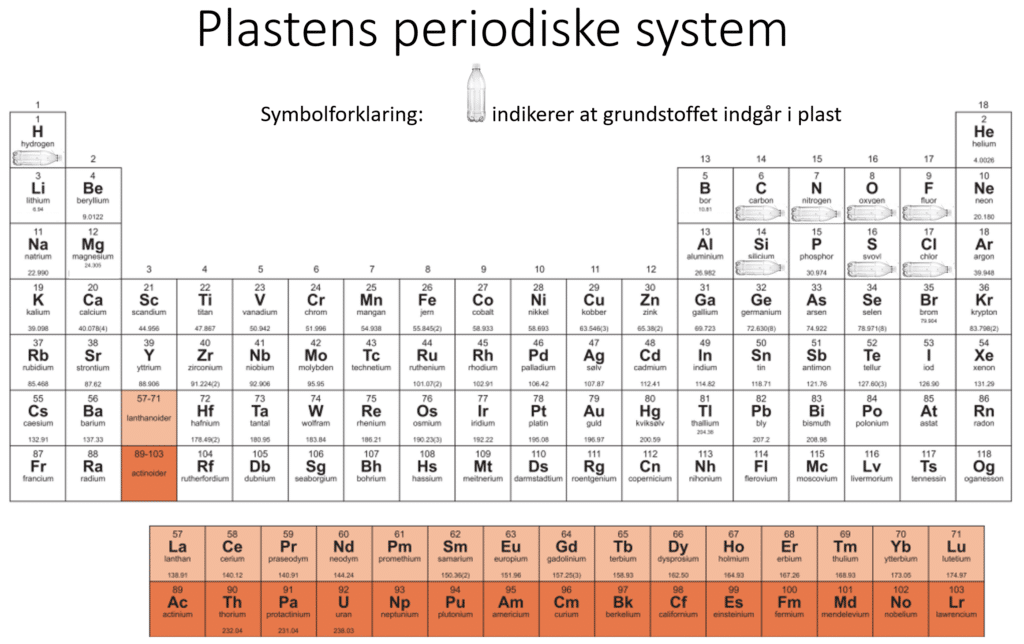
Opgave 2: Grundstoffernes periodiske system og plast
Hvad kendetegner de grundstoffer der indgår i plast? Altså hvad har de tilfælles ift. deres placering i det periodiske system?
Se mere
Selvom der er omkring 8 forskellige grundstoffer, der kan indgå i plast, skyldes de fleste forskellige egenskaber og funktioner af plast, at stofferne har forskellige strukturer.

De bestanddele, der opbygger plast kommer fra råolie, som er en fossil ressource. I faktaboksen Råolie – plastens byggesten kommer du med ind i plastens sorte historie
Kul, olie og gas er fossile ressourcer, og de er hverken fornybare eller vedvarende. Gas henviser til det vi kalder naturgas. Naturgas lyder meget naturligt, men det er vigtigt at forstå, at det er en fossil gas, der ligesom kul og olie er dannet i undergrunden over millioner af år.
Figur 4 illustrerer den geologiske proces, hvor olie, gas og kul dannes.
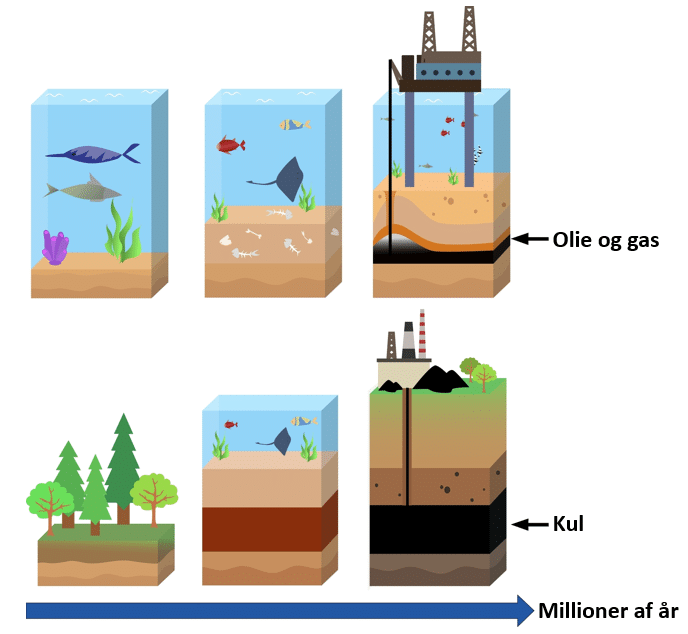
Geologiske processer har under høj temperatur og tryk omdannet det organiske materiale, der stammer fra aflejringer af døde dyr og planter, til kul, olie og gas. Se også You Tube klippet (1:30 min.), der kort forklarer processen.
Råolie, er den ubehandlede olie, som udvindes fra undergrunden. Plastens byggesten kommer fra råolie, faktisk anvendes omkring 6% af råolien til plast. Råolie består af forskellige organiske stoffer med lidt forskellig opbygning. Nogle af forbindelserne indeholder andre også andre grundstoffer end carbon og hydrogen. Det er illustreret i figur 5.
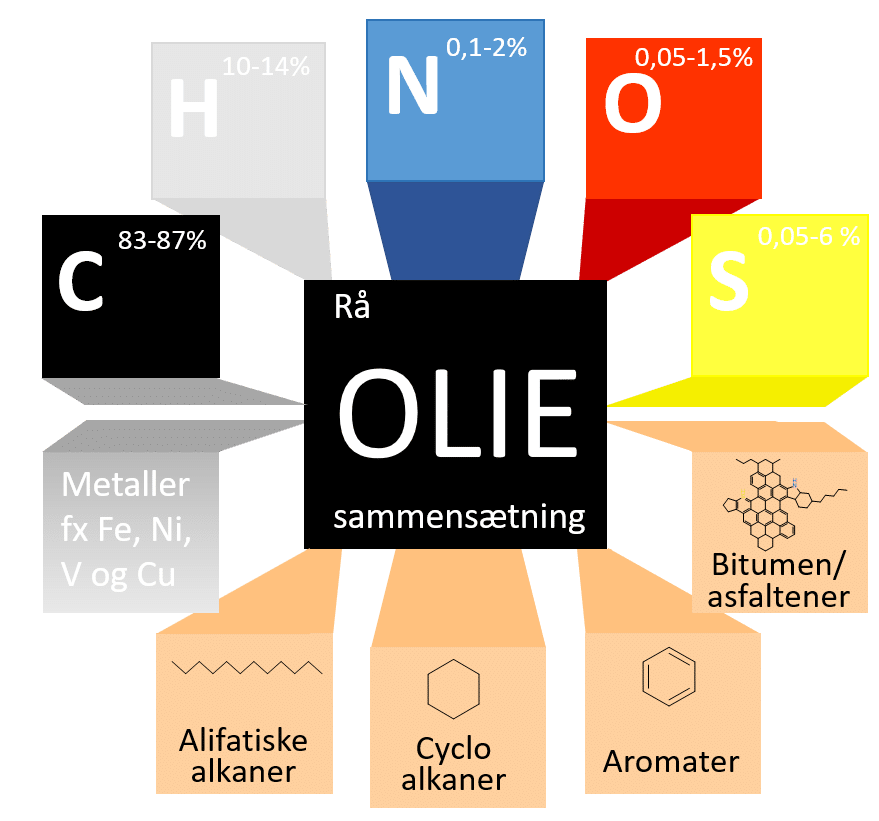
Råolien består primært af carbonhydrider (en kemisk forbindelse, der kun indeholder C og H), herunder såkaldte alifatiske alkaner, cycloalkaner, og aromatiske forbindelser – disse stoffer forklares i næste afsnit. Råolie indeholder også nogle meget store og tunge carbonhydrider, der kaldes bitumen eller asfaltener, som er tjærelignende stoffer der bruger til … ja asfalt. Råolie indeholder ud over carbon og hydrogen også lidt svovl, nitrogen og oxygen, samt spor af metaller. Den specifikke sammensætning af råolien bestemmes af, hvor olien er dannet og under hvilke forhold.
Produkter baseret på råolie kaldes petrokemiske stoffer. Petrokemi er den gren af kemien, der netop beskæftiger sig med at danne kemikalier og produkter som fx plast fra råolie. Men råolie bruges ikke som den er. Den behandles på raffinaderier, hvor den afsaltes og senere opvarmes og adskilles i forskellige fraktioner. Det er i fokus i faktaboksen Fra råolie til plast.
Se mere
De simpleste organiske stoffer er carbonhydriderne. Carbonhydrider er et navn for de kemiske forbindelser, der kun indeholder carbon og hydrogen. De omtales ind imellem som kulbrinter. Kan du forstå hvorfor? Carbonhydriderne er petrokemiske stoffer, da de kommer fra kul, olie eller gas, omtalt i faktaboksen ovenfor. Carbonhydrider er byggesten for plast, så når vi skal lære og forstå opbygningen af plast, og hvorfor det er et fantastisk materiale – med en sort bagside, må vi starte med carbonhydriderne.
Først ser vi på de carbonhydrider, der udelukkende indeholder enkeltbindinger mellem carbonatomerne. Den gruppe kalder vi alkaner.
Alkaner er ikke særlig reaktive. De er ikke syrer eller baser og indeholder ingen funktionelle grupper (du ved, modsat fx alkoholer, der indeholder en ”alkoholgruppe” ). Alkaner anvendes primært som brændstoffer, fordi de kan brænde, som vist i reaktion 1) nedenfor. Her er vist en fuldstændig forbrænding af heptan, der indgår i benzin. Som reaktion 1) viser, danner forbrændingen carbondioxid, som er en drivhusgas. Reaktionen er exoterm – dvs. den udvikler energi (varme).
C7H16 (l) + 11 O2 (g) → 7 CO2 (g) + 8 H2O (l)
(1)
Alkaner er upolære og hydrofobe, dvs. de vil ikke blandes med vand, men flyder ovenpå vand, da de også har en lavere densitet (massefylde) end vand. Ligesom olie. Alkaner er netop hovedbestanddelen af råolie. De andre carbonhydrider forekommer kun i små mængder i råolien. Da alkaner er byggesten for plast, er de lidt mere i fokus her.
Den simpleste alkan, og for øvrigt det simpleste organiske stof overhovedet, er methan. Figur 6 viser forskellige repræsentationer af methan.
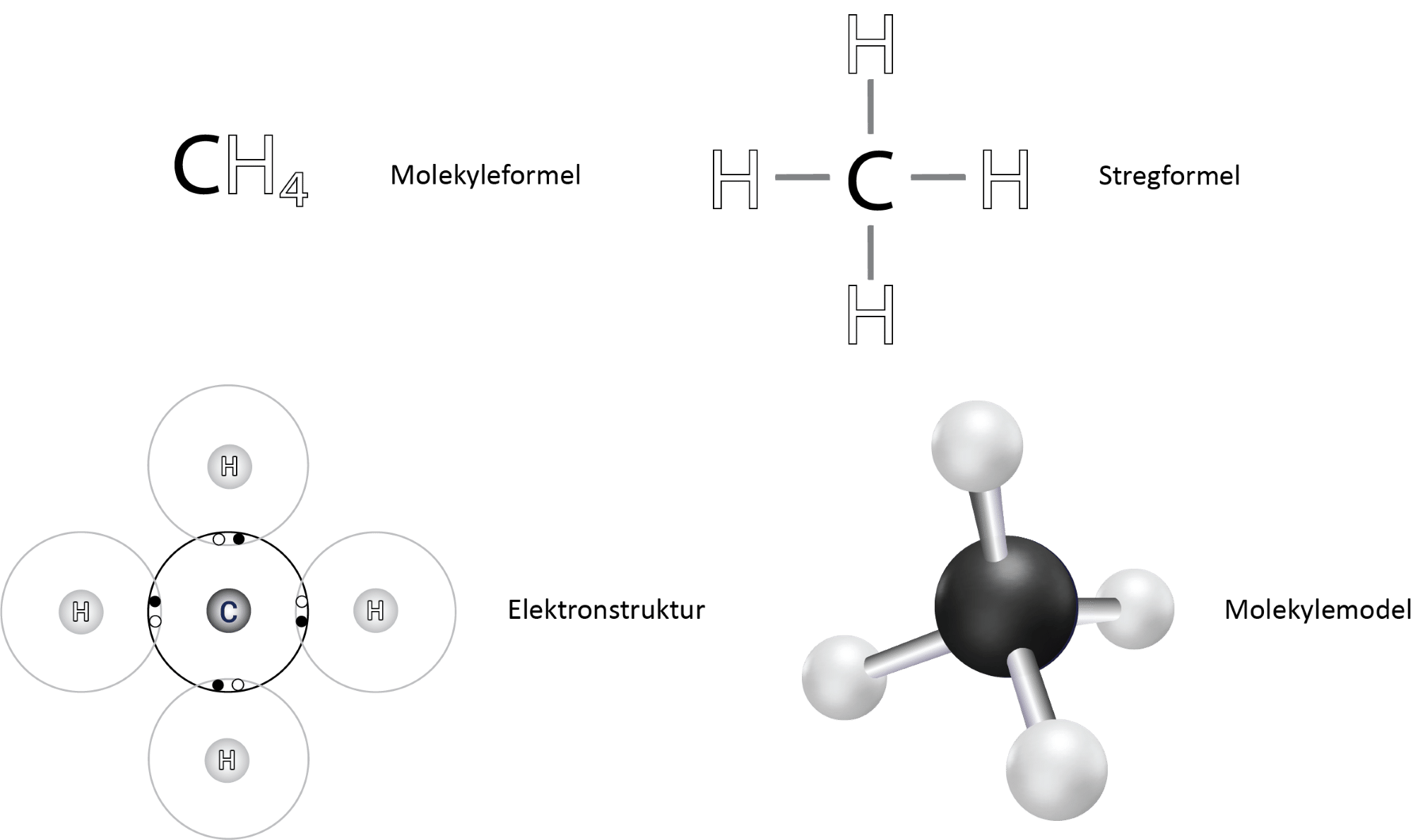
Methan er, ligesom de andre små alkaner, en gas. Methan kommer fra naturgas og udgør hovedbestanddelen af naturgas. Methan kommer også andre steder fra, fx fra køers ”prutter”.
Den næstsimpleste alkan er ethan.
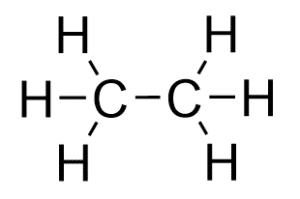
Som du kan se på figur 7 har ethan et carbonatom mere end methan. Alkaner er netop kendetegnede ved, at der mellem de enkelte carbonatomer er en enkel elektronparbinding, som det fremgår at strukturen af ethan, vist i figur 7. Ethan kommer fra naturgas, ligesom methan. Ethan kan indgå i en proces, der hedder cracking (det forklares i faktaboksen ”Fra råolie til plast”) og omdannes til ethen. Ethen minder om ethan, men med en dobbeltbinding mellem de 2 carbonatomer, det forklares nedenfor. Ethen er den primære byggesten i den plasttype, der hedder PE-plast.
Vi kunne fortsætte rækken af alkaner. Næste forbindelse er så propan med formlen C3H8. Det er illustreret i oversigten i figur 8.
Som figur 8 også viser, kan sumformlen (det samme som formlen, bruttoformel eller kemisk formel) opskrives CnH2n+2 . Ser vi på ethan i figur 7 passer det med at der er 2 carbonatomer og dermed 6 hydrogen atomer. Alkanernes navne, formler, oprindelse og anvendelse, er indsat i figur 8. Alkaner og de andre organiske molekyler bliver let uoverskuelige at opskrive i takt med, at de bliver større. Derfor har man indført ”zigzag formler”, som er mere overskuelige, de er også vist i figur 8.
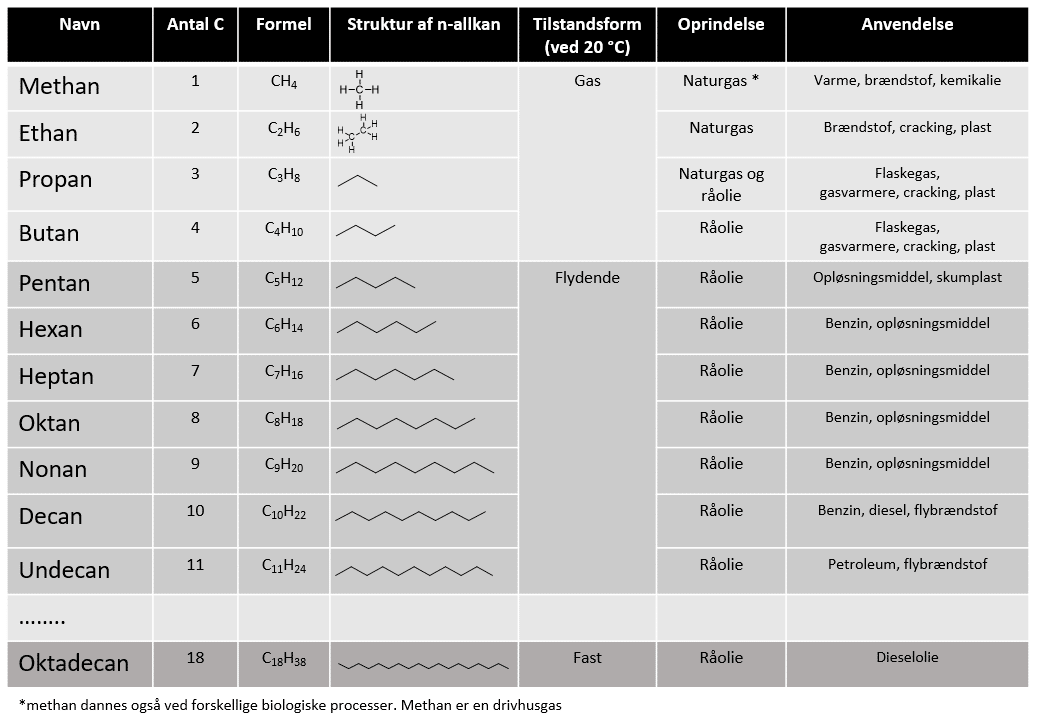
Alkanen decan kan opskrives med en zigzag-formel, hvor man kun tegner elektronparbindingerne mellem carbonatomerne. Hvert knæk i kæden angiver et carbonatom, mens hydrogen atomerne ikke er vist, de er underforståede (implicitte), som vist nederst i figur 9.
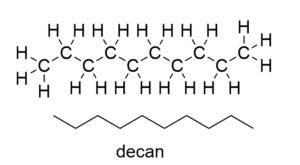
Navngivningen i den organiske kemi tager afsæt i navngivningen af alkaner, så det er vigtigt at lære alkanernes navne.
Opgave 3 Kast og træn alkaners navne
Gå 4 og 4 sammen (3&3 eller 5&5 kan også gå). I skal bruge en ærtepose eller en bold til at kaste med.
Stil jer i en rundkreds.
a. I kaster ærteposen til hinanden på skift, mens I skiftes til at sige alkanernes navne fra 1. Altså person 1 starter med at sige methan, og kaster posen videre til person 2 der siger ethan, sådan fortsætter I med at kaste frem og tilbage og navngive indtil I når til decan. Hvis I kan alle navnene går i videre til opgave b, ellers tager i et par ture mere.
b. Nu siger den der kaster et navn på en alkan, så skal personen der griber sige antallet at C-atomer. Altså hvis person 1 starter med at sige heptan kaster til person 2, der griber posen og siger 7. Og så kaster han/hun posen videre og siger et nyt navn.
Se mere
Alkanerne kan enten være opbygget som lange uforgrenede kæder (så kalder vi det n-alkan, for ’normal alkan). Men alkaner kan også have forgreninger i form af sidekæder.
Las os se på et par eksempler.
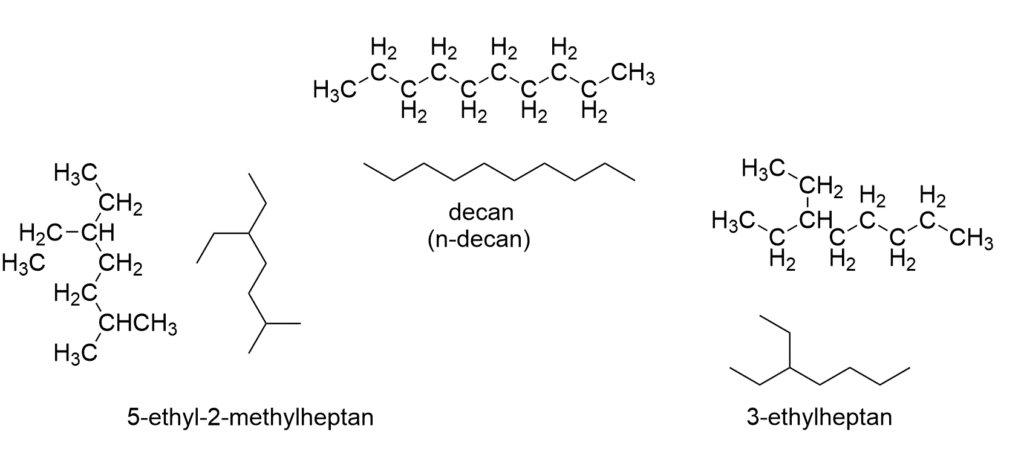
Forskellige stoffer med samme sumformel kaldes isomere stoffer. Figur 10 viser 3 forskellige isomerer af decan. Øverst i figur 10 er vist n-decan, altså en uforgrenet alkan. Til venstre i figur 10 er vist en alkanen vi navngiver 5-ethyl-2 methylheptan, mens isomeren til højre viser en forgrenet decan, som vi navngiver 3-ethylheptan.
Opgave 4 Isomere forbindelser af decan
Se mere
Der er flere hjemmesider, hvor man kan træne organisk kemisk navngivning, fx her eller her (Sidste link forudsætter at din lærer har koden fra LMFK ).
Du kan se hvor alkanerne stammer fra, og hvad de anvendes til i figuren 8. Fælles for alkanerne er altså, at de er fossile brændstoffer og stammer fra olie og naturgas. I faktaboksen Fra råolie til plast præsenteres, hvordan alkanerne isoleres fra olie og naturgas ved destillation og evt. cracking.

Råolie er en kompleks blanding af organiske forbindelser, primært alkaner, dannet i undergrunden gennem millioner af år. Før råolien kan bruges industrielt, behandles og adskilles den i sine bestanddele.
Afsaltning
Først afsaltes råolien. Her fjernes vand og salte. Afsaltningen sker typisk ved at blande råolien med ferskvand, ryste blandingen og lade saltet gå i opløsning i vandet, hvorefter vandfasen fjernes.
Fraktioneret destillation
Herefter sendes den rensede råolie til destillation, hvor råolien opdeles i forskellige bestanddele (fraktioner). Det kaldes fraktioneret destillation, og er centralt i raffinering. Se You Tube klippet nedenfor (4:05 min), der forklarer, hvordan råolie adskilles ved fraktioneret destillation.
Ved destillation udnyttes at alkanerne har forskellige kogepunkter. Der er en simpel sammenhæng mellem alkanernes længde og opbygning og deres kogepunkt. Jo længere kæde og dermed højere molarmasse, jo højere kogepunkt. Jo mere forgrenet kæden er, jo lavere kogepunkt. Det gælder generelt at:
Som du sikkert ved, er det elektronparbindinger, der holder atomer sammen til molekyler. Men det er ikke sikkert, at du har lært, at det er såkaldte intermolekylære kræfter, der holder molekyler sammen til stoffer. Jo stærkere intermolekylære kræfter, der virker mellem molekylerne, jo højere kogepunkter.
Det er illustreret i figur 11.
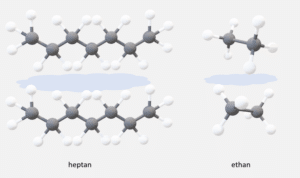
Fraktioneret destillation er illustreret i figur 12.
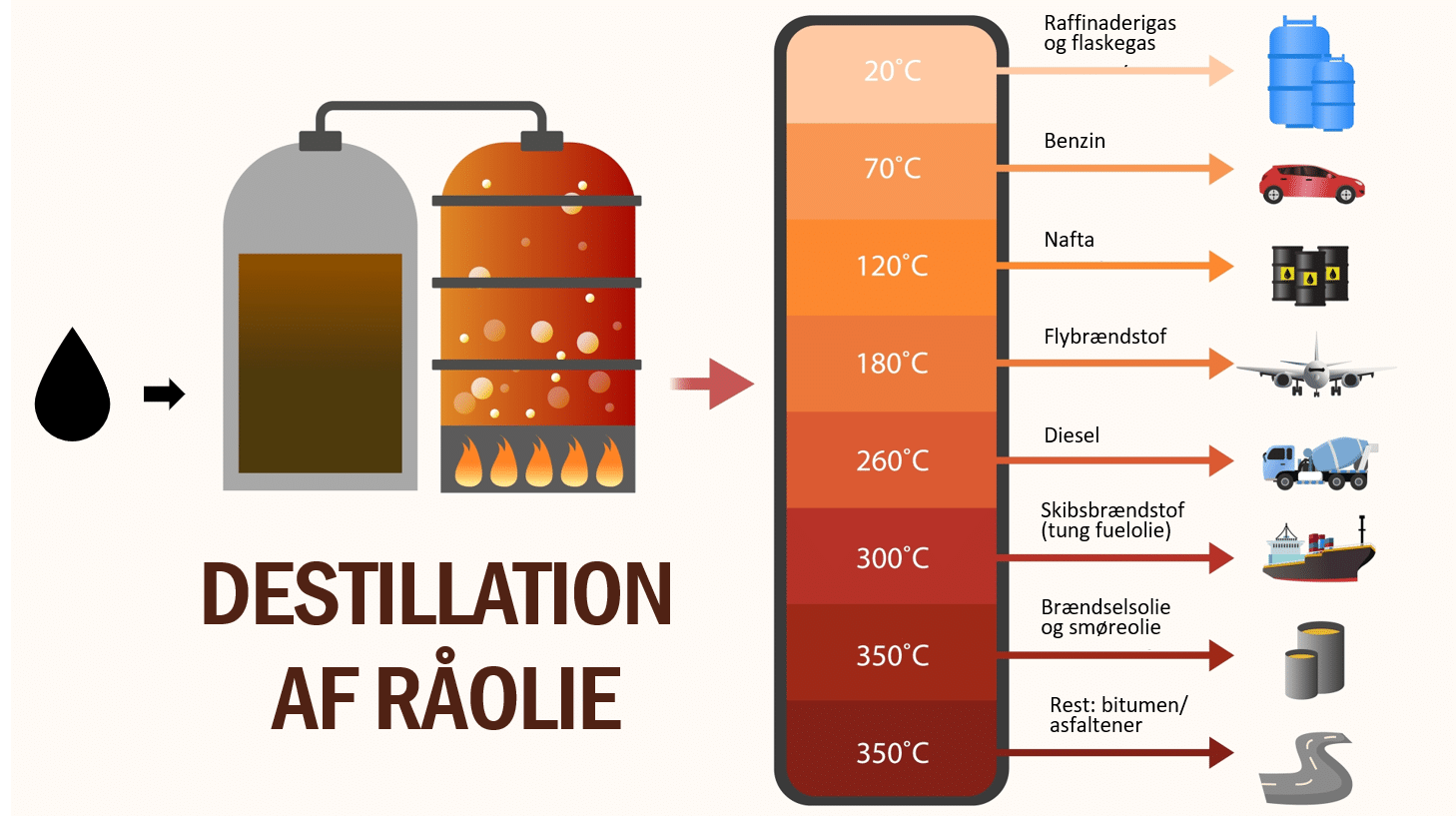
I et destillationstårn opvarmes råolien, så de fleste af stofferne kommer på gasform. Stoffer med høje kogepunkter, skilles fra først (nederst i destillationstårnet, hvor temperaturen er højest), mens de andre gasser ledes op gennem tårnet og afkøles undervejs. Når gasserne når til en temperatur, der er lavere end deres kogepunkt, fortættes gasserne til væske. Op gennem destillationstårnet fortætter de fleste af gasserne til væsker ved forskellige temperaturer, alt efter deres kogepunkter. Sådan opdeles råolie i forskellige fraktioner. Disse fraktioner anvendes til ret forskellige formål, fx som brændstof, olie til opvarmning, flybrændstof og nafta til kemikalier. Nafta, som er en vigtig råvare til plastproduktion, er en blanding af carbonhydrider med omkring 5-12 carbonatomer.
Cracking (krakning)
Det er ofte de mindre carbonhydrider (med korte carbonkæder) vi har brug for til brændstof og plastproduktion. For at danne kemikalier som ethen (ethylen) og propen (propylen) til plast, skal nafta gennem en proces kaldet cracking. Ved ’steamcracking’ opvarmes nafta til meget høje temperaturer (typisk 800–900 °C) i nærvær af vanddamp og katalysator, så de lange carbonkæder i nafta ’knækkes’ eller crackes, som det hedder til kortere kæder. Her dannes især alkaner og alkener, hvor alkenerne er de vigtige, fordi de fungerer som kemikalier (byggeklodser/monomerer), når vi skal have dannet plast. De dannede alkaner udnyttes til fx brændstoffer. Princippet i cracking er vist i figur 13.
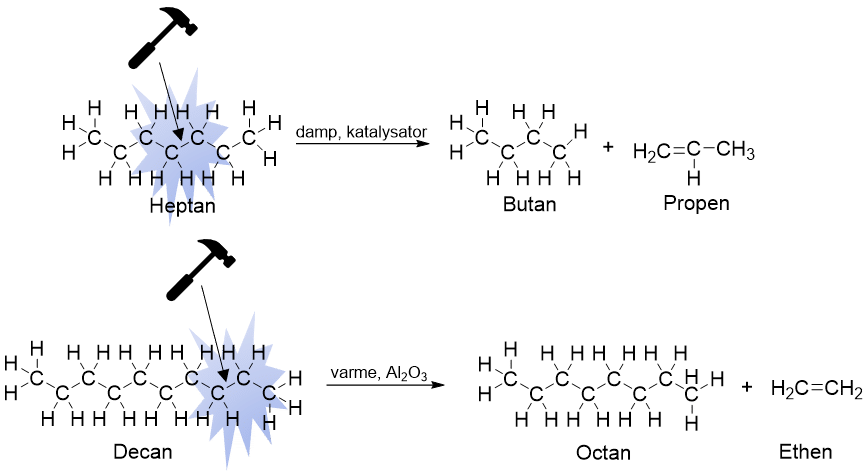
Fra cracking får man de kemikalier (byggesten), som kan indgå i produktionen af plast. Disse byggesten (monomerer) sættes sammen (polymeriseres) hvorved vi får dannet plast (en polymer). Polymerisering, monomerer og polymerer forklares nedenfor.
Hele processen fra råolie til plast er illustreret i figur 14.
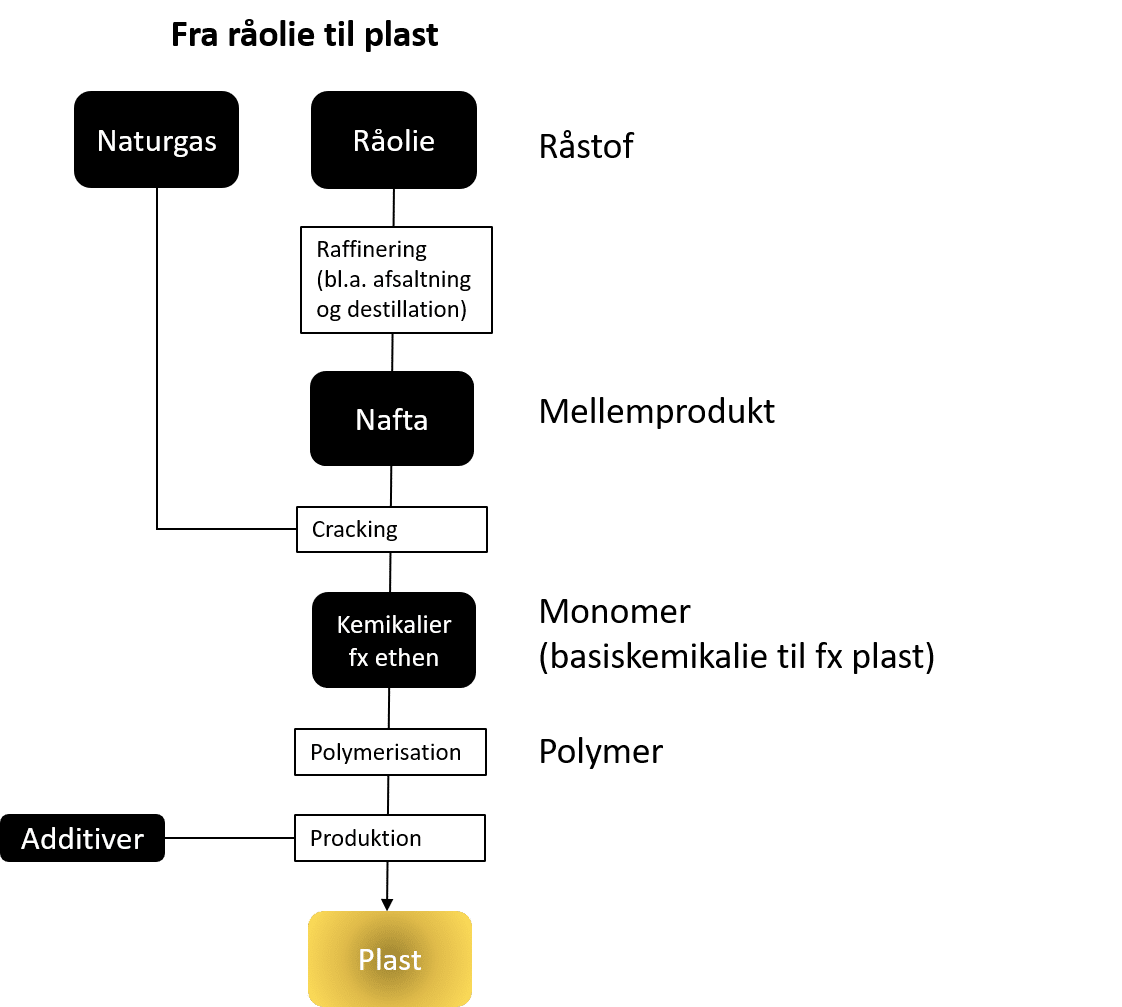
Sådan kommer vi fra råolie og naturgas til de plasttyper, vi anvender i alt fra emballage og tøj til byggematerialer.
Se mere
Opgave 5. Cracking med molekylebyggesæt

Ved hjælp af et molekylesæt skal du modellere, hvordan man kan lave byggesten til plast ud fra cracking. Kig godt på figur 13
a. Byg en model af heptan vist i figur 13.
b. Crack den i overensstemmelse med reaktionsskemaet vist i Faktaboks: Fra råolie til plast, så du får dannet de to produkter.
c. På samme måde som ovenfor, skal du nu selv finde ud af at bygge en anden alkan, og cracke denne, så du får dannet en kortere alkan og en kortere alken.
Se mere
hexan anvendes som opløsningsmiddel, hvor den bl.a. bruges til at udtrække (ekstrahere) spiseolie fra olieholdige frø som solsikke eller raps og sojabønner?
Opgave 6. Hexan og fraktioneret destillation
Hexan er et meget brugt opløsningsmiddel og isoleres fra råolie ved fraktioneret destillation. Kig på figur 12. Hvilken fraktion vil du forvente at finde hexan i, når dets kogepunkt er 69 °C?
Se mere
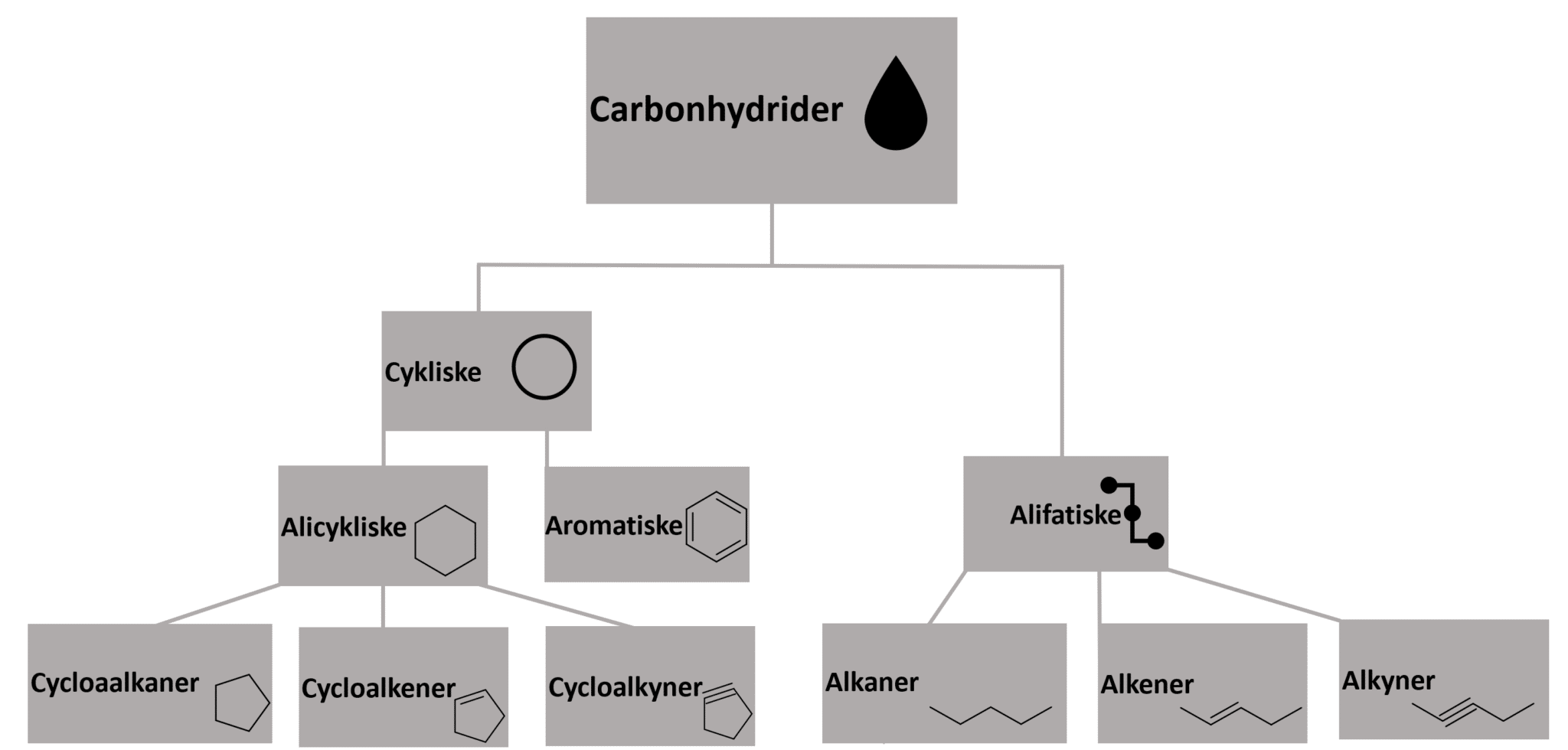
Alkaner er bare én gren af carbonhydriderne, som nedenstående figur 15 viser. Ovenfor har du mødt forskellige kædeformede alkaner. Dem grupperer vi som alifatiske carbonhydrider, sammen med den gruppe, der hedder alkener og alkyner. Nedenfor møder du en alken, der har en dobbeltbinding mellem de 2 carbonatomer. Alkyner er kendetegnet ved, at der er en trippelbinding mellem de 2 carbonatomer. En anden gruppe af carbonhydrider er cykliske forbindelser, hertil hører de føromtalte aromatiske forbindelser.
Ethen er et vigtigt basiskemikalie. Ethen er med til at opbygge plasttypen PE (Poly Ethylen plast), som er den type plast, der fremstilles mest af på verdensplan. Råolie i sig selv indeholder kun ganske små mængder ethen. Derfor dannes ethen fra cracking af alkaner som omtalt i faktaboksen Fra råolie til plast.
Men hvad er ethen?
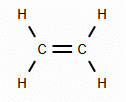
Ethen er et carbonhydrid og tilhører gruppen alkener, der er kendetegnet ved, at der mellem de enkelte carbonatomer er mindst en dobbelt elektronparbinding, som det fremgår af figur 16. Stoffer med dobbeltbindinger eller trippelbindinger omtales som umættede stoffer. Det er fordi, at dobbelt eller trippelbindinger er reaktive, de er det, vi som kemikere kalder en funktionel gruppe.
Alkener navngives som alkaner, men med endelen -en i stedet for -an.
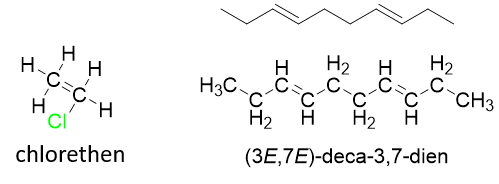
Der kan indgå mere end en dobbeltbinding i en alken, som figur 17 viser. Dobbeltbindinger giver anledning til geometrisk isomeri, det ikke er i fokus her. Chlorethen er et andet eksempel på en alken, der er vigtig i plastproduktionen, den er også vist i figur 17. Chlorethen er med til at opbygge PVC-plast. Som vi skal se på i næste afsnit, så brydes disse dobbeltbindinger, når molekylerne reagerer og danner plast.
Nu kan vi se på, hvordan vi kan danne forskellige typer af plast, da I nu har mødt de byggesten som plast er opbygget af. Der findes over 3.000 forskellige typer plast. Nedenfor skal du møde de hyppigst anvendte.
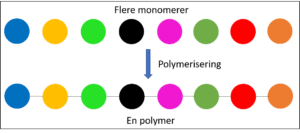
Plast er en syntetisk polymer, som nævnt kort i indledningen. Helt kort er en polymer et større molekyle, der er dannet ud fra monomerer. Polymerer er store molekyler med en molarmase > 2.000 g/mol. Mono betyder en, og poly betyder flere. Polymeren udgøres af sammenbundne monomerer, og monomeren er den gentagne enhed i polymeren. Sammenbindingen af monomerer til en polymer, kaldes så en polymerisering, som illustreret i figur 18.
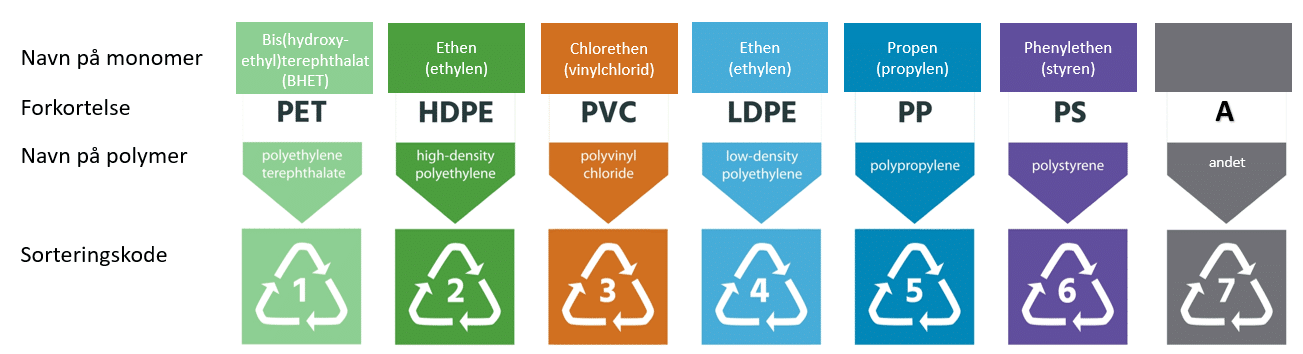
De typer plast, vi anvender allermest, er generelt også dem, der holder kortest tid. Derfor er det netop disse plasttyper, vi skal sørge for at genanvende. I figur 19 er vist de 6 hyppigst forekommende plasttyper, vi anvender i hverdagen. Figuren viser også de tilhørende sorteringskoder.
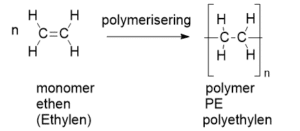
Som modellen i figur 18 viser, dannes en polymer ud fra monomerer. I plast udgøres monomeren af et lille organisk molekyle, der er forskellig alt efter hvilken plasttype der er tale om. Plasttypen HDPE og LDPE består af polymeren polyethylen (PE). Den er dannet ved en sammensætning (polymerisering) af monomeren ethen. Den gentagne enhed er altså ethen, som vist i figur 20.
Plast er makromolekyler, altså store molekyler. Eksempler på makromolekyler og opbygningen af plast, polymerer og monomerer er forklaret i You Tube klippet nedenfor (9:32).. Her forklares også hvordan den trinvise polymerisering sker, med afsæt i PVC-plast.
De forskellige typer af monomerer, der er byggesten for de forskellige plasttyper (polymerer), er forklaret i You Tube klippet nedenfor (32.40) fra Astra. Her præsenteres du for de hyppigste typer af plast, deres kemiske opbygning og funktion. Med brug af molekylebyggesæt får du en fin indføring i de 7 forskellige plasttyper: PE, PP, PVC, PS, PMMA, PA og PET.
Opgave 7 Kædedans og polymerisering
I skal lave en polymeriseringsreaktion.
Se mere
Opgave 8 Byg en polymerisering af polyethen (PE)


Gå sammen i grupper af 3, 4 eller 5.
Se mere
Opgave 9. Polymerisering og reaktionsskema
Se mere

I forsøget kan du lave din egen hoppebold med husholdningskemikalier. Reaktionen er en polymeriseringsreaktion. Øvelsesvejledningen kan hentes her (indsæt link)
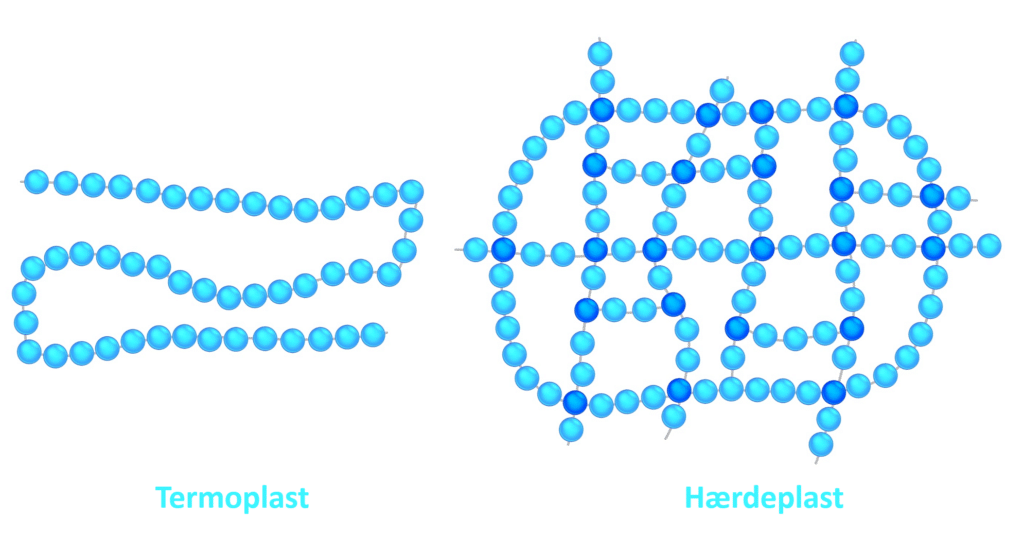
Ofte inddeler vi plast i hærdeplast, termoplast, og elastomerer (fx gummi), da deres egenskaber er ret forskellige. Det skyldes, som forklaret nedenfor, deres forskellige kemiske opbygning, mere end det skyldes forskelle i, hvilke grundstoffer der indgår. Fokus er på hærdeplast og termoplast. Figur 21 er en illustration af forskelle mellem termoplast og hærdeplast. Overordnet kan man sige, at termoplast kun er bundet sammen i 2 dimensioner, mens hærdeplast er bundet sammen i 3 dimensioner.
Termoplast er plast, der kan smeltes og formes igen og igen, når det varmes op. Typisk består termoplast af lange polymerkæder, der ikke er bundet fast til hinanden på kryds og tværs med elektronparbindinger, som angivet i figur 21. Derimod holdes kæderne kun sammen af svage kræfter (såkaldte intermolekylære kræfter). Når plasten varmes op, kan kæderne bevæge sig frit, og materialet bliver blødt og formbart. Når det køler ned, bliver det hårdt igen. Eksempler på produkter vi anvender i hverdagen, som er opbygget af termoplast, er vist i figur 22.
Hærdeplast er plast, der kun kan formes én gang. Når det først er hærdet, kan det ikke smeltes igen. Her er kæderne i polymeren krydsbundede med elektronparbindinger mellem kæderne, som angivet i figur 21. Der dannes et tredimensionelt netværk, som gør plasten meget stærk og varmebestandig. Hærdeplast kan ikke omsmeltes eller opløses igen, men nedbrydes i stedet ved opvarmning. Eksempler på produkter vi anvender i hverdagen, som er opbygget af hærdeplast, er vist i figur 22.
Termoplast udgør ca. 85 % af vores plastforbrug. Termoplast inddeles i yderligere fraktioner, som angivet i figur 22.
Opgave 10. Hærdeplast, termoplast og kemiske bindinger.
Kig på figur 21
Se mere
Som det fremgår af figur 22, er vindmøllevinger typisk opbygget af epoxyplast. Her kan du læse om epoxyplast, og vindmøllevinger. Som det fremgår heraf er meget denne plasttype svært nedbrydeligt, og det besværliggør også at genbruge plasten.
Også tekstiler består af polymerer, enten syntetiske polymerer som plast eller naturlige polymerer som bomuld. Det er i fokus i faktaboksen Kemien i klædeskabet og i forskningsfortællingen Kemien i klædeskabet .
Har du tænkt over hvad der egentlig er i dit tøj? Hvorfor din t-shirts egenskaber varierer alt efter om den er lavet af bomuld eller polyester? En stor del af svaret ligger i tøjpolymerernes kemiske sammensætning – og det er det vi skal kigge på her. Tekstiler kan bestå af enten naturlige eller menneskeskabte fibre eller være en blanding af disse to, se oversigten i figur 23.
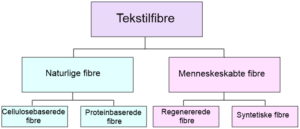
De naturlige fibre kan deles i to grupper: proteinbaserede og cellulosebaserede fibre. Proteinbaserede fibre, som uld og silke, kommer fra dyr, mens cellulosebaserede fibre, som bomuld, kommer fra planter. De menneskeskabte fibre kan også deles i to typer: regenererede og syntetiske fibre. Regenererede fibre laves af naturlige materialer, som først opløses med kemikalier og derefter bliver lavet om til nye fibre. Et eksempel på en regenereret fiber er viskose. Syntetiske fibre bliver lavet af mennesker gennem kemiske processer, ofte ved at bruge olie eller andre fossile ressourcer. Du kender sikkert til polyester, nylon og elastan, som alle er forskellige syntetiske fibre.
Polyester
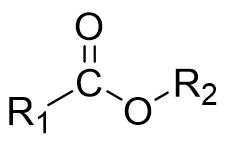
Polyester er den tøjfiber, som udgør den største procentdel af markedet. Faktisk udgjorde polyester 59% af den samlede tekstilfiberproduktion svarende til 77,7 millioner ton i 2024.1 Polyester er faktisk et navn for en række molekyler, som alle består af lange kæder med det der hedder estere, som illustreret i figur 2.
Når vi i dagligdagen taler om polyester henviser vi specifikt til PolyEthylenTerephtalat, PET, se figur 25.
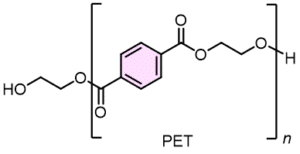
Polyester er billigt at producere, og en af dets egenskaber er, at det er et stærkt og holdbart materiale.
Bomuld
Bomuld er den næstmest producerede fiber og udgjorde 19% af den samlede fiberproduktion i 2024.1 Det, vi bruger til at fremstille bomuld, er de hår, som sidder på bomuldsplantens frø. Bomuld indeholder cellulose, som er en polymer, der er dannet fra monomeren glukose (et sukkermolekyle) og sat sammen i en lang kæde. Cellulose udgør en stor del af plantecellens væg, men det varierer hvor meget cellulose en plante indeholder. Figur 4 viser bomuldsplanten, samt strukturen af cellulose.

Bomuld er populært til tøj, fordi det føles blødt og behageligt mod huden. Polyester og bomuld er altså to eksempler på, hvorfor tekstilfibres egenskaber er forskellige. På samme måde er nylons kemiske sammensætning med til at gøre tøjet slidstærkt, elastan giver tøjet elasticitet, og viskose føles blødt og glat mod huden.
Ofte blander vi de forskellige fibre, så flere af egenskaberne findes i vores tøj på samme tid. Prøv at kigge i det mærke som sidder i dine bukser eller din t-shirt. Min trøje består fx af 46% polyester, 46% viskose, 8% elastan. Hvad er der i dit tøj?

1 kilde: Textile Exchange. Materials Market Report; 2025. https://textileexchange.org/knowledge-center/reports/materials-market-report-2025/
Se mere

Tekstiler og tøj er en vigtig del af vores hverdagsliv, og det kan være svært at forestille sig en verden uden. Produktionen af fibre, som er de helt tynde tråde i vores tøj, er i vækst og i 2024 var den samlede produktion på 132 millioner ton.1 Selvom der findes forskellige genanvendelsesmetoder er det kun omkring 1% af vores tøj som genanvendes fiber-til-fiber, mens størstedelen af det udtjente tøj ender på lossepladsen eller bliver sendt til forbrænding.2 Dette betyder at tøjindustrien både forurener og lægger et pres på vores ressourcer, samtidig med at tekstilindustrien i høj grad følger en lineær model, som er vist i figur 28, hvor tøjet bruges i en kortere periode og derefter bortskaffes.

Forskere arbejder i dag på at finde løsninger til, hvordan tekstilindustrien kan blive mere cirkulær, så fibrene efter brug kan genanvendes i andre tekstiler af samme eller måske endda bedre kvalitet. Jeg er selv en af de forskere. I løbet af min studietid har jeg været en del af et hold i Troels Skrydstrups forskningsgruppe på Institut for kemi, AU, som arbejder med, hvordan man selektivt kan nedbryde elastanpolymeren i tekstiler af blandede fibre, så de andre fibre kan genanvendes.

Elastan er et eksempel på en syntetisk fiber(altså en fiber, som primært er baseret på monomerer fra fossile, ikke-fornybare kilder). Den bruges i tøj, fordi den kan strækkes meget og gå tilbage til sin oprindelige form. Elastan er en polymer, som indeholder to dele (segmenter):
Selvom det er en smule komplekst, kan du holde øje med strukturen af den alifatiske diol, som indeholder hydroxylgrupper i en kæde, den aromatiske enhed som er et eksempel på en cyklisk carbonhydrid, og diaminen, som indeholder to nitrogengrupper. Disse elementer er vist i figur 29

Det er sammensætningen af de to segmenter, der giver elastan sin elasticitet. Elastan bliver lavet i to trin. Først dannes en præ-polymer ved reaktionen mellem et stof, der indeholder aromatiske enheder (MDI) og lange kæder af alifatiske dioler. Herefter reagerer præ-polymeren med et kort molekyle (en diamin), der fungerer som kædeforlænger, hvilket er vist i figur 30.
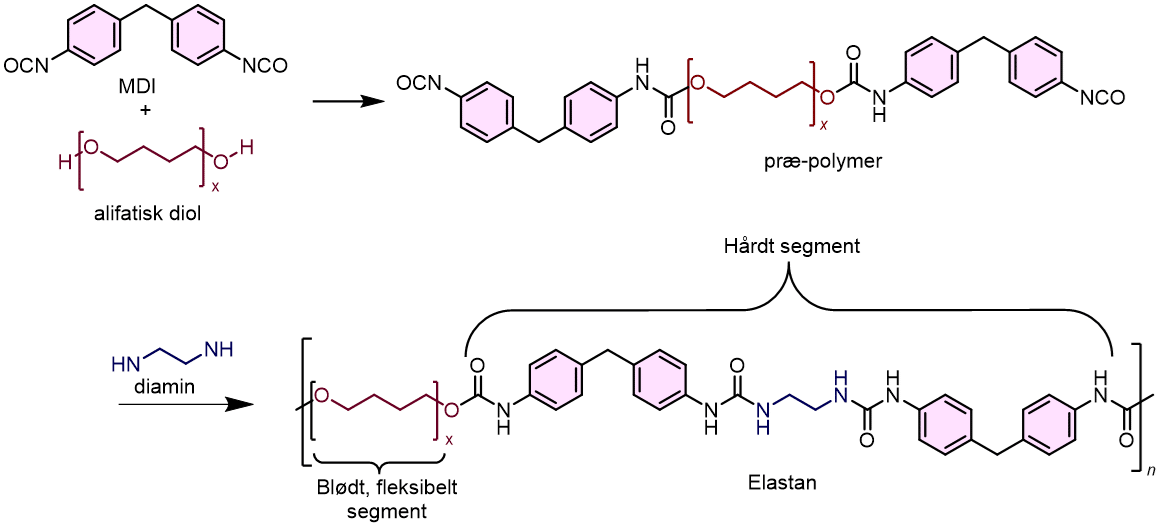
Selvom elastan kun udgør 1% af den årlige tekstilfiberproduktion, bruges den i mange tekstiler som en komponent, der giver strækbarhed, holdbarhed og komfort. Desværre komplicerer det genanvendelsesprocessen, når fibre blandes sammen.
Jeg og andre forskere i Troels Skrydstrups forskningsgruppe har udviklet en metode, hvor vi ved at bruge en alkohol som opløsningsmiddel og små mængder base (som katalysator) kan nedbryde elastan i nylonstrømper uden at nylonfibrene skades, ved en temperatur som ikke kræver alt for meget energi. Dette er vist i figur 31. Fordi elastanpolymeren reagerer med alkoholen kaldes en sådan reaktion for en alkoholyse. For at sikre os, at elastanen blev fjernet fra nylonstrømperne, blev der taget SEM-billeder af strømperne før og efter reaktion. SEM står for scanning-elektronmikroskopi og her bruges et meget kraftigt mikroskop, der bruger elektroner i stedet for lys, så man kan se meget små detaljer. Billederne viste at elastanfibrene blev fjernet ved reaktionen og at nylonfibrene ikke tog skade, men blev lidt løsere, når elastanen ikke længere holdt dem sammen.
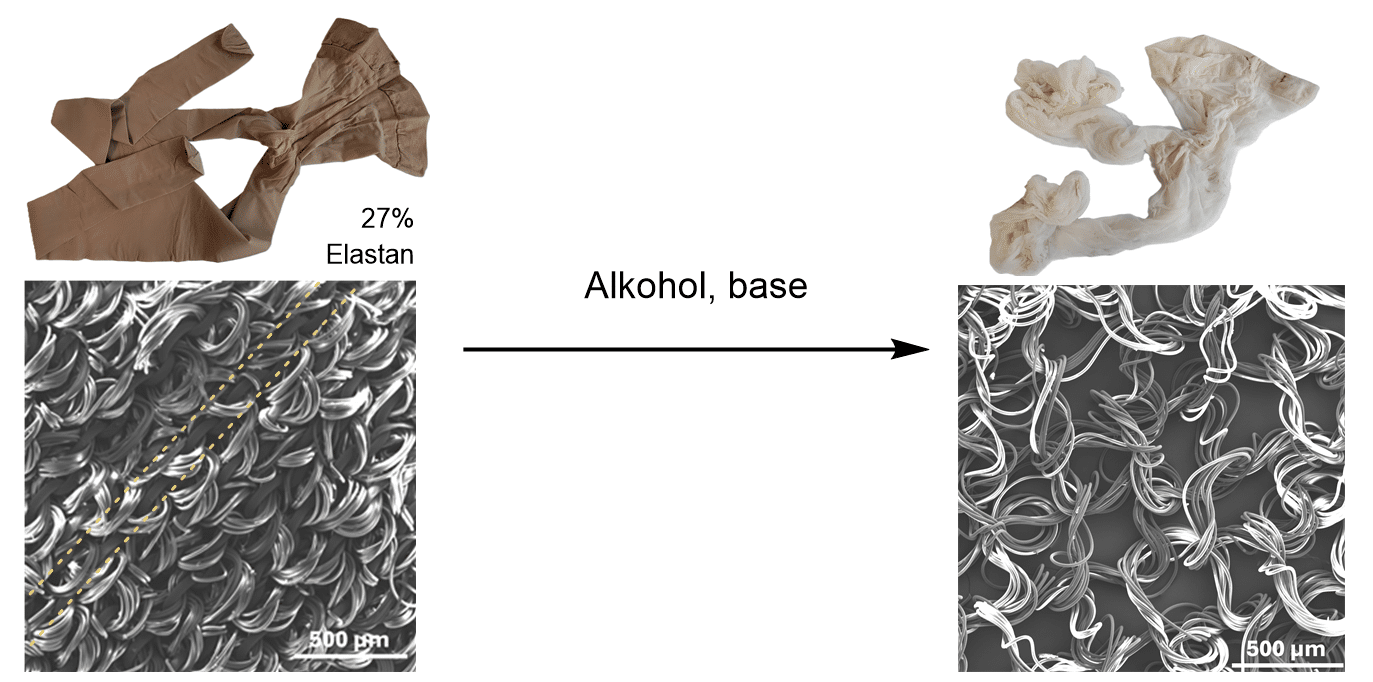
Selvom det er lykkedes at fjerne elastan fra nylonstrømper, er der stadig lang tid, før dette kan implementeres i industrien, da metoden skal udvides til flere forskellige fibertyper, og det skal undersøges, om man kan lave alkoholysen på større mængder tekstil, så det på sigt kan bruges i industrien.
Kilder:
1 Textile Exchange. Materials Market Report; 2025. https://textileexchange.org/knowledge-center/reports/materials-market-report-2025/.
2 Ellen MacAthur Foundation. A new textiles economy: Redesigning fashion’s future; 2017.
Se mere
Som du efterhånden kan se, er plast ikke bare plast. De plasttyper I har mødt er petrokemiske, men plast kan også baseres på biomasse i stedet for råolie.
De plasttyper, der tidligere er præsenteret, kan ikke bare lige nedbrydes til de byggesten de består af, og heller ikke nedbrydes i naturen. Men de kan genanvendes.
Bioplast blev også nævnt tidligere. Måske har du hørt om bioplast andre steder også? Men hvad er bioplast?
Begrebet bioplast er ikke klart defineret. Man skelner typisk mellem:
En plasttype kan godt have petrokemisk oprindelse, og samtidig være bionedbrydelig. Biobaseret plast kan ikke have petrokemisk oprindelse.
Det gode spørgsmål er, om bionedbrydelig plast så kan nedbrydes i naturen?
Nej. Bionedbrydelig plast kan heller ikke lige nedbrydes i naturen. Bionedbrydelig plast forudsætter et kontrolleret miljø, hvor fugtighed, temperatur og tilstedeværelse af de rette mikroorganismer, kan nedbryde plasten. Og disse forhold er ikke til stede i naturen, men i industrielle anlæg .
selvom et produkt er deklareret som at være bionedbrydeligt, kan det ikke lige nedbrydes i naturen?
Så bionedbrydelig plast og biobaseret plast er to forskellige begreber, og er mere præcise ord en bioplast. Men ingen af dem kan nedbrydes i naturen. Figur 32 giver et overblik.
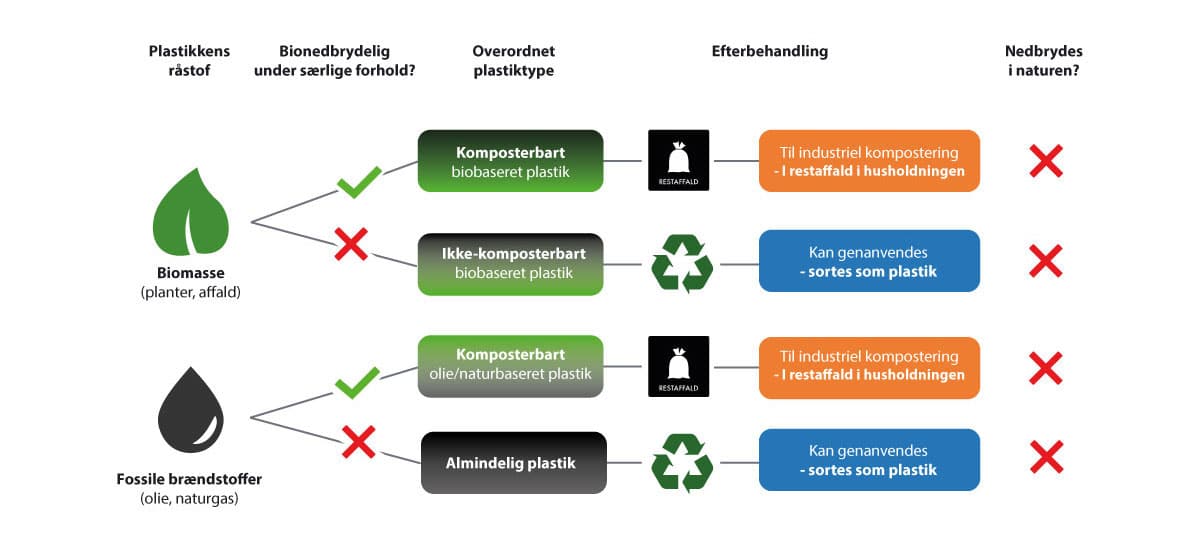
You Tube klippet her opsummerer på 1 min., problematikken omkring bioplast.
Helt så simpelt er det alligevel ikke. For så er der blandingsprodukterne. Som for eksempel den grønne pose man mange steder bruger til bioaffald, eller måske din sweater.
Det ser ud til, at bionedbrydelig plastik ikke helt er vejen frem for grøn plastikomstilling herhjemme. Grøn omstilling for plast bør tage afsæt i at:
Sidste punkt er i fokus i forskningsfortællingen nedenfor: Hvordan kan man lave til biobaserede kemikalier, der kan bruges som byggesten til plast?
![]()
Kan man lave holdbart og genanvendeligt plast fra plantemateriale? Det er et af de spørgsmål, vi skal se på her.
Måske har du hørt om biobrændstof? Hvor man omdanner biomasse (fx halm eller rapsolie) til brændstoffer (fx bioethanol eller biodiesel)? Mange steder går man væk fra idéen om biobaseret brændstof, fordi det bedre kan betale sig at elektrificere, som beskrevet her (i afsnit 3 hvorfor elektrificere?).
I stedet for biobrændstof er fokus på at omdanne biomasse til kemikalier, der så kan indgå i produktionen af fx plast. Det kunne man kalde biokemikalier, og det forsker Christian Marcus Pedersen i.

Christian er professor i organisk kemi på Kemisk Institut Københavns Universitet. Bredt sagt er hans forskning i organisk kemi inden for områder som kulhydratkemi og medicinalkemi. Ligesom mange andre kemikere anvender Christian Machine Learning, fx når der skal udvikles nye kemiske reaktioner og findes nye lægemidler. Christian underviser i en række kurser på universitetet, bl.a. kurset Grøn og bæredygtig kemi.
”Der er mange muligheder for at lave grønnere, mere klimavenlige alternativer til de petrokemiske kemikalier” forklarer Christian. ”Nogle af dem er, at danne nye biobaserede kemikalier, der kan være byggesten for nye typer at plastpolymerer, der ligner de petrokemiske stoffer, har nogenlunde sammen egenskaber, men er grønne alternativer. Vi er særligt interesserede i at anvende biomasse, der består af kulhydrater, som fx cellulose, der ikke er fødekilde for os mennesker” supplerer Christian.
Biomasse er den samlede masse af dyr, planter og andre levende organismer. I forskningsfortællingen her er fokus på biomasse fra planter. Kulhydrater omtaler vi i gymnasiet som carbohydrater.
Christian forsker bl.a. i, hvordan man kan udnytte cellulose, der er en polymer og et makromolekyle, som basis for en række almindelige kemikalier til produktion af plast. At det netop er biomasse baseret på cellulose er ikke tilfældigt. Det er den organiske forbindelse, der er mest af på jorden, og så er den som udgangspunkt ikke menneskeføde.
Christian har været involveret i forskning i en ny type biobaseret plast. Christian fortæller:
”Lige nu produceres en helt ny type plast, kaldet PEF-plast i stor skala, altså til industriel produktion. PEF-plast, er plast opbygget af polymeren PolyEthylenFuranoat (PEF). Biomassen er et carbohydrat, nemlig sukkeren fructose.
Omdannelsen af fructose til PEF-plast er illustreret i figuren nedenfor i figur 33.
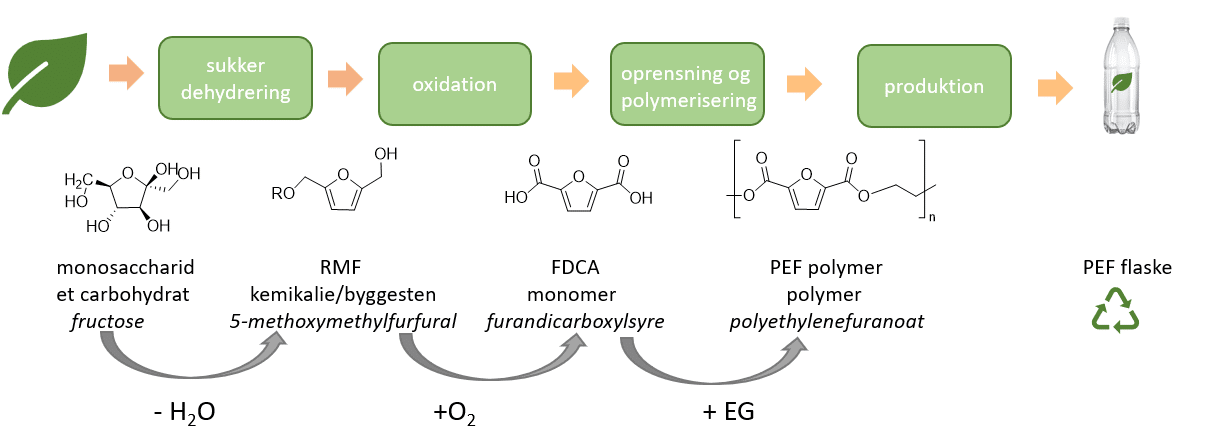
Colaflasker baseret på PEF i stedet for PET er som sagt allerede i produktion. PEF-plast er lige så stabilt som PET-plast. PEF er baseret på carbohydratet fructose, men der er udsigt til at det kan dannes fra cellulose i stedet for”, fortæller Christian
PEF-plast passer ind i vores genbrugssystem for plasttypen PET og vil derfor kunne genanvendes. Så til det indledende spørgsmål i starten af forskningsfortælling er svaret ja, man er på vej.
Der er mange måder at måle bæredygtighed på. Hvis man kigger på såkaldte livscyklusanalyser, viser internationale undersøgelser1, at PEF-flasker er mere bæredygtige end konventionelle PET-flasker:
kilde: 1 https://www.emballagefokus.dk/lca-resultat-bioplasten-pef-overgaar-den-klassiske-pet/).
Se mere
Opgave 11 Biobaseret plast PEF

Se mere
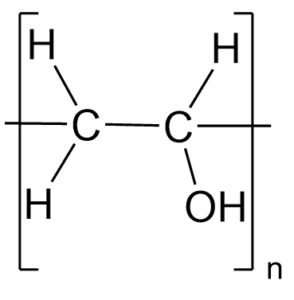
Nogle få plasttyper kan nedbrydes ret nemt, som fx plasttypen PVA, vist i figur 34.

Polyvinylalkohol (PVA) er en termoplast med petrokemisk oprindelse. Du finder PVA som film omkring opvasketabletter, se figur 34. PVA er vandopløselig og bionedbrydelig, og den opløses i opvaskemaskinen. Strukturen af polymeren, der udgør PVA er vist i figur 35.
Opgave 12 PVA
Kig på figur 32
Se mere
Biobaseret plast fra kartoffelmel: Testoteket har lavet en øvelsesvejledning, så du selv kan lave bioplast. Find den her.
Biobaseret plast fra mælk: DTU har lavet undervisningsmaterialet Energi på lager, hvor du bl.a. kan finde denne øvelsesvejledning, hvor man kan lave plast af mælkeproteiner.
Ovenstående 2 øvelser til plastproduktion anvender biomasse, der faktisk er mad. Det afstedkommer nogle etiske problematikker og er ikke vejen frem for biobaseret plast. Men forskning og udvikling af biobaseret plast er ikke så langt endnu og man skal jo starte et sted. Se mere i forskningsfortællingen Hvordan kan man lave til biobaserede kemikalier, der kan bruges som byggesten til plast? .
Vi sorterer i dag (2026) vores affald i 9 fraktioner hjemme i husholdningerne. En af dem er plast. Plast fra husstanden og genbrugsstationen køres herefter til sorteringsanlæg, hvor plasten sorteres yderligere, typisk i 7 forskellige fraktioner, vist i figur 22, inden den sendes videre til forskellige genanvendelsesanlæg.

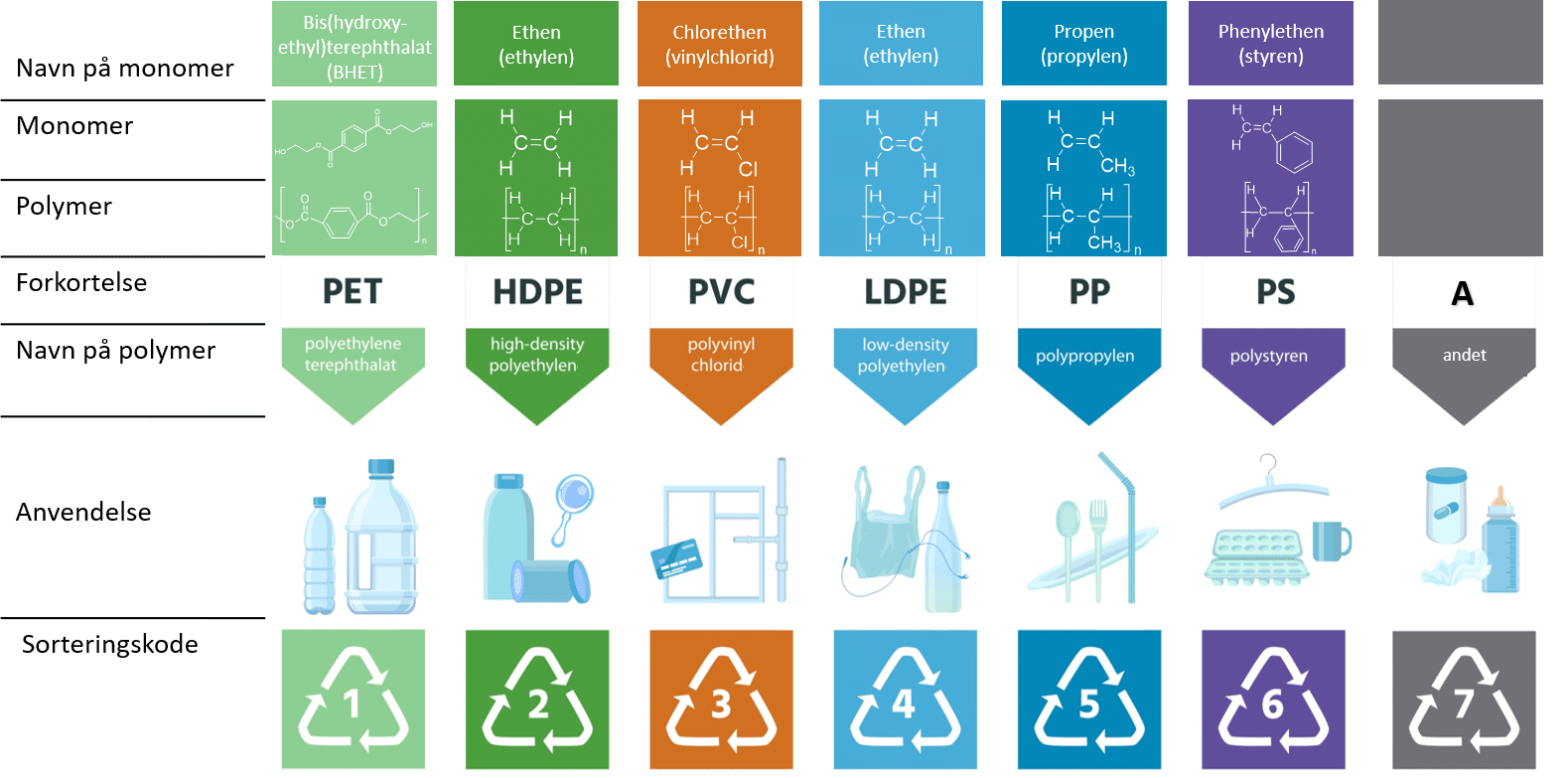
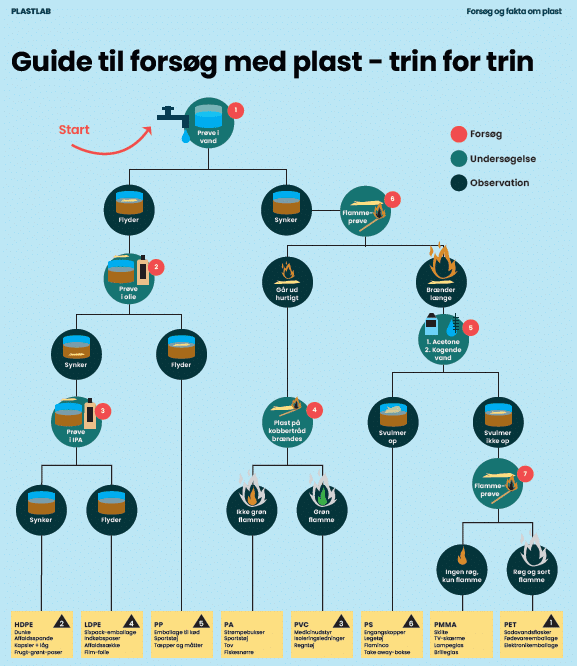
I forsøget her kan I identificere de fraktioner vist i figur 36, samt plasttyperne polyamid (PA) og polymethylmethacrylat (PMMA), der i figur 36 tilhører fraktion 7: Andet. Polyamid indgår i tekstiler, fx strømpebukser og sweaters, mens polymethylmethacrylat ofte omtales som akryl og indgår i bl.a. plexiglas. Undervejs laver i systematiske undersøgelser og observationer, som illustreret på figur 37.
Se øvelsesvejledning her (Indsæt link når det er klart)

Lad os først slå fast at genbrug er, når et produkt bruges til det samme igen. Et eksempel er genbrugstøj. Genanvendelse betyder derimod, at plastmaterialet omdannes til en ny råvare, der derefter kan bruges i produktionen af nye produkter igen. Et eksempel er plastemballagen fra mad, der smides i container til plastaffald. Emballagen bliver sorteret, vasket og genanvendt til en ny råvare, der kan bruges i produktionen af samme plasttype.
Før du læser visere bør du overveje hvad der er bedst (altså hvad der har den mindste klimabelastning, og giver mindst affald). Genbrug eller genanvendelse? Vi vender tilbage til det nedenfor.
Når man i dag genanvender det indsamlede plast, sker det primært mekanisk. I en mekanisk genanvendelse fastholdes strukturen af plastpolymeren. Polymeren forbliver intakt og nedbrydes ikke (i nævneværdig grad). Plastaffald fra industri og husholdninger sorteres typisk i yderligere 7 forskellige fraktioner, som omtalt ovenfor og vist i figur 36. Plast fra hver fraktion deles i mindre stykker ved fx knusning. Derefter vaskes det, og i nogle tilfælde omsmeltes det til granulat, der så kan bruges til nye produkter.
Mekanisk genanvendelse er i dag den mest udbredte form for genanvendelse. Et eksempel er plastaffald af typen PET-plast. Ved en mekanisk genanvendelse kan det altid kun blive til PET-plast igen, fordi polymerstrukturen forbliver intakt i genanvendelsesprocessen. Ulempen ved mekanisk genanvendelse er, at kvaliteten bliver dårligere hver gang. For PET gælder det, at man typisk kun kan genanvende det mekanisk ca. 3-4 gange, herefter er kvaliteten for dårlig, formentlig fordi polymeren er blevet kortere eller beskadiget.
Ofte er man derfor nødt til at tilsætte en smule nye kemikalier i genanvendelsen, da polymerkæden nedbrydes gradvis, ligesom der skal tilsættes additiver for at få de rigtige egenskaber. Derfor er det sjældent mere end 94-98 % genanvendt materiale i et givent produkt.
Ved en kemisk genanvendelse af plast nedbrydes polymerstrukturen i plasten. Plasten nedbrydes til mindre bestanddele som fx til monomerer som igen – potentielt – kan bruges til at fremstille ny plast via en polymerisering.
En kemisk genanvendelsesteknologi kan fx tage afsæt i det modsatte af en polymerisering, nemlig en depolymerisering. Det ser vi nærmere på i 2 forskningsfortællinger: Forskningsfortælling : Recycling af polyester-tekstiler med CO2 som katalysator og Forskningsfortælling: Når kemisk genanvendelse, start-up virksomhed og beskyttelse af havmiljø går hånd i hånd.
Kemisk genanvendelse har tab undervejs og er endnu ikke så langt i sin udvikling. Produkterne fra kemisk genanvendelse kan blive brugt forskelligt: helst i form af monomerer til fremstilling af ny plast, eller som et andet råstof i kemikalieindustrien. Andre gange ender det dog som brændstoffer.
Det er svært at genanvende (både mekanisk og kemisk) blandede materialer. Genanvendelse af plastaffaldet forudsætter jo ofte at plastaffaldet er sorteret i bestemte plasttyper. Hvad gør vi så med materialer, der indeholder forskellige plasttyper, eller tekstiler, der indeholder både plast og bomuld? Også det er i fokus i forskningsfortællingen (navn på fortælling med Jiwoong).
Genbrug er bedre end genanvendelse. Men det affald, der slet ikke opstår, er det allermest klimavenlige.
Før plasten sendes til genanvendelse, sorteres plastaffald på højteknologiske sorteringsanlæg, der kan skille polymertyperne og eventuelt farver ad, typisk ved metoder, der anvender infrarødt lys (IR-spektroskopi eller nær IR (NIR)). Nedenfor skal I selv identificere og sortere plast i forskellige polymertyper.

Ji-Woong Lee er lektor i kemi ved Kemisk Institut på Københavns Universitet og er en central forsker ved ”CO₂ Research Center” forkortet CORC. Han arbejder bl. a. på at fange og omdanne carbondioxid. I denne forskningsfortælling fokuserer vi på genanvendelse af tøj med CO2 som katalysator. Vil du lære om, hvordan forskningsgruppen arbejder med CO2-fangst, så se her: Link til CO2 tema

Som omtalt i Faktaboksen: Kemi i klædeskabet er polyester af plasttypen PET. Det er, som tidligere omtalt, en petrokemisk forbindelse, fordi det stammer fra råolie. Det kræver store mængder energi og giver et stort klimaaftryk at omdanne råolie til polyester.
Der er også et andet problem. Tekstilindustrien og den industri, der genanvender materialerne, har svært ved at håndtere blandede tekstiler, der fx består af både bomuld og polyester. De kan hver især genanvendes, men en blanding af dem kan ikke – endnu.
Ji-Woong og hans forskningsgruppe har netop opfundet en metode, hvor carbondioxid, som vi for nemheds skyld her blot omtaler som CO2, kan fungere som en katalysator til at nedbryde polyester i fx tøj.
Forskningsgruppens arbejde ændrer opfattelsen af CO2-molekylets reaktivitet. ”CO2 som molekyle er mere reaktivt og kan bruges til mere, end vi troede. Det er nyt ” forklarer Ji-Woong. ”Der sker hele tiden reaktioner med CO2 i luften, ligesom der hele tiden sker en reaktion med CO2 i vand” fortsætter Ji-Woong. Og det ved vi godt, når vi registrerer, at en mineralvand med CO2 i bruser fordi CO2 reagerer med vand og danner kulsyre. Derfor smager den også lidt mere surt end postevand fra hanen.
Ji-Woong har sammen med andre i sin forskningsgruppe tidligere vist, at CO2 kan fungere som en katalysator til at nedbryde bl.a. nylon. Med udgangspunkt i de resultater har gruppen nu udviklet og taget patent på en praktisk, effektiv og skalerbar metode til genanvendelse af polyester. Det sker ved at nedbryde produktet med en CO2-katalysator og ”strømline” den grønne proces. At processen er skalerbar betyder, at den også kan laves i store mængder i industrien, og ikke kun i små reagensglas i forskningslaboratoriet. Så Ji-Woongs forskning er både grundforskning og anvendt forskning.
”Plast og CO2 har flere ligheder, fx at de begge er carbonbaserede. Begge dele er affald, der hober sig op. Det er særligt tydeligt for os, når plast hober sig op, mens CO₂‑koncentrationen stiger i atmosfæren ” forklarer Ji-Woong. Det underbygges i figur 39.

Nedenfor dykker vi ned i den proces, hvor blandede tekstiler kan recycles, eller mere præcist kan genanvendes kemisk. Metoden er udviklet til genanvendelse af polyester fra blandede tekstiler ved brug af CO₂ som katalysator.
CO2 som katalysator.
Til nedbrydning af de blandede tekstiler kommer CO2 fra noget så uskyldigt som hjortetakssalt. Hjortetakssalt er trivialnavnet (hverdagsordet) for den kemiske forbindelse ammoniumhydrogencarbonat med formlen NH4HCO3. Når hjortetakssaltet opvarmes til over 36 °C, nedbrydes saltet til CO2, ammoniak (NH3) og vand. Det udnytter vi også i bagning, hvor gasserne bliver fanget inde i dejen og gør den luftig. Reaktionen er opskrevet nedenfor.
2) NH4HCO3 (s) → CO2 (g) + NH3 (g) + H2O (l)
Det er smart, for gruppen har fundet ud af at nedbrydning af polyestertekstiler uden nedbrydning af bomuldsfibre netop bedst sker i et let basisk miljø. Der har været mange baser i spil forklarer Ji-Woong. Til spørgsmål om hvordan man finder en base, der ikke også nedbryder bomuld, svarer Ji-Woong: ”Vi prøver dem alle! ” Deres undersøgelser viste, at de skulle bruge en svag base, og det er netop hvad ammoniak er.
”Så hjortetakssaltet er en immobiliseret form af CO2 ” forklarer Ji-Woong. Immobiliseret betyder at CO2 er fastgjort i hjortetakssaltet. ”Og samtidig får vi den base, der er brug for i forsøget” fortsætter Ji-Woong.
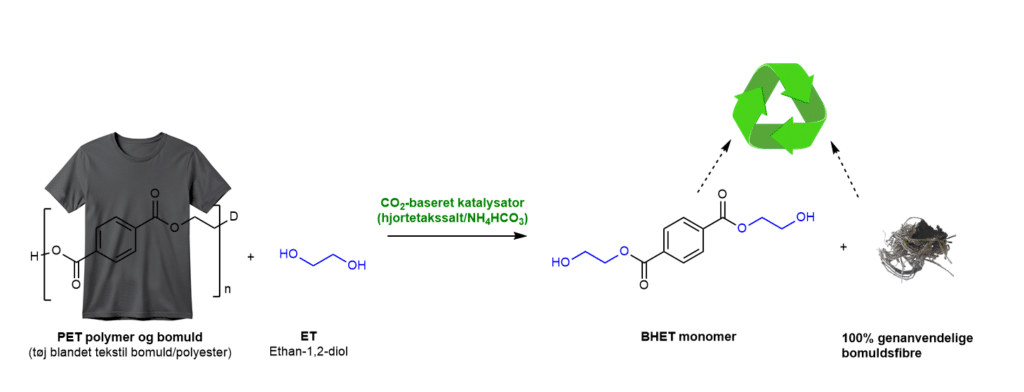
I forsøget med Recycling af polyester-tekstiler med CO2 fra hjortetakssalt, recycles blandede tekstiler, der indeholder både bomuld og polyester, som fx en t-shirt. Forsøget kan laves i kemilaboratoriet på gymnasiet, link til vejledning er her (indsættes nær det er klart)). I forsøget nedbrydes polyester bestående af polymeren PET-plast til monomeren kaldet BHET (bis(2-hydroxyethyl) terephthalat), uden at beskadige bomuldsfibrene, der så kan udvindes fra stoffet og genbruges. BHET kan også genbruges fx i opbygningen af nyt plast. Det er vist i reaktionen figur 40.
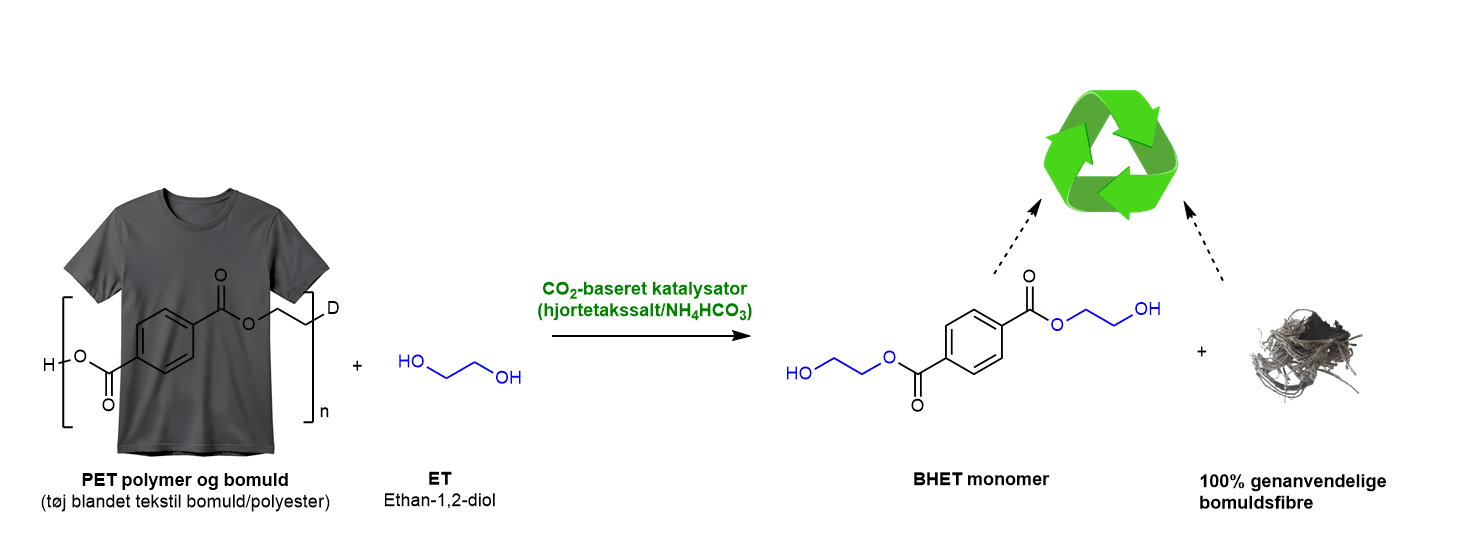
Med den metode kan man nedbryde plasten til monomerer og samtidig bevare bomulden på en simpel og miljøvenlig måde. Udvikling af metoden er der kommet et ”spin out firma” ud af, nemlig firmaet Glyon. Firmaet fokuserer på at adskille og genanvende blandede tekstiler af bomuld og polyester (PET‑plast).
Ji-Woong mener, at EU vil regulere affaldshåndteringen på en måde, så enkelte EU‑lande ikke kan sende deres affald til udlandet, som mange lande gør i dag. ”Det affald ender ofte senere i naturen” forklarer han. Det bringer os ind på noget af det, der driver Ji-Woong i hans forskning : at redde verden. Ovenfor har du mødt ét af hans bidrag!
Se mere
Nu kan I selv komme i gang med at recycle (genanvende) tekstilaffald, der består af blandede tekstiler, både bomuld og polyester. Polyester består typisk af PET-plast. CO2 er med til at katalysere processen, og den får vi fra bageingrediensen, hjortetakssalt, der i virkeligheden bare er NH4HCO3.
Se øvelsesvejledning her (Indsæt link når det er klart).
Du skal møde Shriaya Rütershoff. Hun har været med til at udvikle forsøget ”Recycling af polyester-tekstiler med CO2 fra hjortetakssalt”, som I selv kan lave i kemilaboratoriet, se mere her.

Shriaya er kemiker og ansat på Kemisk Institut ved Københavns Universitet. Hun har arbejdet med polymerkemi gennem sin uddannelse. Hun lavede sit ph.d.- projekt om ”CO2-aktivering af molekyler” igen et eksempel på, når CO2 går fra klimasynder til byggesten, som også er beskrevet i temaet her.
Shriayas arbejde indebærer blandt andet at kommercialisere en metode til kemisk genanvendelse af plastaffald, særligt fra plastflasker, for at muliggøre cirkulær kemi i industriel skala” i stedet for det linære brug-og-smid-væk. Shriaya undersøger, hvordan processen, der blev anvendt i forsøget ”Recycling med polyestertekstiler og med CO2 fra hjortetakssalt” kan opskaleres. Opskalering af processen til industriel implementering betyder at udføre den i en langt større skala end blot 10 g — i stedet 100 kg eller mere — og dermed bygge bro mellem akademisk innovation og anvendelse i virkeligheden.
Shriaya har været med til at stifte en start‑up virksomhed ved navn GLYON, som allerede arbejder på at løse problemet med tekstilgenanvendelse. Det er ikke så enkelt. Processen skal gøres robust, og potentielle fejlkilder skal undersøges. Reaktionen er vist nedenfor:
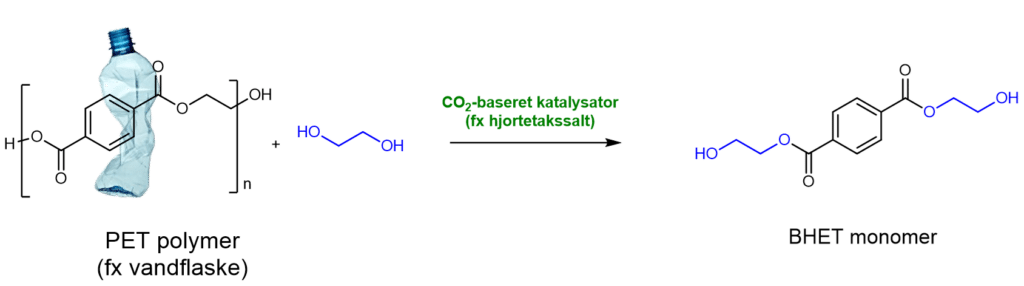
Mere end 90 % af de virksomheder, der genanvender plast i dag, bruger metalkatalysatorer, som potentielt kan bidrage til yderligere metalforurening. Desværre omfatter disse ofte metaller, der står på listen over kritiske råmaterialer.
Shriaya har også undersøgt kemisk genanvendelse af blandede plastprodukter, og af blandede tekstiler – både polyester og elastan, polyester og nylon samt polyester og bomuld. I forskningsfortællingen Kemi i klædeskabet af Inge Kiel Hermanns er fokus netop på at nedbryde elastan-polymeren i tekstiler af blandede fibre se her.
Proceduren nedbryder specifikt polyester og ikke de andre polymerer. Det har store perspektiver for klima og miljø, hvis plast kan genanvendes mere effektivt i fremtiden.
Shriaya har en stor personlig interesse i dette arbejde, da hun har været med til at udvikle metoden gennem flere år. Hun brænder for ”at løse endnu uløste problemer med plastikaffald, og løse "real world problems”, som hun formulerer det.
Mere end 90 % af de virksomheder, der genanvender plast i dag, bruger metalkatalysatorer, der potentielt kan bidrage til metalkontaminering. Desværre anvendes også metaller, der er på listen over kritiske råstoffer (se mere her). Shriaya forklarer at ”ikke-metal katalysatorer, som hun arbejder med er mere grønne. ”
”Metoden med kemisk genanvendelse af plast virker ikke kun på ren plast, men også plastaffald fra naturen” forklarer Shriaya. Nedenfor står hun med en hel kasse plastaffald som frivillige har indsamlet i naturen, og som Shriaya forsøger at genanvende.

Se mere
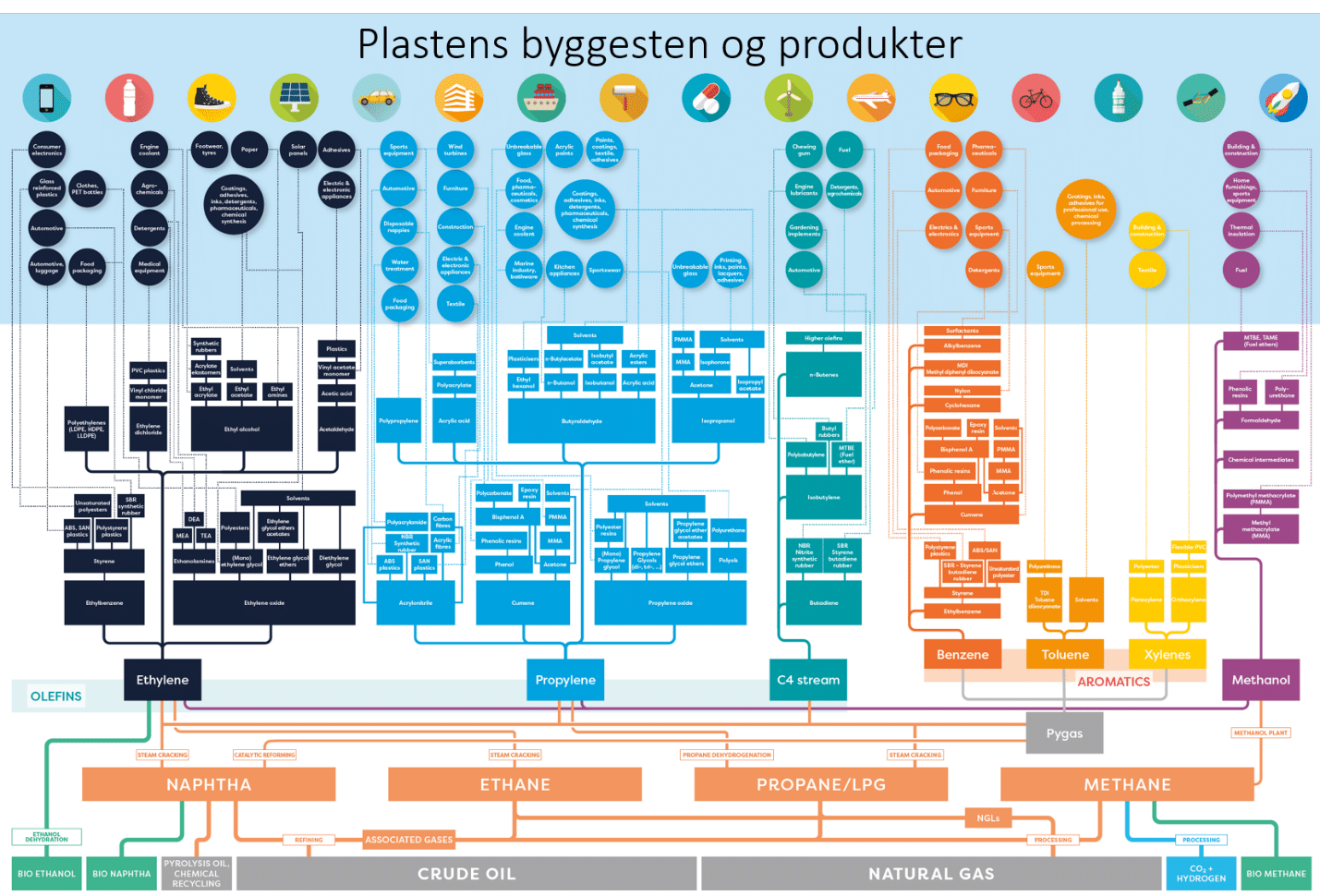
Som tidligere nævnt er der mere en 3.000 forskellige typer plast, og der kommer hele tiden nye plasttyper til. Vi har kigget på en lille håndfuld af dem. Vi har fokuseret på den type plast, der er petrokemisk, og I er blevet introduceret til biobaseret plast. Vi har set på genanvendelse af plast. Vi har ikke haft fokus på additiver i plast eller mikroplast. Figuren nedenfor viser et omfattende kort over plastens byggesten og produkter.
Der er 3 forsøg til temaet:
Find dem under fanen Eksperimentelt